
苏欣 王焱
厦门大学附属心血管病医院
导言
心血管疾病是威胁人类健康的“第一杀手”,位居全球死因首位。长期持续暴露于高水平的低密度脂蛋白胆固醇(LDL-C)会使动脉粥样硬化性心血管疾病(ASCVD)风险增高。50年的证据表明,血浆LDL-C每降低1mmol/L,3年后ASCVD事件相对风险降低20%,随后每年降低1.5%,充分体现降脂治疗在防治ASCVD中的重要地位。
近日,美国心脏协会科学年会(AHA 2022)的“降脂治疗”专场公布了多项血脂领域新型药物的临床研究成果,包括ORION-3研究(PCSK9 siRNA药物Inclisiran)、SHASTA-2研究(APOC3 siRNA药物ARO-APOC3)和ARCHES-2研究(ANGPTL3 siRNA药物ARO-ANG3)。其中,Inclisiran是全球首个用于心血管领域的小干扰RNA药物,已被证实能通过RNA干扰机制在表达水平阻断肝脏前蛋白转化酶枯草溶菌素9型(PCSK9)蛋白的合成,从而上调肝脏LDL受体,降低循环LDL-C水平。目前,Inclisiran已在全球范围内欧盟、英国、美国、中国香港等国家/地区获批,用于在他汀基础上治疗原发性高胆固醇血症或混合性血脂异常的成人患者。之前发表的全球Ⅲ期临床试验(ORION-9、ORION-10、ORION-11)结果说明,在18个月研究期间,Inclisiran每年仅需皮下注射两针,即可长久平稳地降低LDL-C,降幅可达50%以上[1-3]。
而对于临床高度关注的该药长期疗效与安全性问题,本次公布的ORION-3研究是基于2期ORION-1研究,在原有52家中心382例患者基础上,进行为期4年的开放标签延长试验,结果给出了令人满意的答案!
研究背景
Inclisiran作为全球首个小干扰RNA降脂药物,其作用机制是基于生物体内天然的RNA干扰机制,并经过巧妙设计以确保其精准靶向作用于特定基因表达的调控。ORION-3研究是一项为期4年的开放标签扩展试验,旨在评估长期应用Inclisiran的疗效和安全耐受性[4]。它延长自Ⅱ期临床试验ORION-1研究,患有ASCVD或具有ASCVD高危因素(如糖尿病、家族性高胆固醇血症)、且LDL-C水平升高的受试者在完成为期1年的ORION-1研究之后,进入ORION-3的长期扩展研究。
研究方法
ORION-3研究共纳入5个国家52个中心,共计382例受试者,以非随机方式分为两组:(1)Inclisiran治疗组(Inclisiran-only arm)(n=290):ORION-1中分配至Inclisiran组的受试者继续接受Inclisiran治疗,持续4年;②换药组(switching arm)(n=92):ORION-1中分配至安慰剂组的受试者,先接受1年依洛尤单抗治疗(140 mg Q2W),之后转至接受3年Inclisiran治疗。如图1所示。
主要临床终点为第210天时,Inclisiran治疗组较基线(ORION-1研究第1天)的LDL-C变化百分比。其他评估终点包括LDL-C、PCSK9水平和其他血脂指标随时间的变化以及安全耐受性终点等。
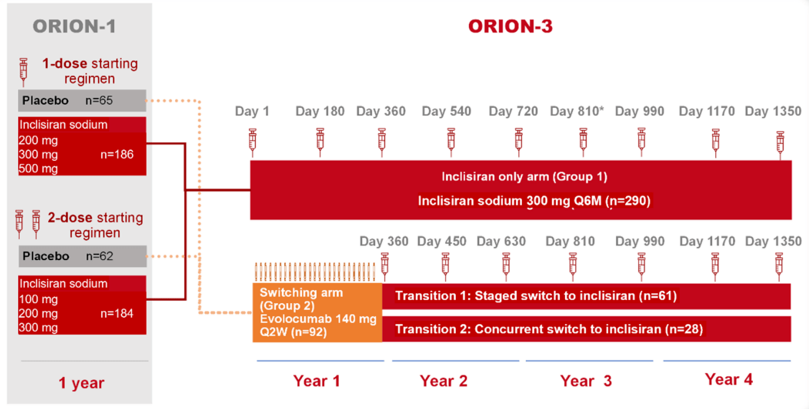
图1 ORION-3研究设计
研究结果
在Inclisiran治疗组,共290例受试者入组,其中233例(80.3%)完成了研究。从ORION-1研究起始至ORION-3研究完成,中位治疗时间为4.5年。患者平均年龄63.3岁,其中50%患者年龄≥65岁。ORION-1研究基线平均LDL-C水平为128.9 mg/dl(3.3 mmol/L)。主要结果包括:
Inclisiran治疗组中,第210天时LDL-C水平较基线降幅为47.5%(95% CI:-50.7~-44.3,P <0.0001,图2),且LDL-C水平在4年研究期间维持稳定,平均LDL-C降幅可达44.2%。在整个研究的任何时点,接近80%的受试者LDL-C水平低于70 mg/dl(1.8 mmol/L),接近93%的受试者LDL-C水平低于100 mg/dl(2.6 mmol/L)。该部分结果重点说明了Inclisiran治疗可强效、持久且平稳地降低LDL-C水平。
除了LDL-C水平外,Inclisiran治疗组中,PCSK9水平较基线平均降低62.2%~77.8%。此外,患者非高密度脂蛋白胆固醇(non-HDL-C)水平和载脂蛋白B(ApoB)水平也持续明显降低。另外,关于ORION-3安全性分析显示:整个4年研究期间,Inclisiran总体安全耐受性良好,未发现新的不良反应。主要药物相关不良事件为注射部位反应,均为轻中度且自限性[5]。
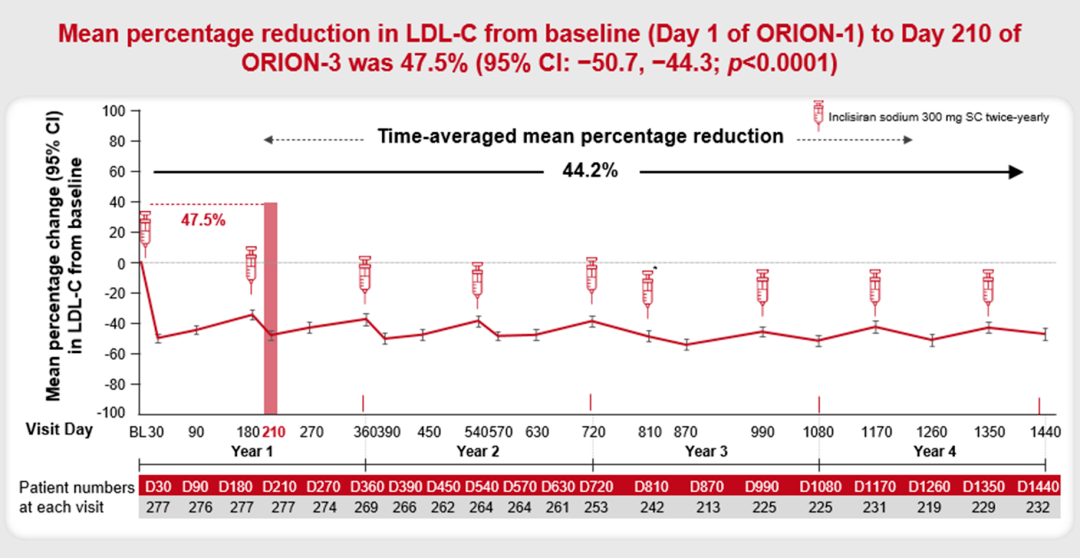
图2 ORION-3研究结果:inclisiran强效、持久、平稳降低LDL-C水平
研究结论
Inclisiran作为首个小干扰RNA降脂药物,既往Ⅲ期临床研究已证实其一年两针,即可长久平稳降低LDL-C水平,同时安全耐受性良好。本次ORION-3研究更是将上述结论从1.5年扩展至4年,为其长期临床应用的有效性和安全性提供了重要依据。
王焱教授点评
LDL已经明确是ASCVD的重要致病因素之一。LDL在动脉壁内修饰、蓄积,导致动脉粥样硬化斑块的形成和进展,斑块侵蚀、破裂进一步引起心血管事件的发生。因此,降低血浆LDL-C是防控ASCVD风险的首要干预靶点,通过调脂治疗降低LDL-C并维持在较低水平,能够稳定和逆转斑块,从而降低ASCVD患者的心血管风险。
Inclisiran作为首个小干扰RNA降脂药物,既往Ⅲ期临床研究已证实1年2针Inclisiran可长久平稳降低LDL-C水平的临床疗效,同时安全耐受性良好。本次ORION-3研究更是将上述结论从1.5年扩展至4年,为其长期临床应用的有效性和安全性提供了重要依据。值得注意的是,能够在长期研究中实现如此稳定的临床疗效和良好的安全耐受性,与Inclisiran作为新一类小干扰RNA药物所独有的RNA干扰机制和N-乙酰半乳糖胺(GalNAc)递送系统脱不开关系。
详细来说,如图3所示,Inclisiran作为一类小干扰RNA药物,其作用机制便是利用了体内天然的RNA干扰现象[6],即外源的双链RNA能够特异性地诱导细胞内与之配对的mRNA的降解。小干扰RNA药物便是这样一类双链RNA,其RNA序列经设计可特异性识别并诱导靶点蛋白的mRNA降解,实现精准的基因表达调控。因此,小干扰RNA药物理论上能够靶向任何致病基因,干预传统无法成药的靶点,且不影响其原有的DNA序列,也不影响其他基因的表达[7-8]。
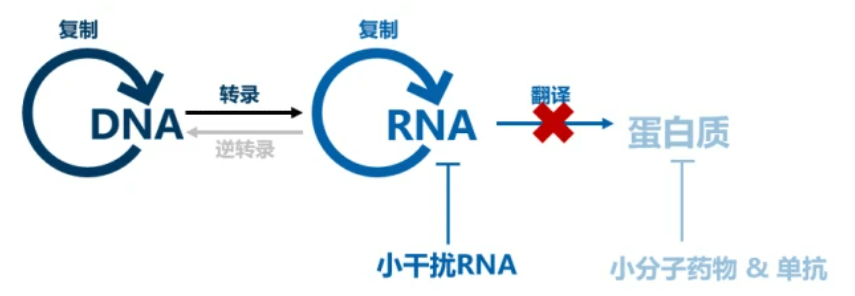
图3 小干扰RNA药物在mRNA层面实现精准的基因表达调控
另外,Inclisiran偶联的GalNAc结构可协助其精准靶向肝脏。GalNAc是一类广泛使用的小干扰RNA递送系统,其作为一类碳水化学物基团,仅与肝细胞表面高度表达的去唾液酸糖蛋白受体(ASGPR)结合[9-11]。因此凭借GalNAc结构,Inclisiran能够实现肝脏的定向摄取,降低其他脏器的潜在暴露风险,实现肝脏PCSK9蛋白的精准干预。
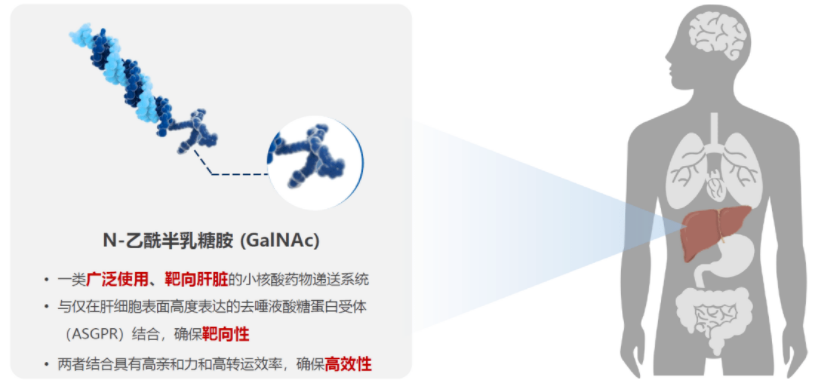
图4 GalNAc协助小干扰RNA靶向肝脏
目前,降脂治疗已逐步迈入精准靶向的小核酸时代。小干扰RNA药物作为一类源自于诺贝尔奖的小核酸药物,可通过RNA干扰机制,在mRNA层面精准调节特定基因的表达,不影响原有的基因序列或其他基因的表达,实现 分子层面的“靶向”;同时,GalNAc递送系统又可使其由肝脏定向摄取,实现 组织层面的“靶向”。
专家简介
王焱
厦门大学附属心血管病医院
厦门大学附属心血管病医院院长,香港大学医学博士、教授、主任医师、博士生导师,美国心脏病学院会员(FACC),欧洲心脏病学会会员(FESC),国际心血管介入学会会员(FSCAI),中华医学会心血管分会委员,中国胸痛中心认证委员会副主任委员,中华医学会心血管病学分会介入心脏病学组副组长,海峡两岸医药卫生交流协会心血管病分会主任委员,国家卫生健康突出贡献中青年专家,具有丰富的临床工作经验,从事心血管系统疾病的诊治,在冠状动脉、外周血管疾病及心脏瓣膜疾病诊治方面有很高造诣。
门诊时间:周四下午
苏欣
厦门大学附属心血管病医院
医学博士,毕业于中南大学湘雅二医院,现就职于厦门大学附属心血管病医院。厦门市高层次卫生人才。擅长心衰、高血压、心肌病诊治和冠心病、心脏瓣膜病的微创介入诊治,美国心脏协会(ACC)FIT,Clinica Chimica Acta、Frontiers in Medicine杂志审稿人,主持多项省、市级课题,参与多项国家级课题,发表SCI论文近40篇,第一作者单篇最高因子12.76分。

