
二尖瓣外科生物瓣置换的患者,远期存在生物瓣叶衰败的风险,当前,经导管二尖瓣瓣中瓣手术(TMVinV)已成为生物瓣衰败的一项常见技术,因其具有创伤小、出血少、恢复快等优势而更受患者青睐。然而,TMVinV技术也存在一定的难度和手术风险,例如左室流出道梗阻(LVOTO)、外科瓣与介入瓣尺寸不匹配(PPM)、房间隔穿刺位点确定、介入瓣膜同轴性调整等问题的考虑都是术前评估的重点。
基本信息
赵某某,女,73岁,体重46Kg,二尖瓣、主动脉瓣位生物瓣置换及三尖瓣成型术后12年,间歇性气短,乏力加重3月。二尖瓣位27#Hancock II,心功能IV级,二尖瓣狭窄关闭不全(重度),三尖瓣关闭不全,肺动脉高压。EDV:61ml, ESV:25ml, EF:58%, FS:31%, SV:36ml.
术前CT评估

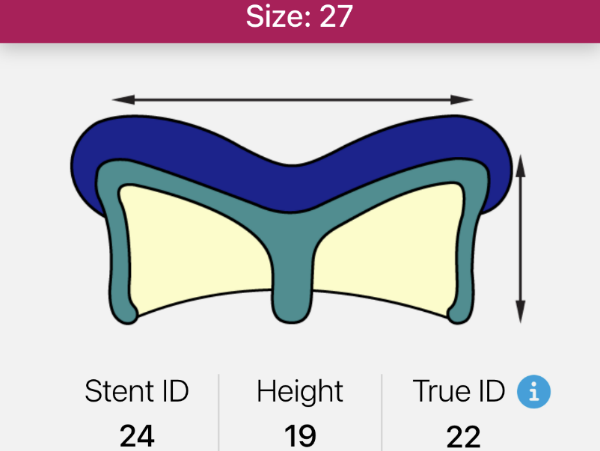

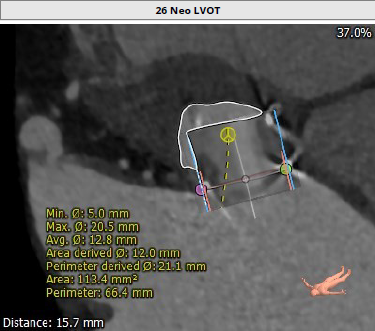
根据27#外科生物瓣,可选择23/26mm SAPIEN 3瓣膜,基于CTA测量瓣环内径面积424.4mm²,模拟植入SAPIEN 3瓣膜,测得Neo-LVOT面积分别为:123.5 mm²(23#),66.4mm²(26#)。


主动脉瓣-二尖瓣瓣环夹角113.9°,左心室小,模拟植入26mmS3瓣膜后瓣架底端距离室间隔4.2mm,术后左室流出道梗阻(LVOTO)风险极高。

房间隔常规穿刺。
术前3D数字模型
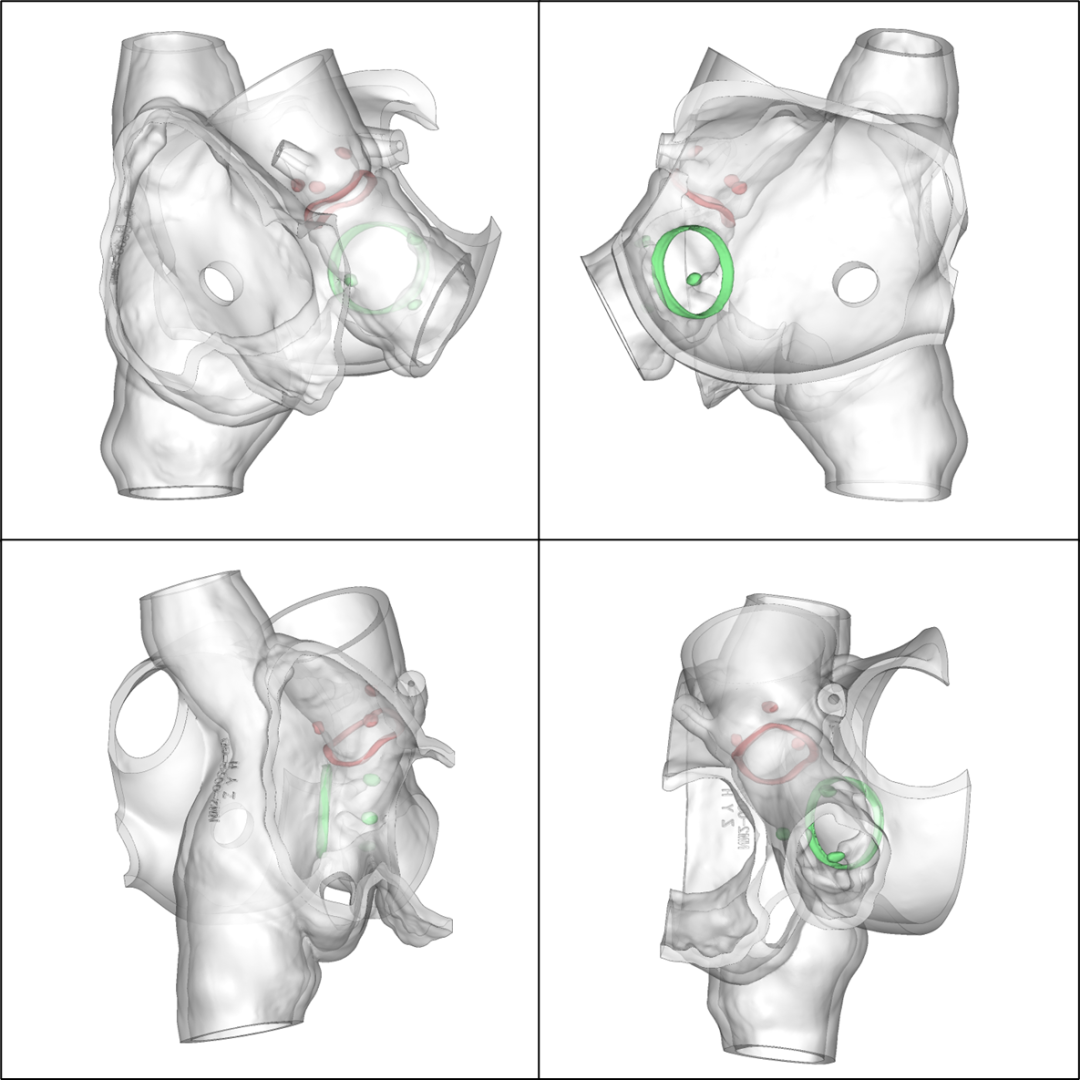
手术策略
术中操作
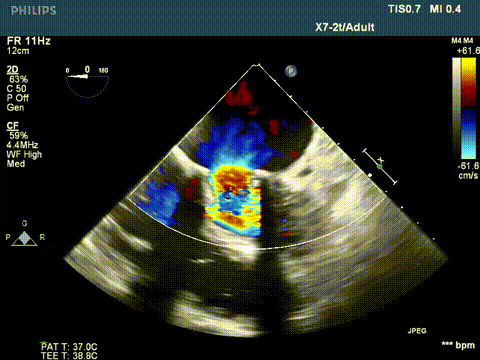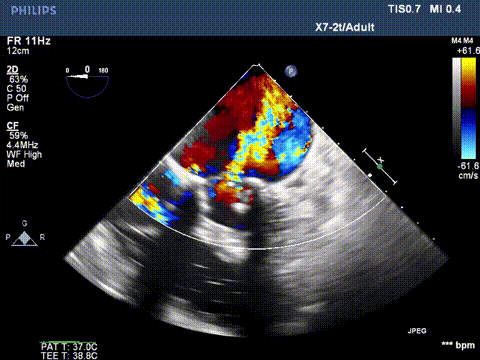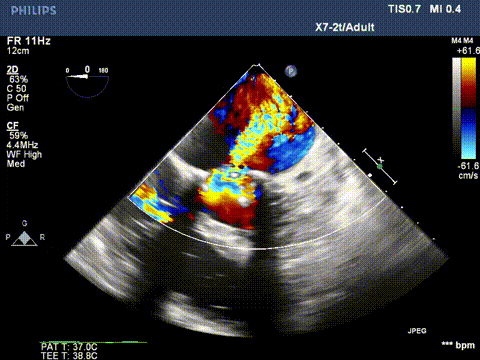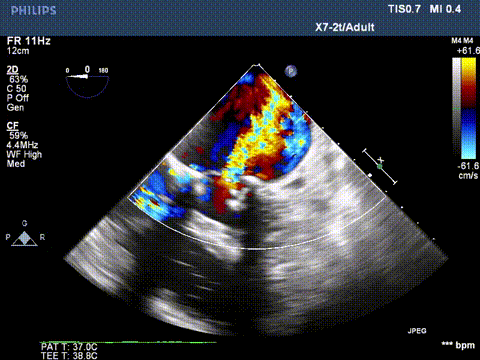
超声显示二尖瓣大量反流
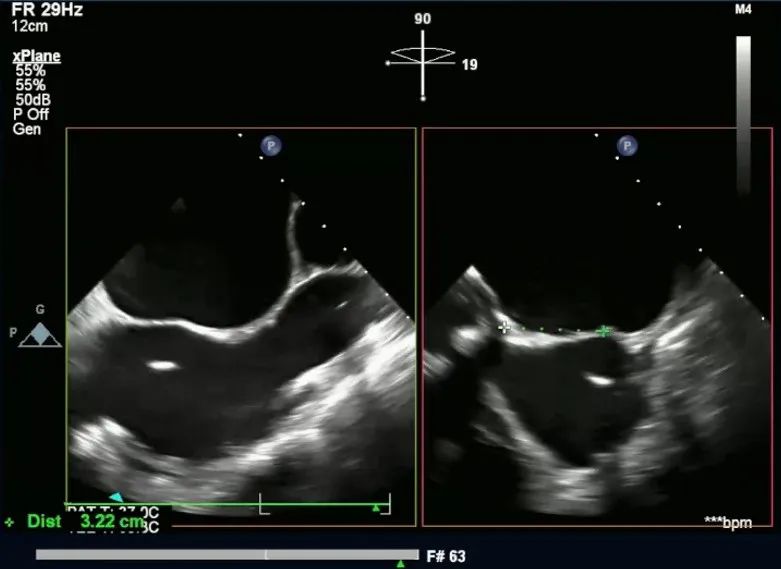
预穿刺点距离主动脉3.22cm

预穿刺点距离下腔1.61cm
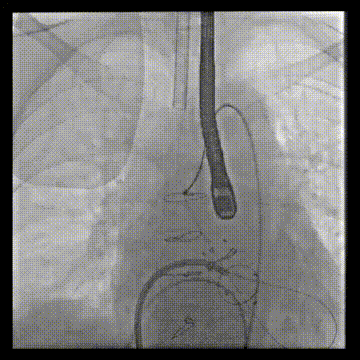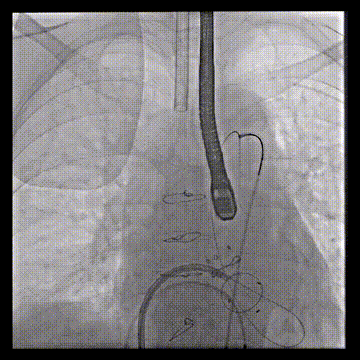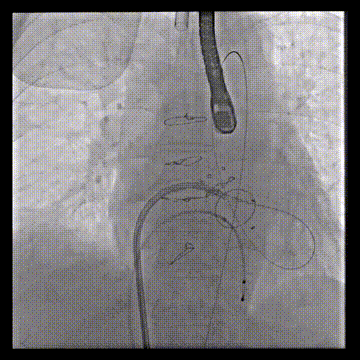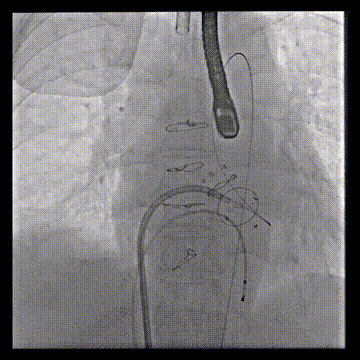
经房间隔二尖瓣跨瓣后,抓捕器在升主动脉抓捕J头泥鳅建立体外化轨道
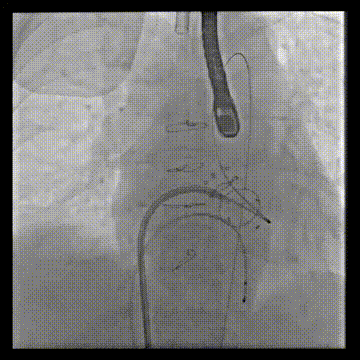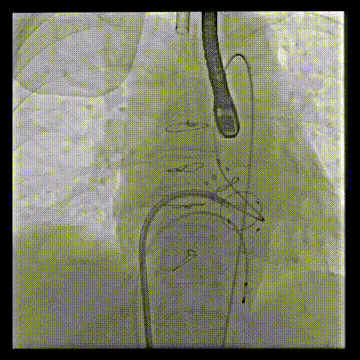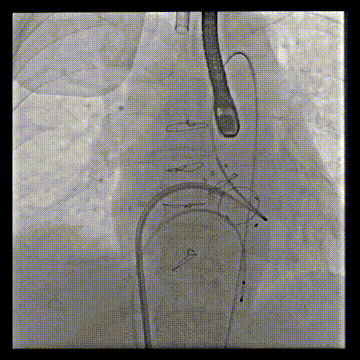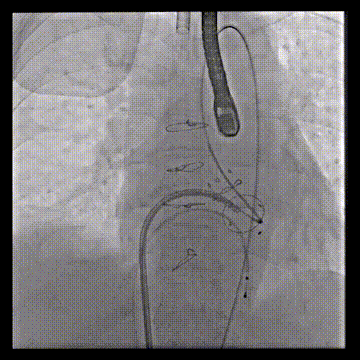
动脉系统送入7F guiding,将guiding套在JR4导管里面,完成整体导管通路的建立
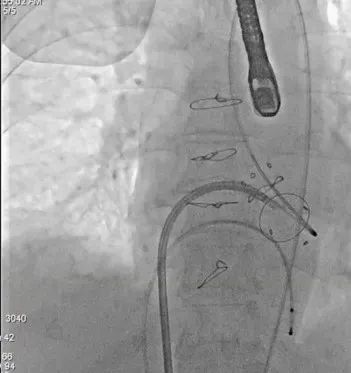
导管轨道交换Astato 300cm 导丝,确认轨道导丝体外化

将JR4与guiding脱离,guiding头端留在心室,JR导管撤回Agilis可调弯鞘管内
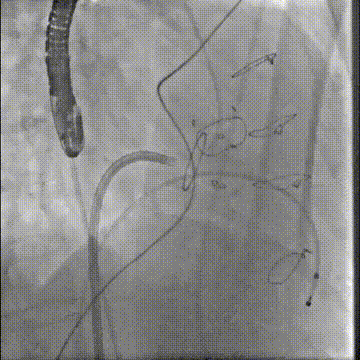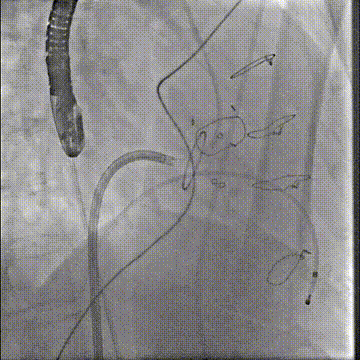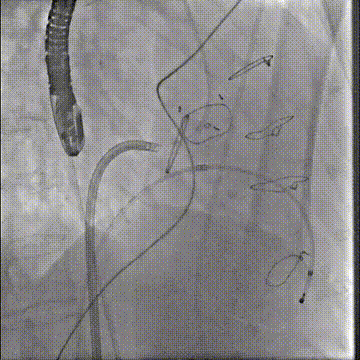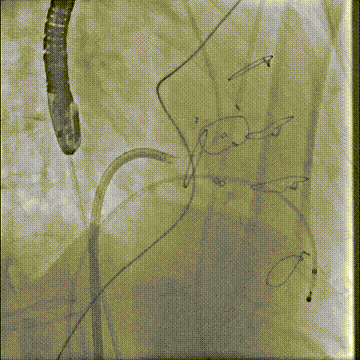
切割前:左室压 110 左房压 58,切割时需要时刻监测左室压,以保证guiding头端在左室内,防止电流接触主瓣
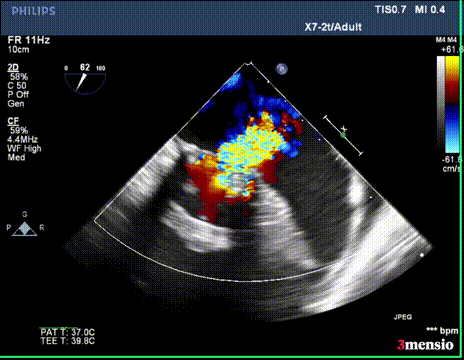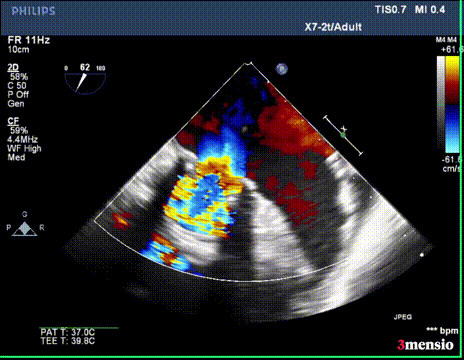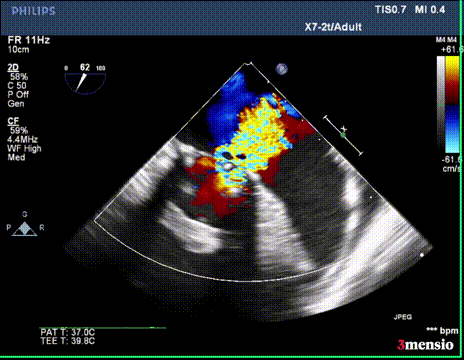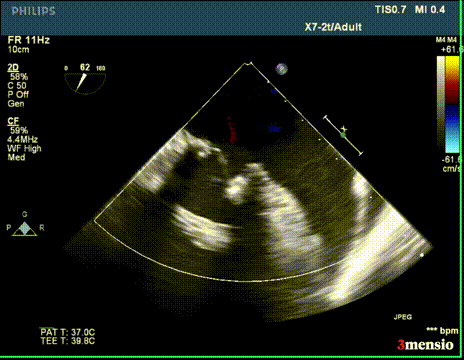
切割前彩超
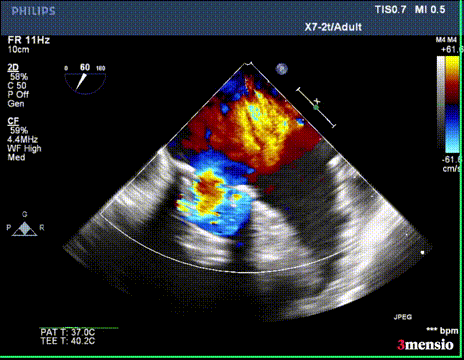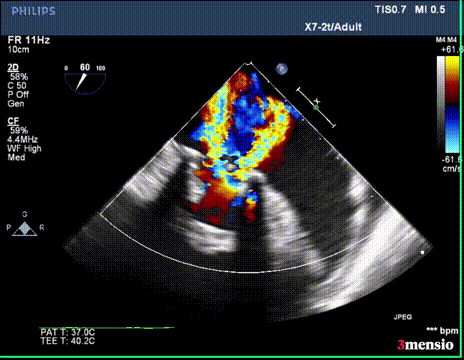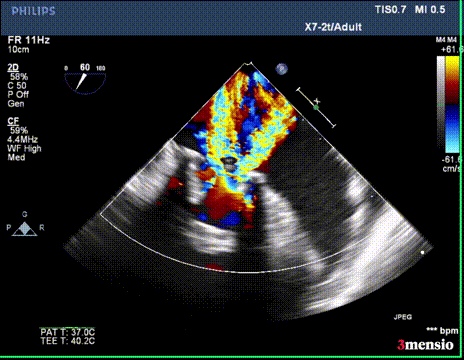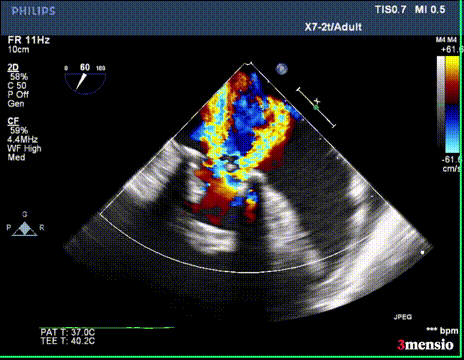
第一次切割后,导丝紧,血流分为两束
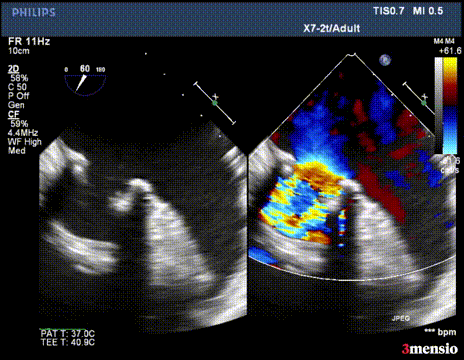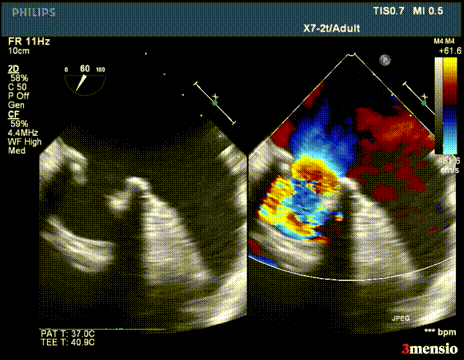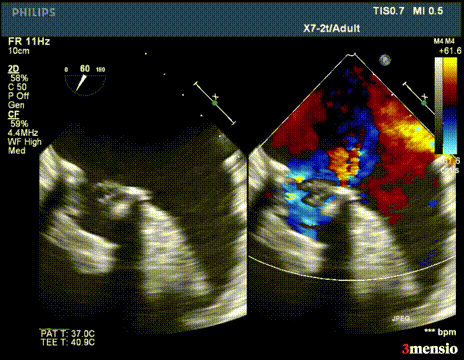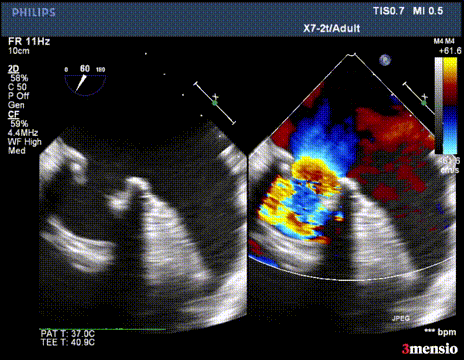
第一次切割后,导丝松,血流又合为一束,但方向改变
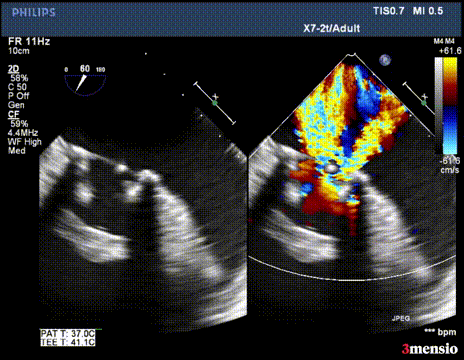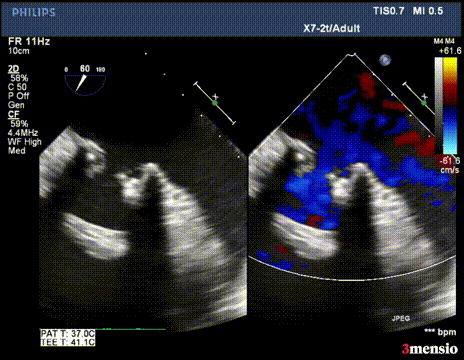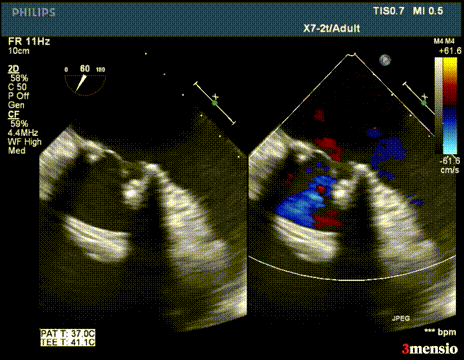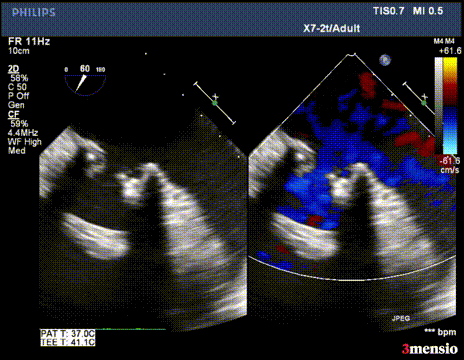
第二次切割后,导丝紧,血流分为两束
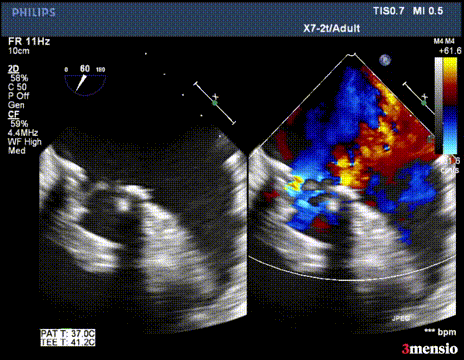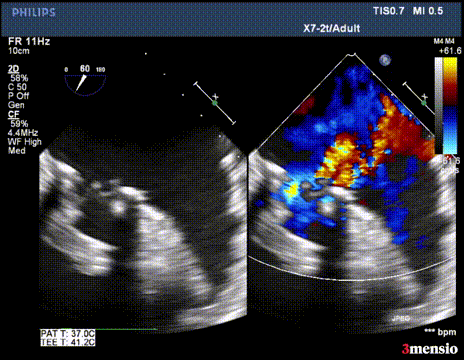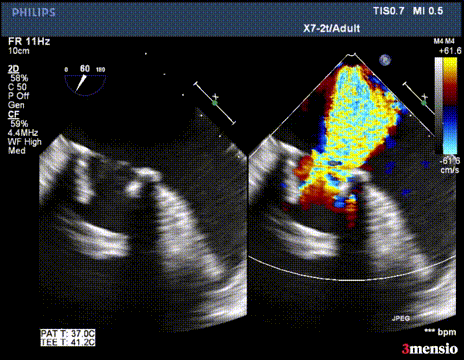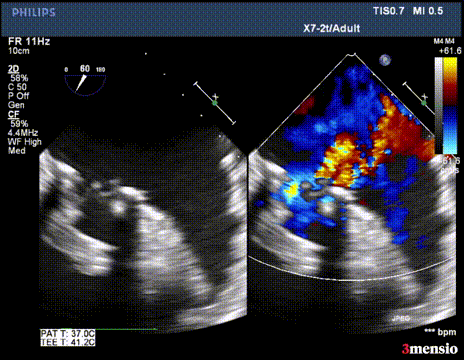
第二次切割后,导丝松,血流已打散
40w的电凝进行切割,2-3次,每次不超过10秒。
切割时拉紧导丝两端,不切割时,放松导丝,解除对瓣叶的压力后,用彩超观察血流方向,切割成功后,可以观察到彩超血流的改变。
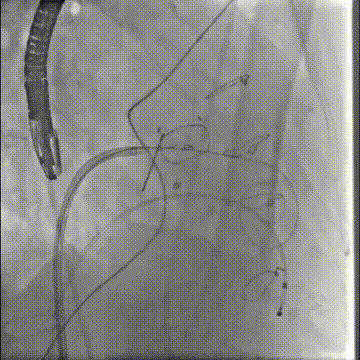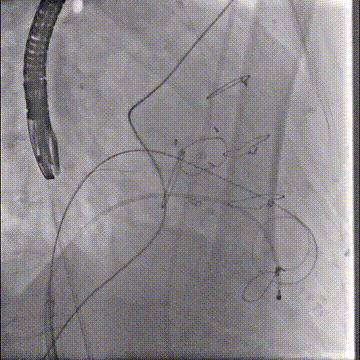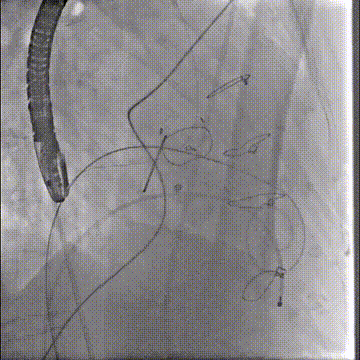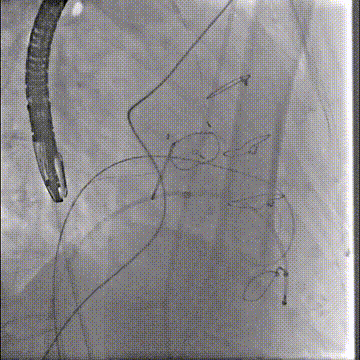
确认Lampoon技术成功后,保留全轨情况下二尖瓣环内放入超硬导丝至左心室
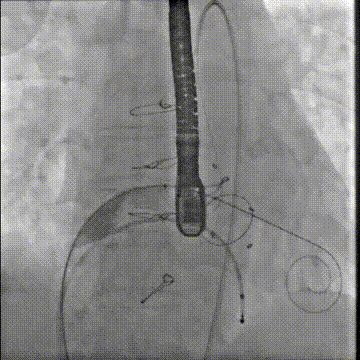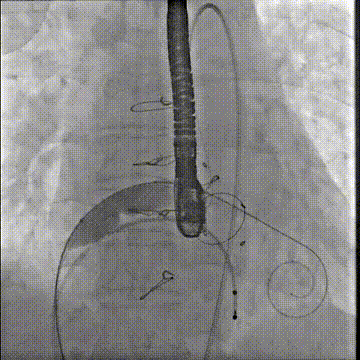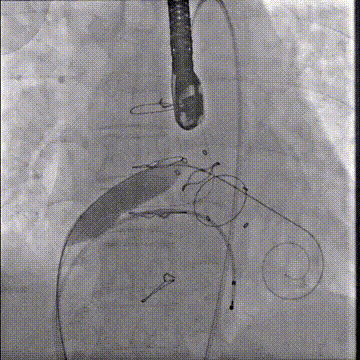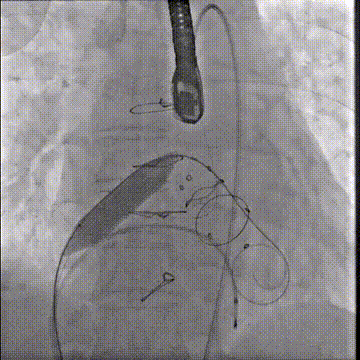
应用14mm球囊充分扩张房间隔
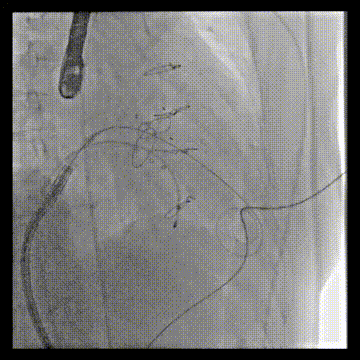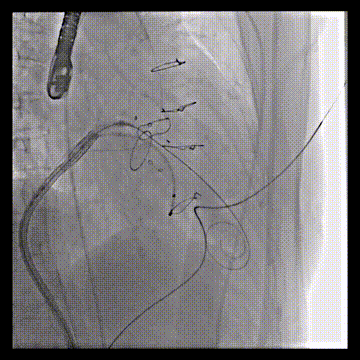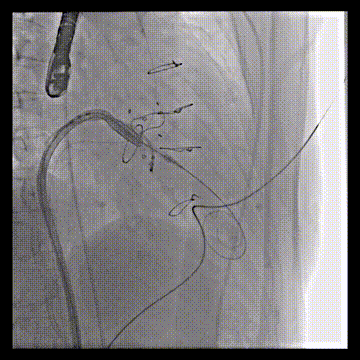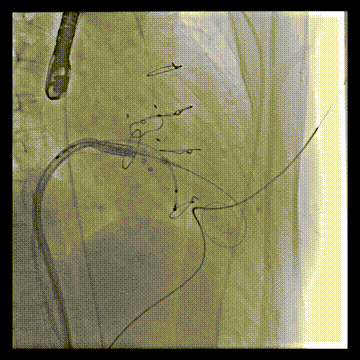
送入23mm SAPIEN 3瓣膜
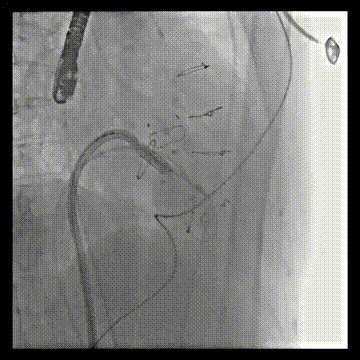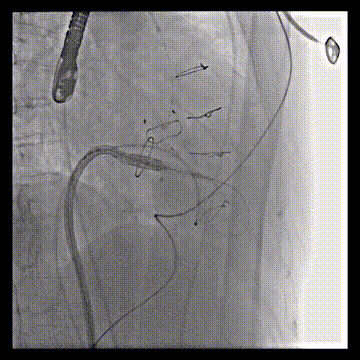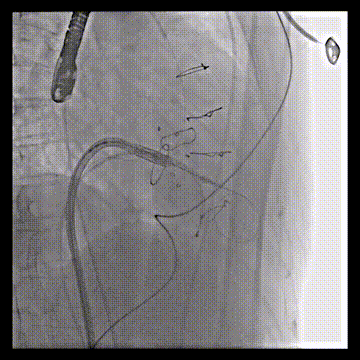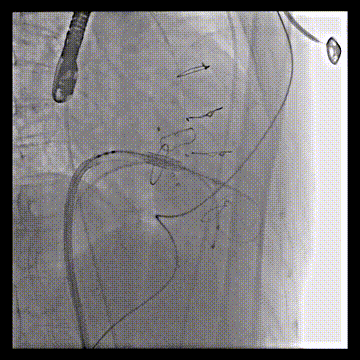
DSA引导下调整瓣膜位置
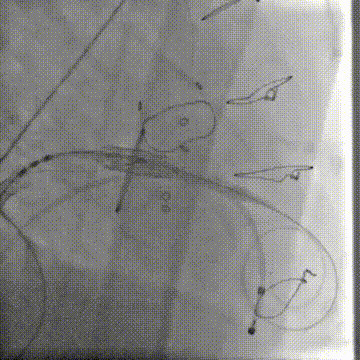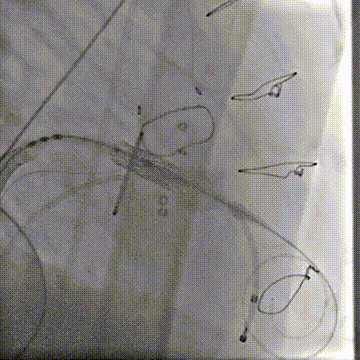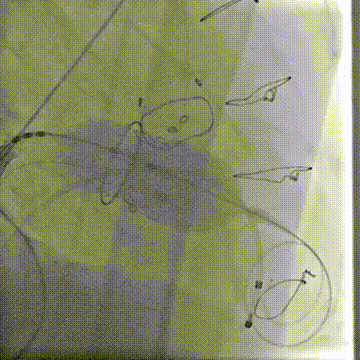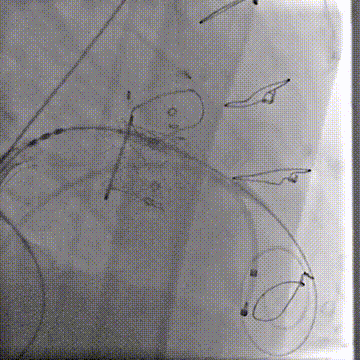
快速起搏180次/分,23mm+2cc球囊膨胀扩张瓣膜
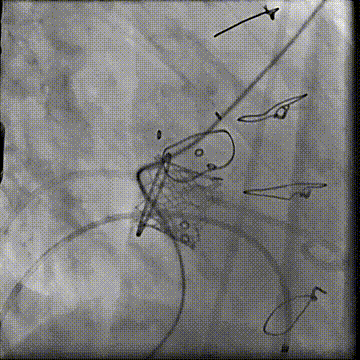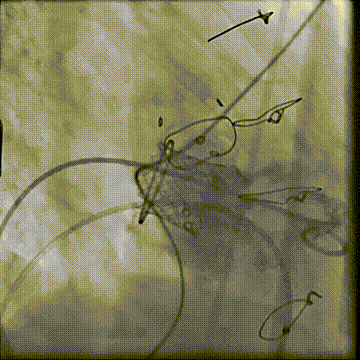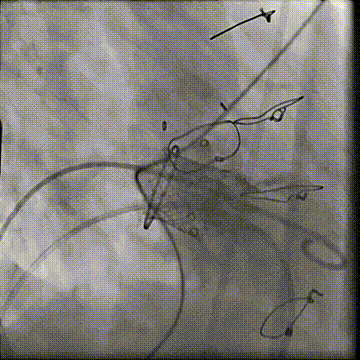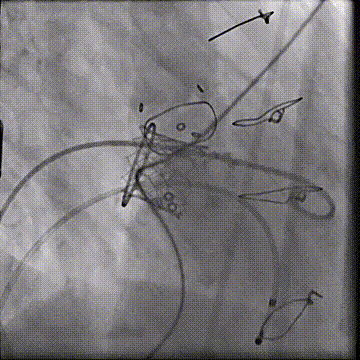
左室造影显示无PVL
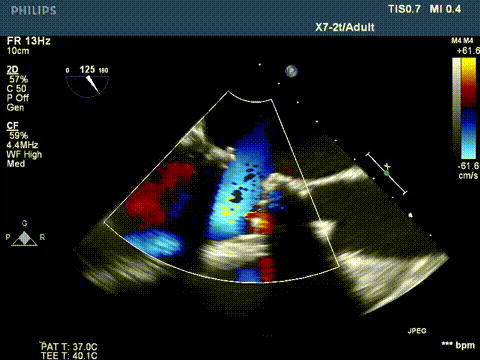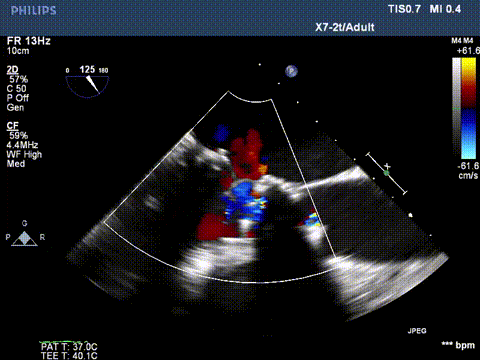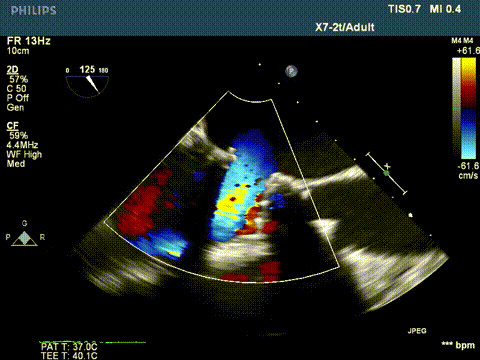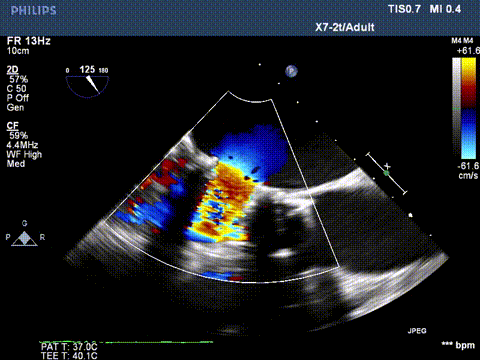

二尖瓣反流消失,跨瓣压差3mmHg;左室流出道血流速度正常
术后3D数字模型
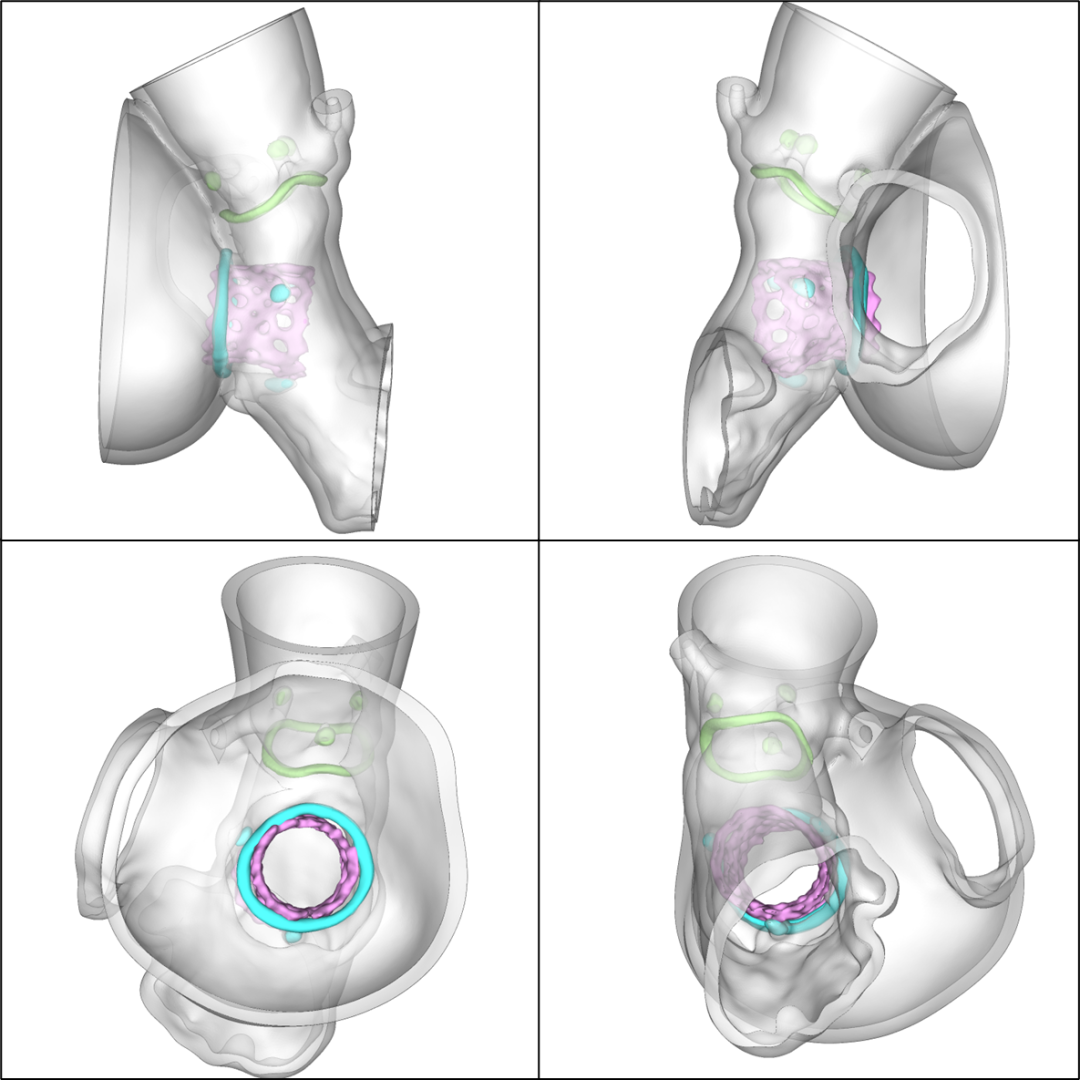
小结
1.术前患者CTA影像对解剖结构的测量、3D数字模型观察以及3D打印体外模拟多模态评估技术,有助于TMVinV手术策略制定,降低手术风险;
