
无导线起搏器正逐渐成为传统经静脉起搏器的替代方案,这主要归因于其能够减少特定并发症。与经静脉起搏器需要通过皮下囊袋将电极送至锁骨下静脉不同,无导线起搏器无需囊袋和电极导线,从而避免了囊袋相关问题(如血肿、感染、破溃、气胸、血胸和电极移位)的风险。此外,经静脉起搏器通常需排除患有永存左上腔静脉、锁骨下静脉或上腔静脉血栓形成或闭塞、严重三尖瓣反流、三尖瓣置换术后、老年患者以及出血或感染高风险人群。尽管无导线起搏器植入避免了这些与囊袋和电极相关的并发症,但使用更粗更硬的输送系统也带来了穿刺部位并发症和心脏穿孔等其他风险。近期,唐都医院团队在《Rev Cardiovasc Med》发表了题为“Comparison of Postoperative Outcomes between Leadless and Conventional Transvenous Pacemakers Implantation: An Up-to-Date Meta-analysis”的最新荟萃分析(PROSPERO注册编码CRD42023453145),基于现有已发表的研究,系统比较了无导线起搏器与经静脉起搏器的术后效果。

本荟萃分析旨在全面比较心动过缓患者中无导线起搏器与传统起搏器相关的并发症情况,分析其优缺点。这些结论对于患者和医疗人员就起搏器选择做出决策至关重要。本研究不仅评估了标准结局,还探索了其他终点事件,包括三尖瓣反流或瓣膜功能障碍、囊袋相关并发症和感染率。
方 法
文献检索
通过PubMed、Ovid Medline、Web of Science、Embase、Cochrane、中国知网、万方和维普等数据库,从建库至2023年8月3日进行了系统文献检索。检索使用的关键词包括:“‘无导线起搏器’或‘无导线起搏’或‘Micra’或‘Nanostim’和‘经静脉起搏器’或‘传统起搏器’”。此外,还评估了相关参考文献。
纳入与排除标准
纳入标准包括:
(1)比较两种起搏器类型术后结局的研究;
(2)考虑纳入随机对照试验和观察性研究。
排除标准包括:
(1)缺乏指定观察终点的研究;
(2)无法获取全文的研究;
(3)多次报告同一人群的研究;
(4)数据不完整或模糊的研究;
(5)两名独立审稿人认为质量较低的研究。
数据提取
提取的数据包括:
(1)纳入研究的基本信息,如研究时期和研究类型;
(2)受试者的一般特征,包括样本量、平均年龄、性别分布和随访期;
(3)关注的特定结局。
终点事件与定义
终点事件包括:并发症发生率,如心包积液或穿孔、穿刺部位事件(血肿、动静脉瘘、假性动脉瘤)、感染性心内膜炎、电极/起搏器移位、囊袋相关并发症(血肿、感染、破溃)、三尖瓣反流或瓣膜功能障碍、任何部位感染、右心室起搏阈值增高、栓塞和深静脉血栓形成、心脏起搏器相关肺栓塞或血栓形成。
三尖瓣反流或功能障碍的定义为:与植入时相比,随访期间新出现的三尖瓣反流或反流程度加重。感染是指为全身性或起搏器相关性感染。右心室起搏阈值增高的定义为:与起搏器植入时的阈值相比,升高超过2倍。栓塞和血栓形成指的是深静脉血栓形成、心脏起搏器相关肺栓塞或血栓形成。
结 果
文献搜索结果与基线信息
最初从八个数据库中共检索出4414篇研究。其中,353篇因重复被排除,3820篇因相关性不足被排除,219篇符合排除标准而被排除,1篇因不符合纳入标准而被排除。另有1篇研究因其全文无法获取且其设计(非大样本队列研究)限制了其对我们研究问题的普遍适用性而被排除。
在审阅相关参考文献后,增加了四篇研究。因此,最终有24篇研究被纳入分析。这些研究中,19篇为英文发表,4篇为中文发表。研究选择的过程详见图1。这些研究参与者的集体基线信息如表1所示。所有纳入的研究均为观察性研究,发表于2016年至2023年间。
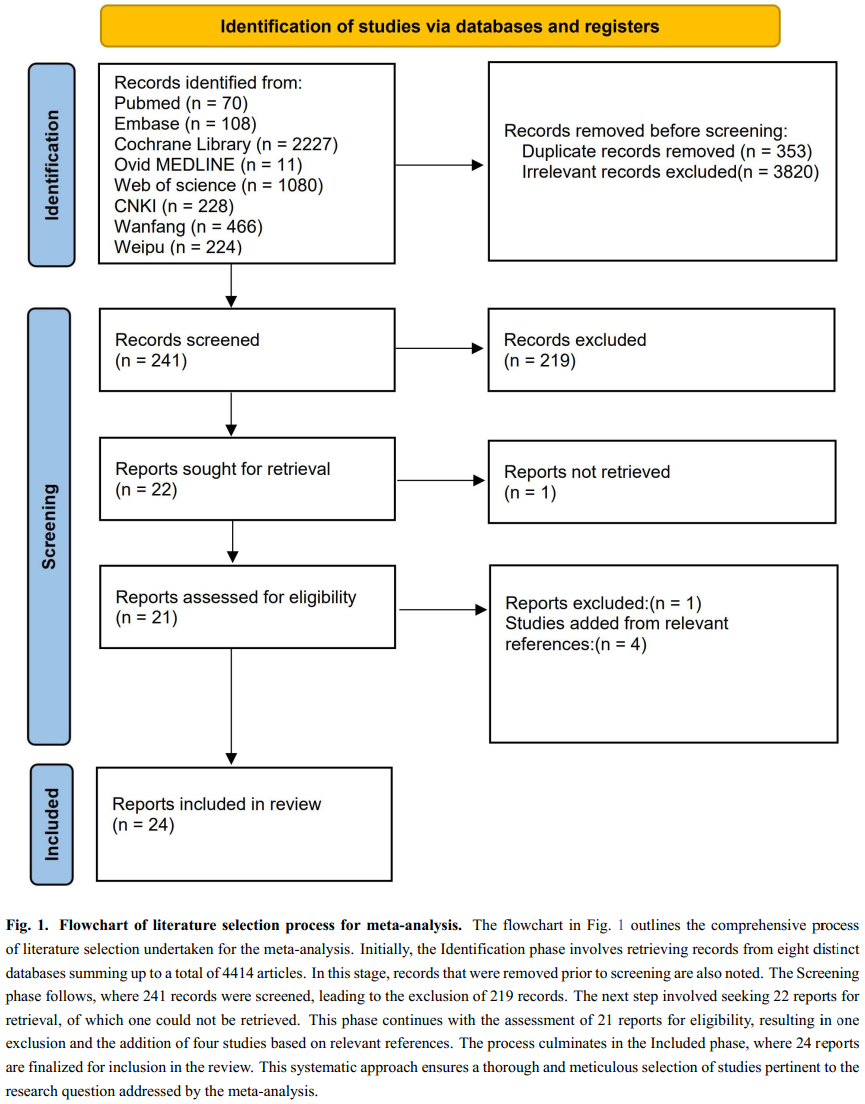
图1.荟萃分析的文献选择流程图。
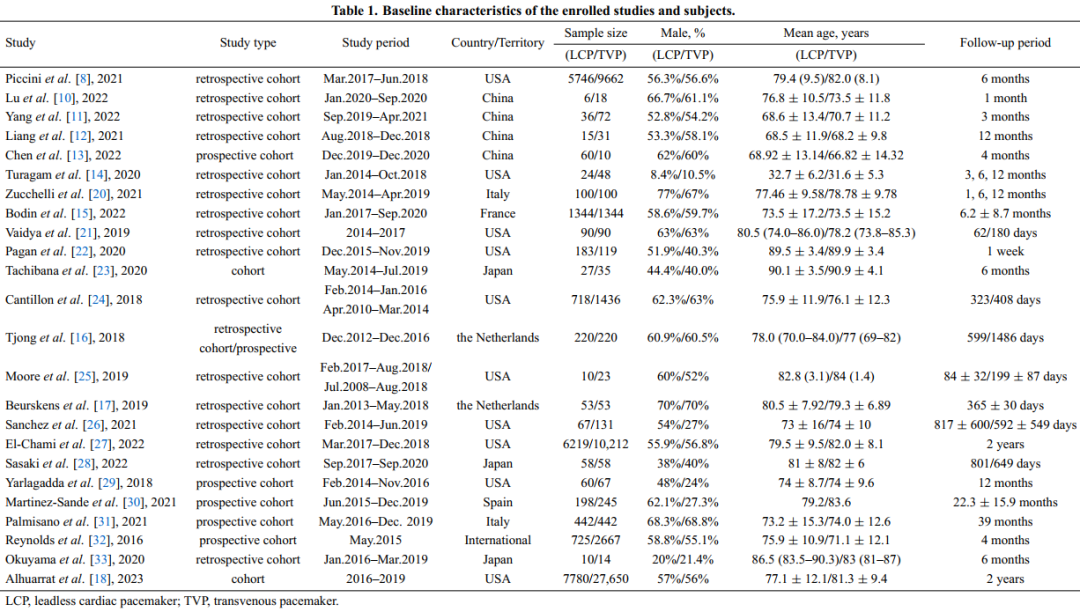
表1.纳入研究和受试者的基线特征。
质量评估
使用Newcastle-Ottawa质量评估量表对观察性研究的质量进行了评估,如表2所示。分数越高表示研究质量越高。质量评分分为以下几类:0-3分表示低质量,4-6分表示中等质量,7-9分表示高质量。本分析纳入的研究均显示出较低的偏倚风险。

表2.使用Newcastle-Ottawa质量评估量表对队列研究进行质量评估。
主要终点
1.穿刺部位事件
共有17项研究纳入了78,938例患者,对穿刺部位事件进行了分析。提示异质性的I²值为0.00%(p=0.74),表明各研究之间的差异可以忽略不计。漏斗图分析和基于回归的Egger检验均未发现显著的发表偏倚证据(p=0.699)(图2A)。采用固定效应模型的荟萃分析显示,与无导线起搏器组相比,经静脉起搏器组的穿刺部位事件发生率显著降低(OR=0.24,95% CI:0.19-0.32,p<0.01)(图3)。

图2.不同并发症的发表偏倚漏斗图。(A)穿刺部位事件。(B)电极/起搏器移位。(C)囊袋相关并发症。(D)心包积液/穿孔。
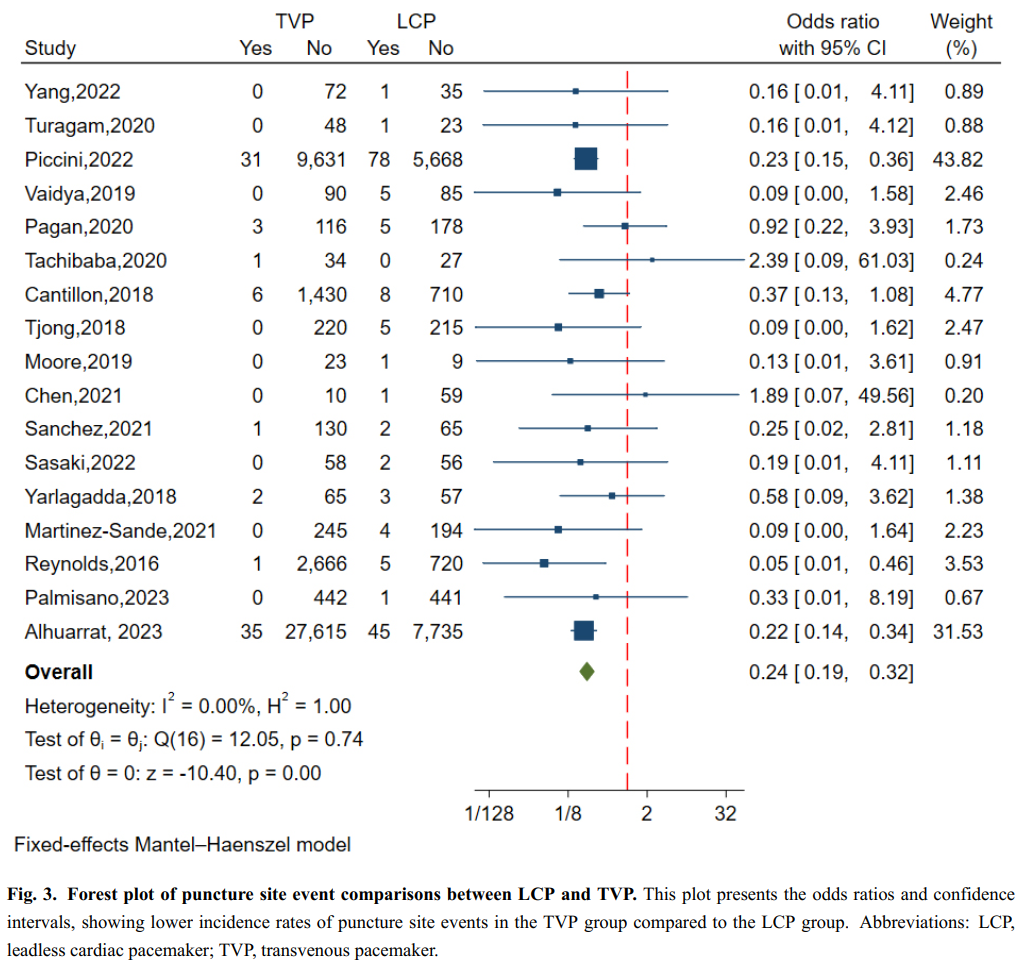
图3.无导线起搏器与经静脉起搏器穿刺部位事件比较的森林图。
2.电极/起搏器移位
共有10项研究纳入了6271例患者,对电极或起搏器移位的发生率进行了分析。这些研究显示出极小的异质性(I²=0.00%,p=0.54),支持使用固定效应模型。漏斗图分析和基于回归的Egger检验均未发现发表偏倚(p=0.162)(图2B)。结果表明,与经静脉起搏器组相比,无导线起搏器组的电极或起搏器移位发生率显著降低(OR=3.32,95% CI:1.91-5.77,p<0.01)(图4)。

图4. 无导线起搏器与经静脉起搏器电极/起搏器移位比较的森林图。
3. 感染性心内膜炎
共有8项研究纳入了8404例患者,对感染性心内膜炎的发生率进行了分析,结果显示异质性极小(I²=0.00%,p=0.91)。漏斗图分析和基于回归的Egger检验均未发现发表偏倚(p=0.984)。分析显示,与经静脉起搏器组相比,无导线起搏器组的感染性心内膜炎发生率显著降低(OR=3.62,95% CI:3.10-4.24,p<0.01)(图5)。
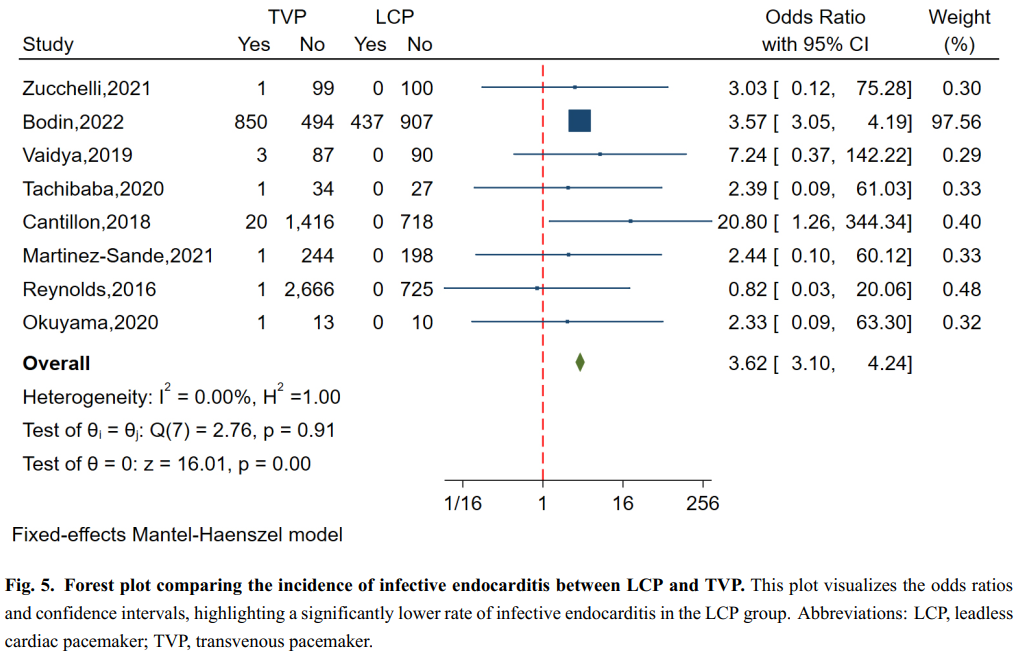
图5.无导线起搏器与经静脉起搏器感染性心内膜炎发生率的比较森林图。
4.三尖瓣反流或瓣膜功能障碍
共有4项研究纳入了816例患者,对三尖瓣反流或瓣膜功能障碍的发生率进行了分析,结果显示异质性极小(I²=0.00%,p=0.470)。漏斗图分析和基于回归的Egger检验均未发现发表偏倚(p=0.481)。结果表明,虽然无导线起搏器组的三尖瓣反流或瓣膜功能障碍发生率略低于经静脉起搏器组,但这一差异并不具有统计学显著性(OR=1.26,95% CI:0.80-2.00,p=0.32)(图6)。

图6.无导线起搏器与经静脉起搏器三尖瓣反流或功能障碍发生率比较的森林图。
5. 感染
共有5项研究纳入了3082例患者,对感染的发生率进行了分析,结果显示异质性相对较小(I²=19.21%,p=0.290)。漏斗图分析和基于回归的Egger检验均未发现发表偏倚(p=0.249)。分析显示,与经静脉起搏器组相比,无导线起搏器组的感染发生率显著降低(OR=3.93,95% CI:1.67-9.24,p<0.01)(图7)。
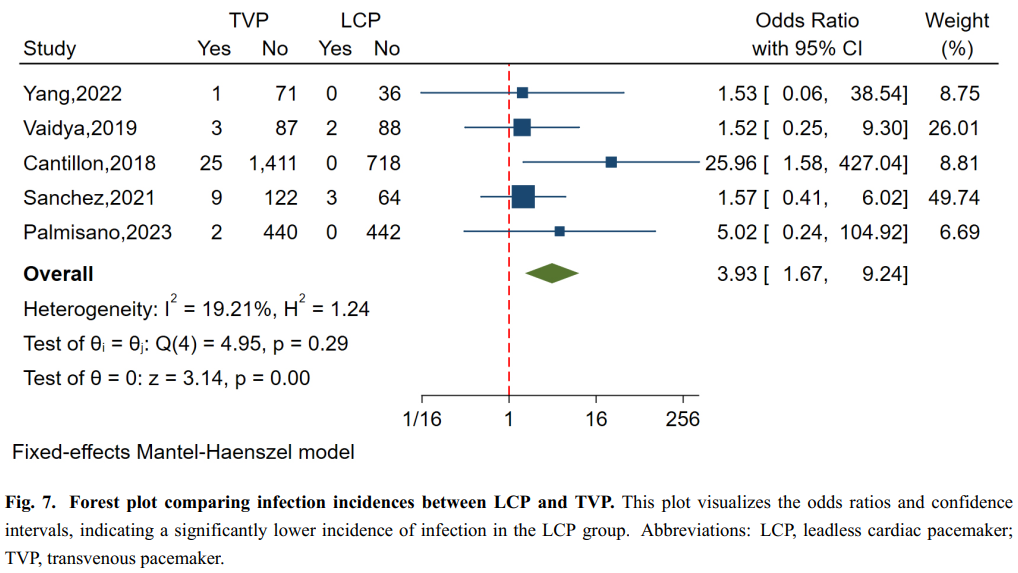
图7. 无导线起搏器与经静脉起搏器感染发生率比较的森林图。
6.右心室起搏阈值增高
共有5项研究纳入了4518例患者,对右心室起搏阈值增高的发生率进行了分析,结果显示异质性相对较小(I²=17.03%,p=0.310)。漏斗图分析和基于回归的Egger检验均未发现发表偏倚(p=0.896)。总体而言,研究发现无导线起搏器患者的右心室起搏阈值增高率略高于经静脉起搏器患者,但这一差异不具有统计学显著性(OR=0.37,95% CI:0.12-1.09,p=0.07)(图8)。

图8.无导线起搏器与经静脉起搏器右心室起搏阈值增高率的比较森林图。
7.心包积液或心脏穿孔
共有12项研究纳入了53243例患者,对心包积液或心脏穿孔的发生率进行了评估,结果显示异质性相对较小(I²=17.82%)。漏斗图分析和基于回归的Egger检验均未发现发表偏倚(p=0.701)(图2D)。固定效应模型显示,与经静脉起搏器组相比,无导线起搏器组的心包积液/心脏穿孔发生率显著更高(OR=0.33,95% CI:0.28-0.39,p<0.01)(图9)。

图9.无导线起搏器与经静脉起搏器心包积液或穿孔发生率的比较森林图。
8.血栓形成和栓塞
共有5项研究纳入了61184例患者,对血栓形成和栓塞的发生率进行了评估,结果显示异质性相对较大(I²=93.25%,p<0.01)。漏斗图分析和基于回归的Egger检验均未发现发表偏倚(p=0.136)。随机效应模型显示,无导线起搏器组的血栓形成和栓塞发生率低于经静脉起搏器组,但这一差异不具有统计学显著性(OR=0.76,95% CI:0.30-1.92,p=0.57)(图10)。
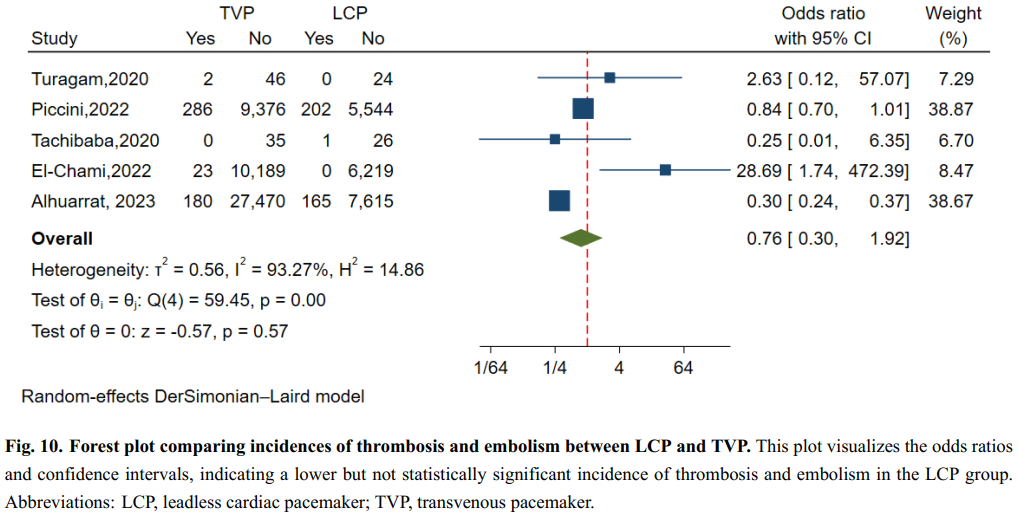
图10.无导线起搏器与经静脉起搏器血栓形成和栓塞发生率的比较森林图。
9.囊袋相关并发症
共有14项研究纳入了2926例患者,通过荟萃分析评估了囊袋相关并发症的发生率。漏斗图分析和基于回归的Egger检验均未发现显著的发表偏倚(p=0.144)(图2C)。这些研究的I²值为55.54%,表明异质性相对较大,因此采用了随机效应模型。森林图显示,经静脉起搏器后囊袋相关并发症的发生率为1%(OR=0.01,95% CI:1%-2%,p<0.01)(图11)。

图11.森林图显示了经静脉起搏器组中囊袋相关并发症的发生率。此图可视化了囊袋相关并发症的发生率,突出了经静脉起搏器组中该并发症的持续发生情况
讨 论
本荟萃分析扩展了关于无导线起搏器与经静脉起搏器在各种临床终点上的安全性比较的证据。研究结果证实了起搏器选择策略的复杂性,突出了不同设备类型相关的风险模式。强调了在选择最合适的起搏器技术时需考虑患者个体状况和临床情况。
本综述共纳入了24项观察性研究,显示在所有终点上均无发表偏倚。对于心包积液或心脏穿孔、穿刺部位事件、感染性心内膜炎、电极或起搏器移位、三尖瓣反流或瓣膜功能障碍、任何部位感染以及右心室起搏阈值增高,不同研究间的异质性相对较低。然而,对于血栓形成和栓塞以及囊袋相关并发症,异质性相对较高。值得注意的是,无导线起搏器组的感染性心内膜炎、电极或起搏器移位、任何部位感染以及囊袋相关并发症的发生率低于经静脉起搏器组,而经静脉起搏器组的穿刺部位事件和心包积液或心脏穿孔的发生率低于无导线起搏器组。
无导线起搏器没有电极和锁骨下区域的囊袋,因此避免了与之相关的并发症。既往研究表明,与经静脉起搏器相关的囊袋并发症发生率在2.90%至4.50%之间。本荟萃分析显示了较低的发生率,为1%(95% CI:1%-2%),这可能是由于纳入的研究数量有限所致。此外,无导线起搏器的手术过程更简单,步骤更少,创伤更小,是其安全性的原因。
尽管无导线起搏器减少了电极和囊袋并发症,但它们增加了心包积液/心脏穿孔等心脏损伤的风险,既往研究报告的发生率在0.9%至1.6%之间。此外,心脏损伤可能导致严重后果。例如,在563例接受植入术并出现心脏损伤的患者中,150例患者死亡(27%),499例患者发生心脏压塞(89%),64例患者出现心包积液(11%),146例患者(26%)在30天内需要紧急手术。此外,一半的穿孔与操作失误有关。
无导线起搏器定位是影响心包积液/心脏穿孔发生率的关键因素,常被认为是第二常见的设备相关问题。在上市后注册研究中,与室间隔位置相比,心尖部位的并发症发生率更高(52% vs 33%)。标准定位方法是在右前斜位(RAO)下将无导线起搏器植入心脏轮廓的中心,并在左前斜位(LAO)时向左植入。然而,挑战依然存在;例如,在左侧位视图中指向游离壁时,有17.6%没有遵循最佳放置策略。Hai J等尝试通过在左侧位时将起搏器指向远离胸骨的方向来改进这一点。然而,植入部位未通过CT或超声心动图确认,导致1例报告穿孔(2%)。因此,Li等建议应常规进行右室造影,以提高无导线起搏器在右室室间隔中部植入的准确性。尽管采取了这些措施,但在通过右室造影引导后,仍有约6.2%的无导线起搏器未正确定位在室间隔中部。室间隔中部定位的难度可能归因于心脏转位。这强调了提高植入技能从而降低心脏穿孔和心脏积液风险的必要性。
传统起搏器电极和右心室起搏均被认为是导致瓣膜功能障碍以及整体心脏功能减低的潜在因素。既往研究表明,经静脉起搏器植入可能导致或加重约10%至45%病例的三尖瓣反流,可能是由于电极植入过程中对三尖瓣瓣叶或瓣下结构的损伤以及跨瓣电极的长期机械应力所致。虽然无导线起搏器避免了传统起搏器电极对三尖瓣机械功能的影响,但它并未完全消除三尖瓣功能障碍的风险,这是一个可能受不同随访时间影响的慢性过程。
随着Micra AV和心房无导线起搏器等技术的进步,无导线起搏器的植入范围已得到扩展。作为一项相对较新的技术,无导线起搏器植入存在一定的学习曲线。操作者的熟练程度在术后并发症(如心包积液或心脏穿孔)的发生率中起着至关重要的作用。随着经验的积累,植入技能的提高,手术相关并发症将会减少。
结 论
与经静脉起搏器相比,无导线起搏器植入可降低感染性心内膜炎、电极或起搏器移位、感染以及囊袋相关并发症的风险,但穿刺部位并发症以及心包积液或心脏穿孔的风险较高。因此,本研究有助于制定针对不同患者的个性化治疗方案。当然,为了获得更为明确的结论,需要进一步多中心、大规模、长期随访的随机对照试验研究。
· END ·
