
冠状动脉瘤(Coronary Artery Aneurysm, CAA)和冠状动脉扩张(Coronary Artery Ectasia, CAE)统称为冠状动脉瘤或扩张(Coronary Artery Aneurysm or Ectasia, CAAE),是一类以冠状动脉异常扩张为特征的血管病变。冠状动脉造影检出率约为0.15%-5.3%,男性占比显著高于女性(83% vs. 60%)。随着多层CT和MRI等影像学技术的普及,无症状或偶然发现的病例逐渐增多,部分患者可出现不稳定心绞痛、急性心肌梗死(MI)、心律失常甚至心源性猝死等并发症,年主要不良心血管事件(MACE)发生率高达10%。其病因、发病机制及治疗策略仍存在诸多争议。本文结合《Biomedicines》“Coronary Artery Aneurysm or Ectasia as a Form of Coronary Artery Remodeling: Etiology, Pathogenesis, Diagnostics, Complications, and Treatment”及最新研究进展,系统解析CAAE的病因、发病机制、诊治要点及治疗方案的优劣。

一、核心定义与分型
定义
冠状动脉扩张(CAE):指冠状动脉节段性或弥漫性扩张,直径超过正常节段1.5倍,长度>20mm或超过血管长度的1/3,可分为弥漫型(多支或单支广泛扩张)和局限型(节段性扩张)。
冠状动脉瘤(CAA):表现为局限性扩张,分为囊状(横径>纵径)和梭状(纵径>横径),直径超过正常4倍者称为巨大动脉瘤(仅占0.02%)。

图1、冠状动脉瘤样扩张的可能形态和临床表现。白色箭头表示血液流动方向
解剖分布
右冠状动脉近中段:40%-73%
左前降支近段:10%-51%
左回旋支:4%-43%
左主干:2%-9%
病理特征
冠状动脉扩张(CAE):表现为血管壁弹力纤维和胶原降解、弹力层破坏;
冠状动脉瘤(CAA):则因局部扩张导致血流动力学改变,易继发血栓形成和斑块破裂。
Markis分型
根据受累范围,CAE分为四型:
Ⅰ型:2-3支血管弥漫性扩张
Ⅱ型:1支血管弥漫性扩张+另1支局限性扩张
Ⅲ型:单支血管弥漫性扩张
Ⅳ型:局限性或节段性扩张

表1、CAAE患者血管壁结构的IVUS分型
二、病因与发病机制
病因分类
动脉粥样硬化:最常见病因,约50%的CAE/CAA与之相关,斑块负荷导致血管代偿性扩张(正向重塑),高血压、吸烟、高同型半胱氨酸血症为重要危险因素。
先天性与遗传性因素:20%-30%为先天性,遗传因素包括HLA-DR B1813、DR16、DQ2和DQ5等位基因,MMP-3基因的5A等位基因的发生以及ACE基因的缺失-插入多态性(ACE DD 基因型)。
其他病因:川崎病(儿童CAAE的主要病因)、感染(如EB病毒)、血管炎(如IgG4相关疾病)、医源性损伤等。
病理机制
炎症级联反应:C反应蛋白(CRP)、白细胞介素-6(IL-6)升高,黏附分子(VCAM-1、ICAM-1)水平升高,促进血管壁炎症。
基质代谢失衡:基质金属蛋白酶(MMPs)活性增强,导致血管壁基质降解。MMP-2、MMP-9过度表达,抑制金属蛋白酶组织抑制剂(TIMP),血管弹力层破坏引发血管薄弱和扩张。
遗传与分子靶点:单核苷酸变异(SNVs)参与血管重塑,ADAMTS13、GALC、ITPKB、NPC1和PERM1。其中,ADAMTS13、ITPKB和PERM1存在错义突变,而GALC和NPC1存在剪接位点突变。。
血流动力学与内皮功能障碍:湍流和剪切应力异常导致内皮损伤,促凝状态形成,加速血栓和动脉瘤进展。
三、诊断要点
冠状动脉造影(CAG)
优势:显示病变部位、形态(囊状/梭状)及狭窄程度,是诊断金标准。
局限:血栓存在时可能低估动脉瘤实际大小,扩张冠状动脉段的湍流可能影响成像质量。

图2、冠状动脉造影
(A)右冠状动脉的囊状动脉瘤(箭头),(B)左前降支中段囊状动脉瘤(箭头),(C)左前降支梭形动脉瘤(箭头),(D)左主干的囊状动脉瘤(箭头),(E)右冠状动脉的冠状动脉扩张,(F)左回旋支冠状动脉扩张
血管内超声(IVUS)
核心价值:精确测量血管直径,鉴别真性动脉瘤(三层结构完整)与假性动脉瘤(外膜破坏),指导支架尺寸选择(尤其复杂病变)。
适用场景:CAG显示不清、怀疑血栓或夹层、拟行PCI的病变评估。

图3、左前降支中段囊状动脉瘤的冠状动脉造影(箭头)及相应IVUS图像
IVUS显示近端和远端参考血管和动脉瘤与参考直径的比率,以显示病变大小。
图例:A-动脉瘤;p-近端;d-远端;箭头-动脉瘤的最大血管直径。
光学相干断层扫描(OCT)
优势:超高分辨率,清晰显示斑块成分(脂质、钙化)、血栓及内膜撕裂。
局限:穿透深度浅,对于较大的动脉瘤,无法评估整个血管横截面。

图4、左前降支梭形动脉瘤(箭头)的冠状动脉造影(箭头)及相应OCT图像
OCT显示近端和远端参考血管和动脉瘤与参考直径的比率,以显示病变大小。
图例:A-动脉瘤;p-近端;d-远端;箭头-动脉瘤的最大血管直径;星号-侧支。
冠状动脉CT血管成像(CCTA)
核心优势:准确评估动脉瘤大小、位置、钙化及血栓负荷,可三维重建血管解剖,指导外科手术规划(如左主干动脉瘤与周围结构关系)。
推荐场景:无症状人群筛查、已知CAAE患者的长期随访。
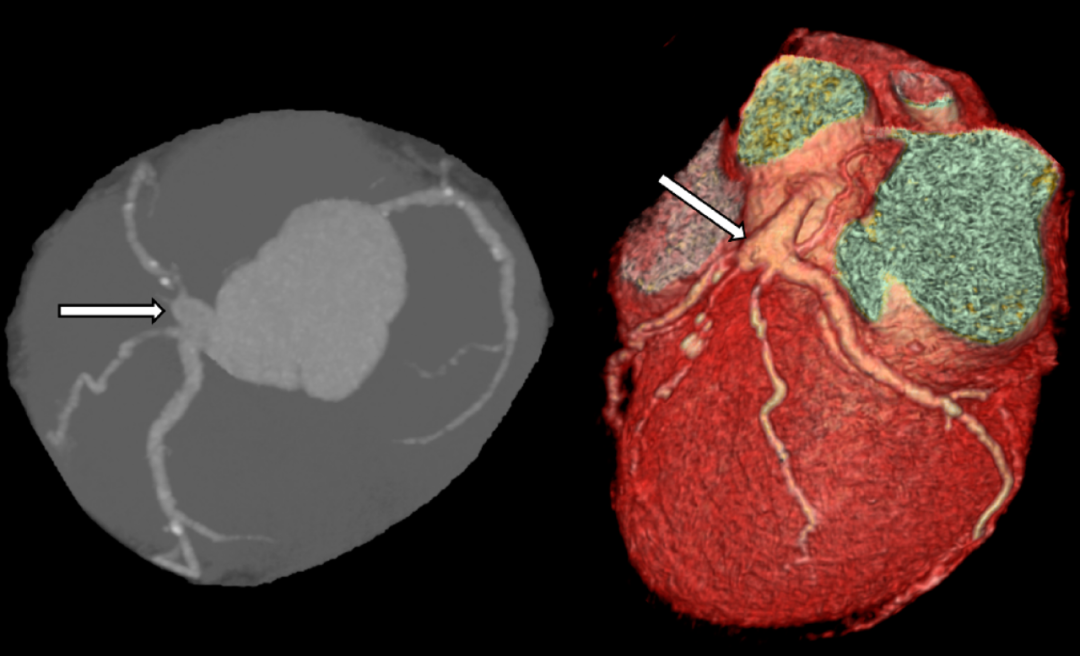
图5、CT中左冠状动脉主干的动脉瘤样病变(箭头)
四、临床意义与并发症
心肌缺血的多重机制
微栓塞与血流障碍:动脉瘤内血栓脱落导致远端血管栓塞,TIMI帧计数升高提示冠状动脉血流缓慢,心肌灌注分级(MBG)下降。
冠状动脉微血管功能障碍(CMD):包括功能性(收缩和舒张)和结构性(血管重塑)功能障碍。冠状动脉微循环阻力(由IMR值表示)在CAAE组中显著高于无阻塞性冠状动脉的缺血性患者(INOCA),提示微血管重塑异常,即使无显著狭窄也可导致心肌灌注不良。
血管痉挛与斑块破裂:炎症激活交感神经,诱发冠状动脉痉挛;CAAE和冠状动脉显著狭窄的共存非常常见(>50%),不稳定斑块破裂引发急性冠脉综合征(ACS)。
性别差异与预后影响
CAAR注册研究:女性患者年龄更大,高血压患病率更高,吸烟及严重狭窄比例更低,接受抗血小板治疗较少(DAPT中位时长3个月 vs. 男性9个月),但长期MACE无显著差异,男性ACS发生率更高(15% vs. 10%)。
临床启示:需关注女性患者的潜在炎症状态和抗栓不足问题,避免因“低风险”误判导致治疗不足。
并发症
血栓栓塞:瘤内血流淤滞导致远端栓塞,引发心肌梗死。
动脉瘤破裂:罕见但致命,可致心脏压塞或心脏腔室、主动脉或肺动脉的瘘管形成。
机械性压迫:巨大动脉瘤(>20mm)压迫食管致吞咽困难,压迫右心房引发右心衰竭。

图6、CAAE临床表现图解
五、治疗策略
保守治疗
保守治疗取决于CAA的病因。如果病因是动脉粥样硬化,应优化动脉粥样硬化治疗方案,控制心血管危险因素。
(1)抗栓治疗
抗血小板药物:对于偶然发现的CAAE患者,双联抗血小板治疗(DAPT)或治疗性抗凝的作用尚不明确。合并CAD的患者根据指南进行治疗。
抗凝治疗:华法林或新型口服抗凝药(NOAC)可能减少血栓事件,但需权衡出血风险。
(2)病因治疗
川崎病:仅在有大或快速进展的CAA时推荐抗凝治疗。川崎病发病后十天内静脉注射免疫球蛋白(IVIG)可降低CAA发生率(从23%降至5%),将巨大动脉瘤的发病率从5%降低到1%,改善CAA退行性变,减少MACE的发生。
IgG4相关疾病:糖皮质激素(首选),复发者用利妥昔单抗,需警惕激素加速动脉瘤变性和增加破裂风险。
(3)药物干预
他汀类药物:可能有助于抑制MMPs,其对MMPs活性的影响因他汀类药物的亲脂性而异。更亲脂性的他汀类药物(辛伐他汀和阿托伐他汀)可降低MMP-9活性(但亲水性他汀类药物普伐他汀则不然)。然而,阿托伐他汀和普伐他汀可以降低MMP-2的活性。
ACEI/ARB:血管紧张素转换酶抑制剂(ACEIs)在预防或延缓冠状动脉瘤进展中的作用尚无定论。由于ACE基因多态性与CAE之间的关系,给予ACEIs似乎也是合理的。然而,这仍需进一步研究。
(4)禁忌药物
硝酸酯类:可能加重冠状动脉窃血并加剧心肌缺血,应避免使用。
有创治疗
对于无ACS的CAAE患者,目前尚缺乏明确的介入治疗建议。
尽管文献中报道了一些成功使用支架治疗CAE的案例,但我们应知晓可能的后果,特别是支架内再狭窄(ISR)和血栓形成的风险(支架内皮化时间延长)
对于伴有高风险临床或解剖特征的患者,应根据动脉瘤的形状和大小调整治疗方案。例如,囊状动脉瘤和小假性动脉瘤可采用覆膜支架植入术(除非涉及主要分支血管),而涉及主要分支血管的囊状或梭形动脉瘤可采用球囊或支架辅助的线圈栓塞或手术切除。
对于有症状且CAA快速扩大或大CAA引起外部压迫的患者,经皮封堵术(使用Amplatzer封堵器)或线圈栓塞(有或无自身血管PCI)可以作为手术治疗的替代方案。
对于累及左主冠状动脉、多个或巨大(>20mm,或>4倍参考血管直径)CAA患者,以及静脉桥血管动脉瘤患者,手术应作为一线治疗。
对于有多个动脉瘤且伴有冠状动脉显著狭窄的患者,以及巨大左主冠状动脉动脉瘤患者,或因动脉瘤引起压迫症状、瘘管和其他危及生命的并发症的患者,也应考虑手术治疗。
新技术应用与挑战
目前市场上尚无专门用于治疗CAA的支架,但一些支架移植物系统已用于CAA的非指定用途治疗。对于巨大动脉瘤,可考虑使用四氟乙烯涂层的自膨胀支架。在覆膜支架放置过程中,可能因严重扭曲、钙化或分支血管受累风险而变得复杂和具有挑战性,此时可采用支架辅助或球囊辅助的线圈栓塞技术。此外,还有关于使用AngioJet血栓切除术的数据。
总之,冠状动脉瘤或冠状动脉扩张的诊治和治疗较为复杂,涉及多种因素和方法。未来仍需进一步的研究以明确其发病机制、优化治疗方案并改善患者预后。
六、预后
动脉瘤内血栓形成导致动脉闭塞或远端栓塞可能引发心肌梗死。不同研究对CAAE的预后观点不一。CASS研究认为该异常可视为冠状动脉疾病的一种形式,而Baman等研究发现CAAE患者5年生存率仅为71%,建议积极治疗。总体而言,CAAE与心肌梗死及心肌梗死复发风险增加相关。
严道心得:从争议到共识,个体化治疗是关键
CAAE作为冠状动脉重塑的特殊形式,其诊治仍面临诸多挑战:病因复杂(动脉粥样硬化与非粥样硬化因素交织)、治疗证据等级低(多为回顾性研究)、并发症风险多种多样。从争议到共识,个体化治疗仍是管理的关键,需遵循以下原则:
精准诊断:结合CCTA初筛与IVUS/OCT精细评估,明确病变性质(真性/假性动脉瘤、有无血栓/夹层)。
病因导向:区分动脉粥样硬化、先天性、炎症性病因,针对性干预(如川崎病早期IVIG、IgG4病免疫抑制)。
风险分层:依据动脉瘤大小、部位、合并症制定策略,巨大/左主干病变首选外科,轻中度病变强化药物+密切随访。
抗栓谨慎:无ACS者单药抗血小板为主,DAPT和抗凝仅限高血栓风险或术后患者,平衡出血与缺血风险。
多学科协作(心内、心外、影像、风湿免疫)是优化CAAE管理的趋势,随着更多真实世界数据的积累,未来仍需进一步的研究以明确其发病机制、优化治疗方案并改善患者预后。