
本文报道一例89岁男性患者,因起搏器囊袋反复感染合并电极导线断裂深埋于锁骨下深层组织,经多次清创及保守治疗无效后,武汉大学中南医院心血管外科团队采用杂交手术方案,结合外科切开与激光鞘技术,成功拔除严重粘连的断裂电极导线。根据文献统计,起搏器电极导线感染病人如果不进行系统性拔除,一年内死亡率高达32%。该案例为复杂电极导线拔除提供了创新性解决方案,提示激光鞘技术在低牵引力条件下的临床应用价值。
病史与诊疗经过
患者于2013年植入双腔起搏器,2023年3月因囊袋感染行起搏器置换术,术后仍反复感染。2023年8月,因纹带棒状杆菌感染,行局部清创、剪断电极导线并植入无导线起搏器。2023年11月,感染再次复发,来我院行囊袋清除缝合术。今年4月份因感染复发,再次到我院进行检查治疗。影像学检查显示电极导线残端深埋于锁骨下深层组织,且锁骨下静脉及上腔静脉均与导线形成闭塞性粘连(图1)。

图1
挑战与决策
患者既往因电极导线被剪断后回缩至锁骨下深层组织,导致无法从囊袋触及导线残端。因上腔静脉造影提示锁骨下静脉及上腔静脉与导线存在闭塞性粘连,常规下腔圈套器拔除存在血管撕裂或导线断裂风险;而外科开胸需同时处理锁骨下静脉及上腔静脉,操作复杂且手术难度极大(文献未见类似成功报道)。若保守治疗则感染持续进展危及生命。为了解决患者病痛,在武汉大学中南医院心血管病医院刘金平院长的指导下,经心血管外科团队多次讨论,由科室首席专家赵金平主任医师和朱明林副主任医师、陈赵主治医师合作,最终制定杂交手术方案:①外科切开定位深埋电极头端,置入锁紧钢丝加固导线;②应用目前国际上最先进的激光鞘消蚀并分离粘连组织,把电极导线与血管分离。
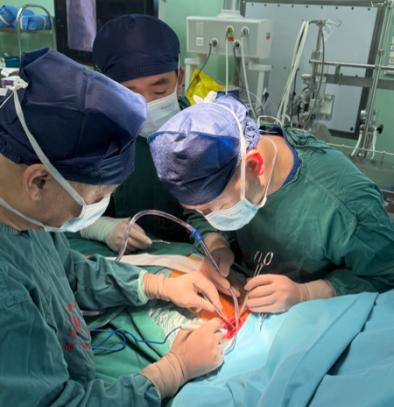
图2
手术过程
1. 外科切开锁定电极残端
于锁骨下深层组织分离出心房及心室电极头端(图3-6),经心房电极置入锁紧钢丝以增强牵引力(图7-10)。因电极结构损坏,心室电极仅能锁定3-4cm,牵引力微弱(图11-14)。
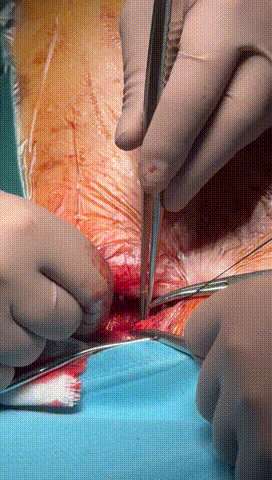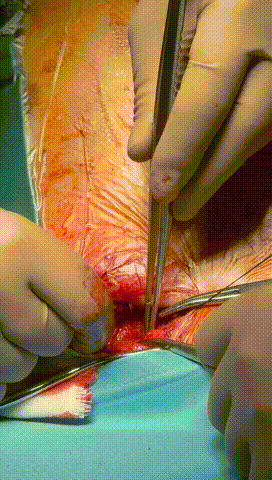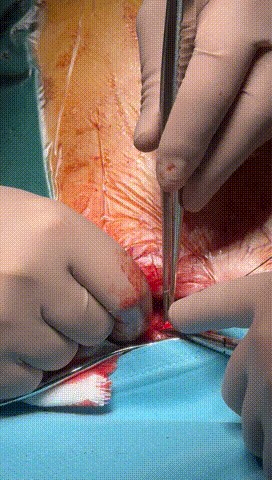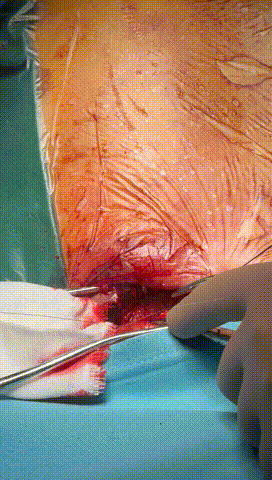
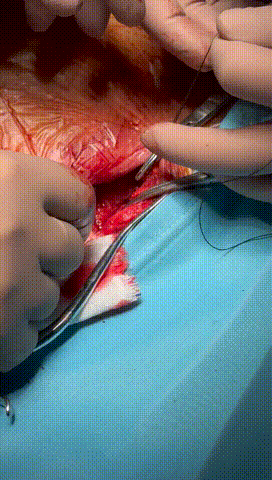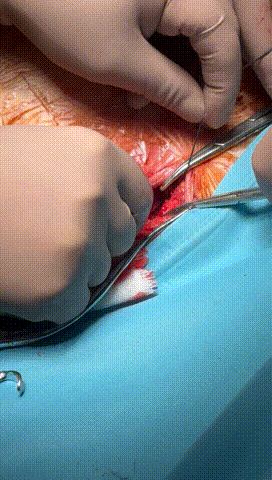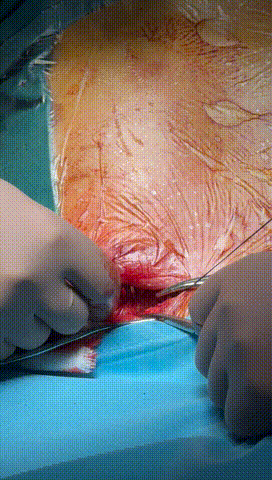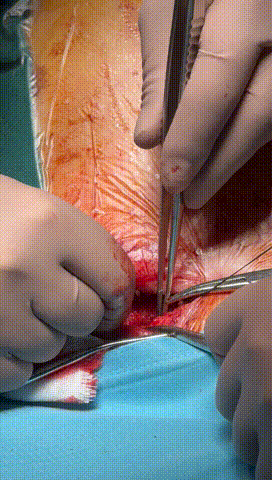
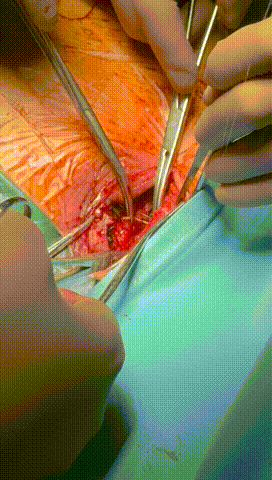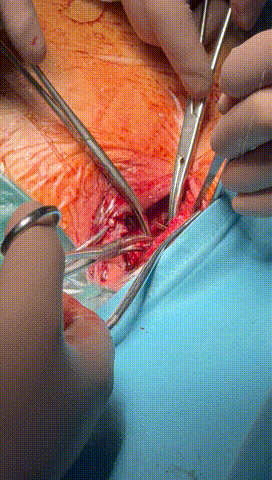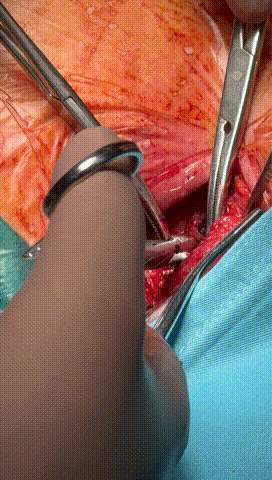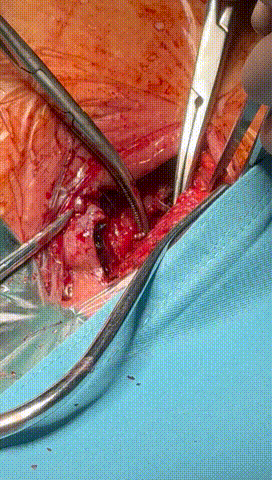
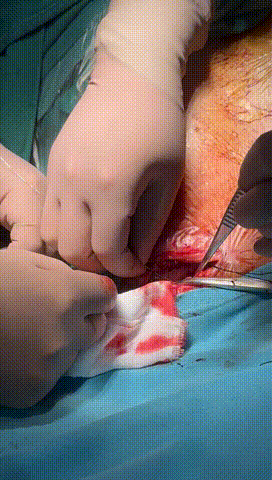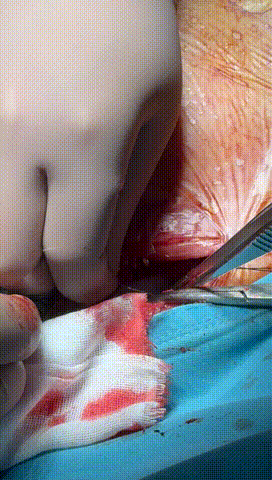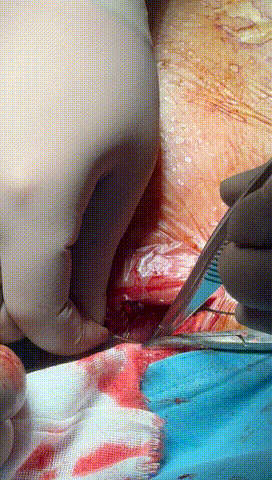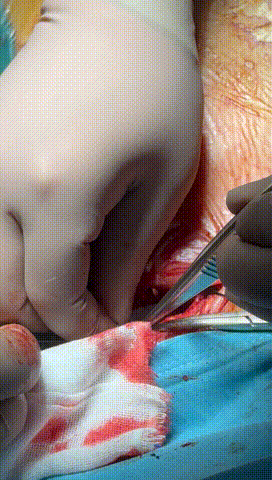
图3-6 经过小心谨慎探索,分离出心室及心房电极头端,并用钢丝清理电极内部


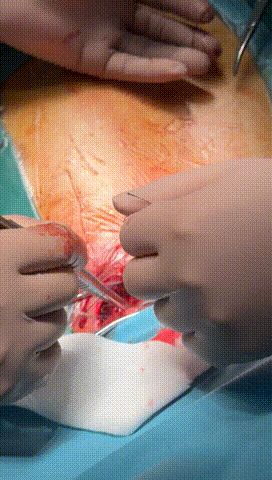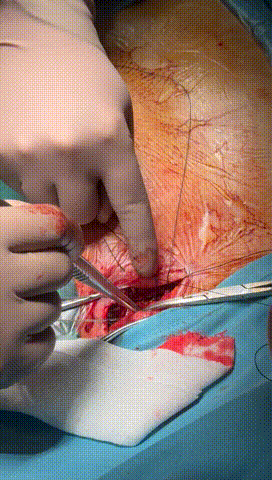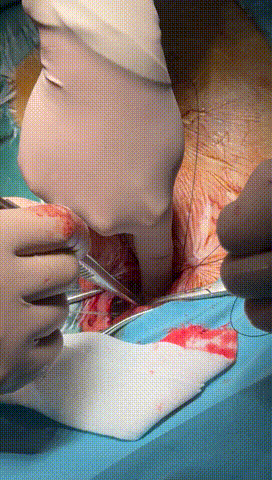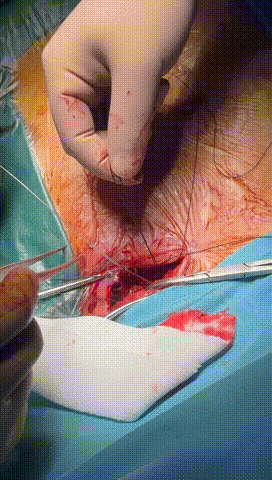
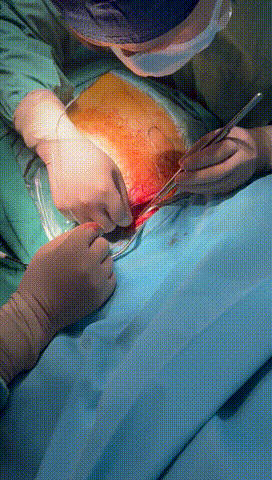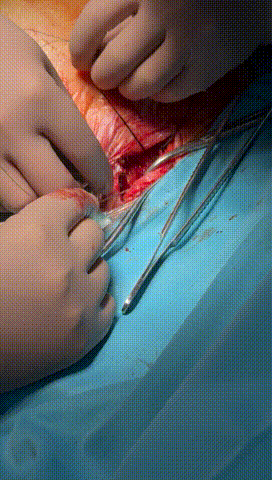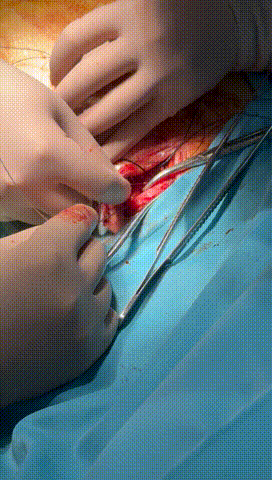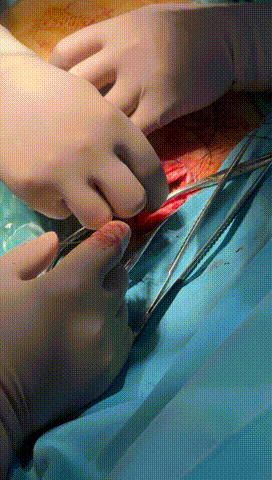
图7-10 锁紧钢丝顺利进入心房电极锁紧,并用缝线绑紧电极导线与绝缘层



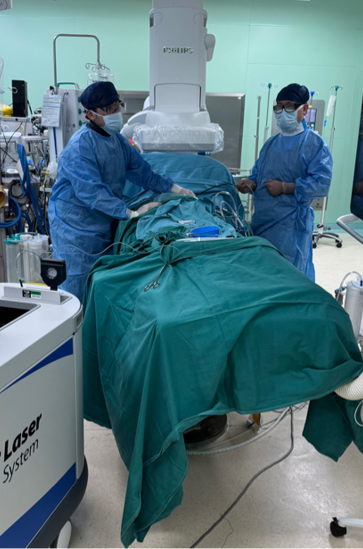
图11-14 由于电极结构损坏,锁紧钢丝只能进入心室电极内部约3-4cm,因此心室电极的牵拉强度非常弱
2. 激光鞘分步消蚀粘连组织
心房电极拔除:上腔静脉造影显示锁骨下静脉、无名静脉及上腔静脉完全闭塞,心房电极与锁骨下静脉粘连非常严重,激光鞘逐步消蚀并与外鞘交替使用缓慢前行,使用超硬泥鳅导丝辅助松解粘连组织(图15-18)。耗时1小时成功拔除心房电极,可见长段粘连组织(图19-22)。
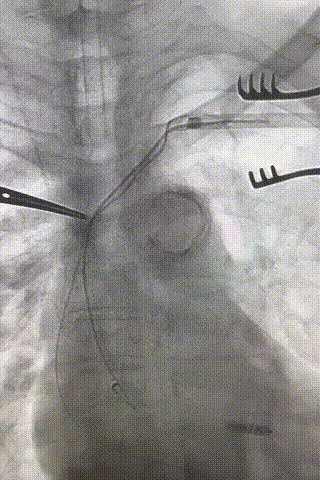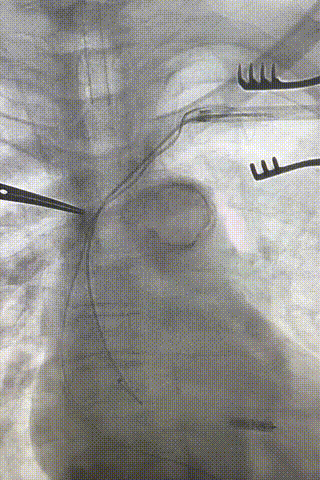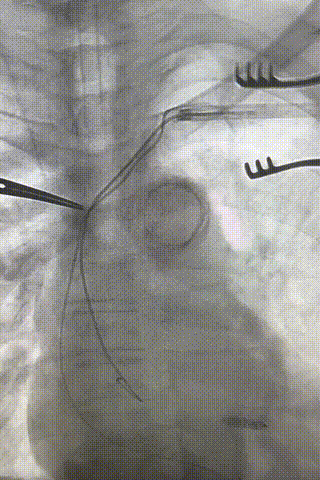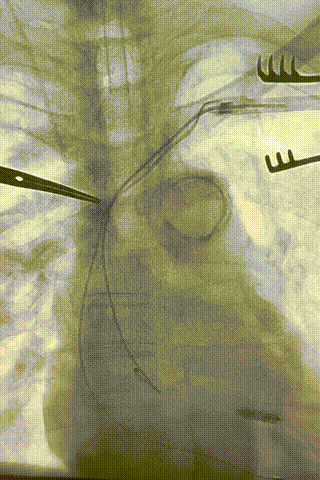
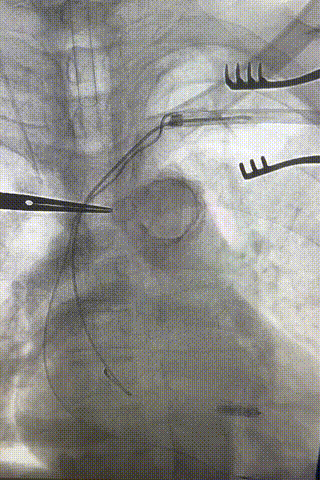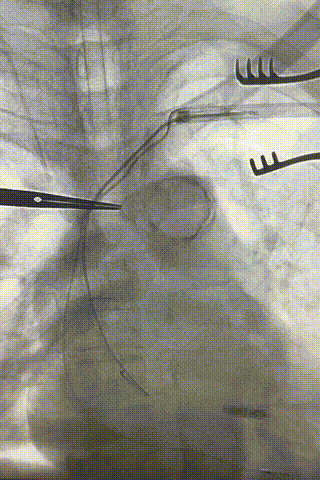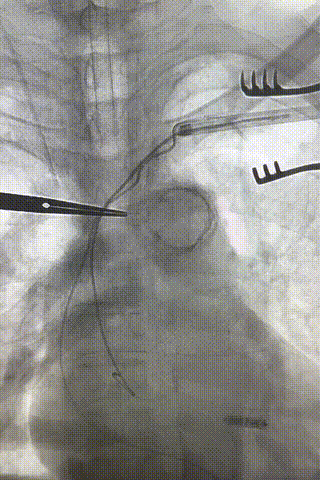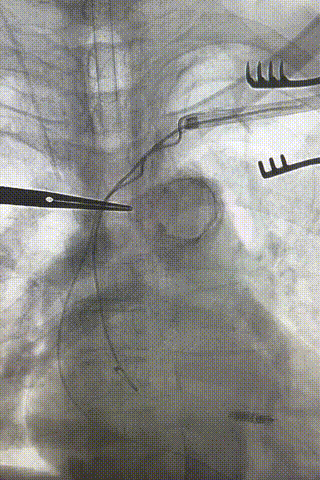
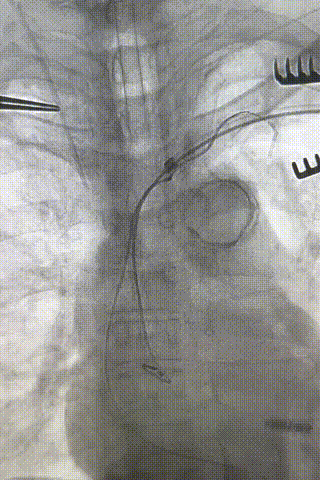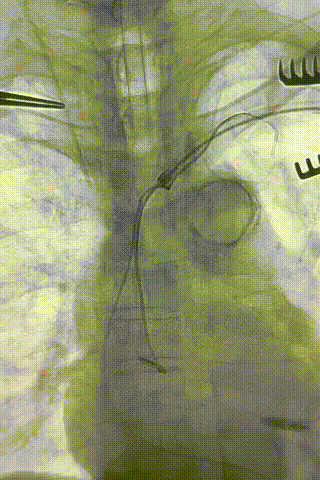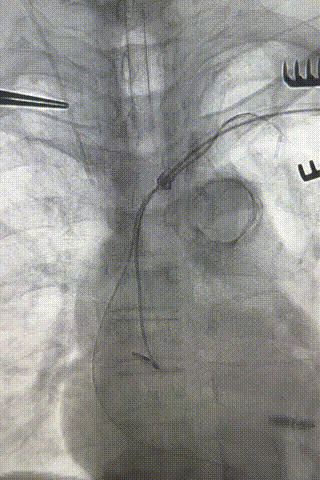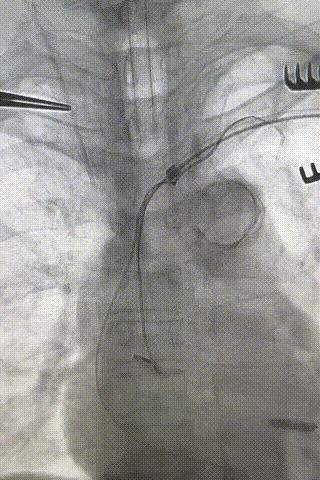
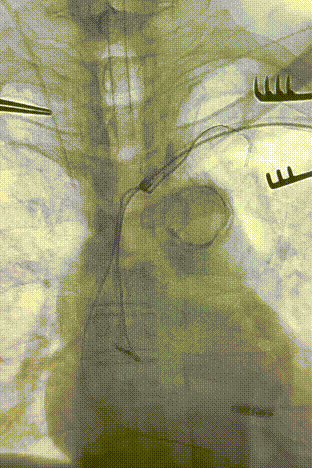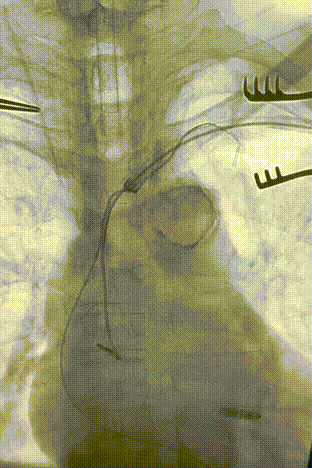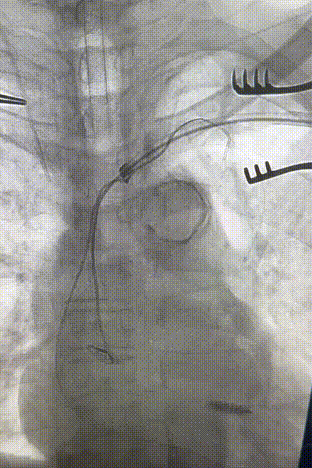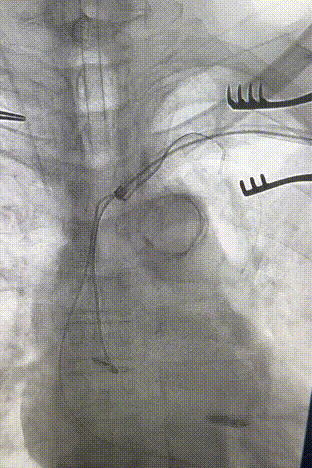
图15-18
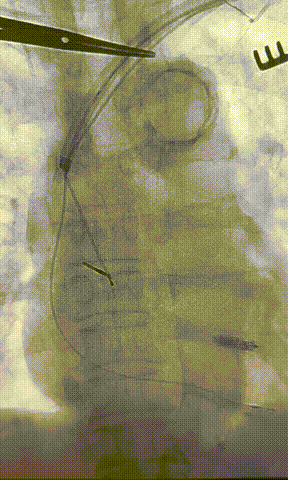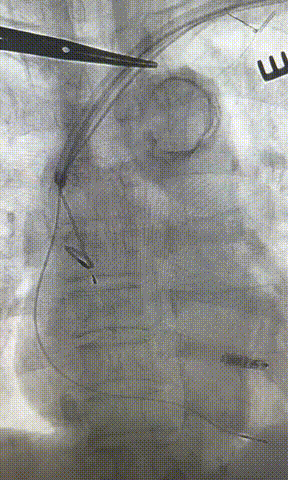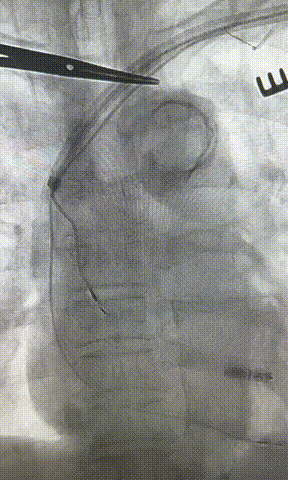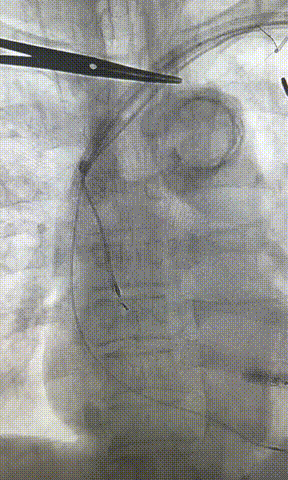
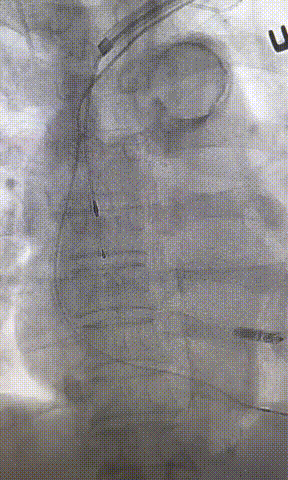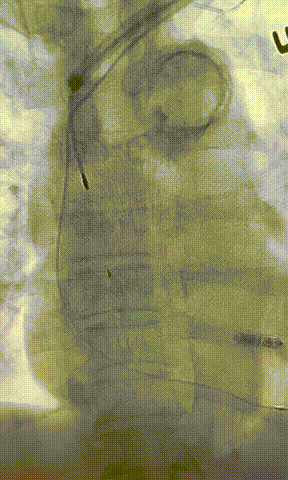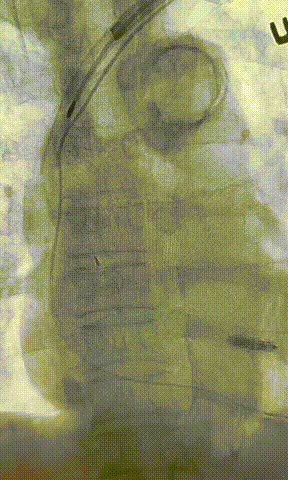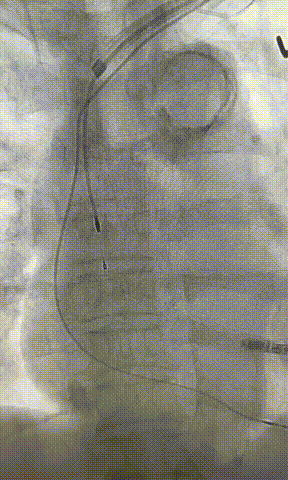
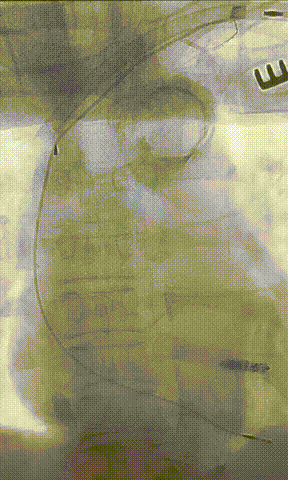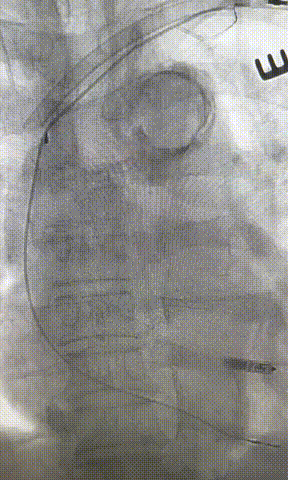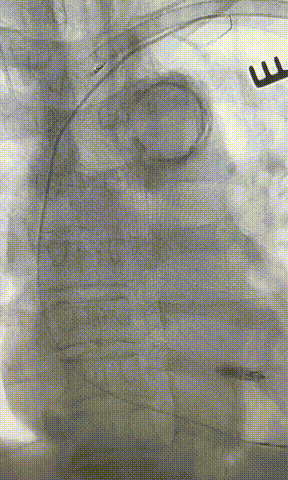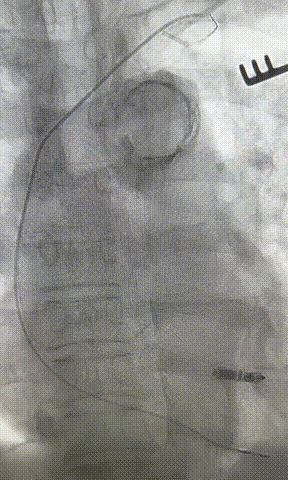

图19-22
心室电极拔除:因锁定钢丝牵引力不足,以外鞘前向分离为主,激光鞘辅助消蚀,逐步分离粘连组织(图23-36),耗时近1小时,激光鞘联合外鞘经三尖瓣进入心室,发现电极与心室壁严重粘连。因牵引力不足,术者凭借心脏解剖经验精准调整角度,利用激光鞘逐步分离粘连组织,最终经外鞘成功剥离电极,可见长段粘连组织(图27-30)。
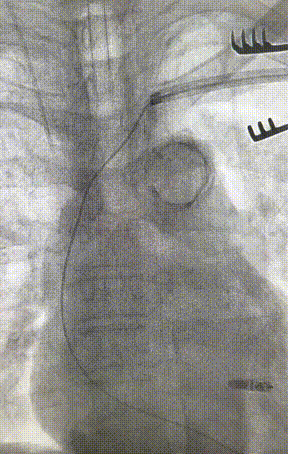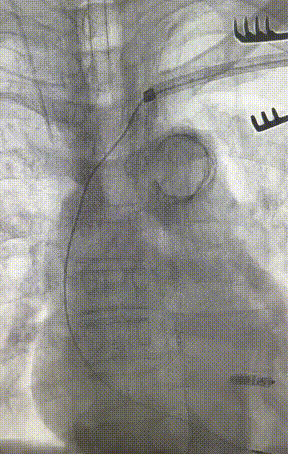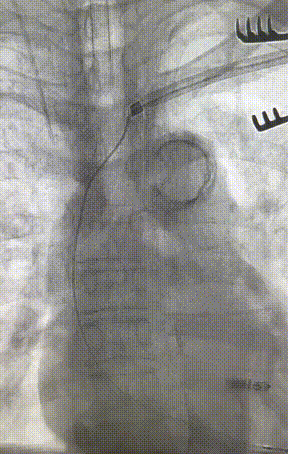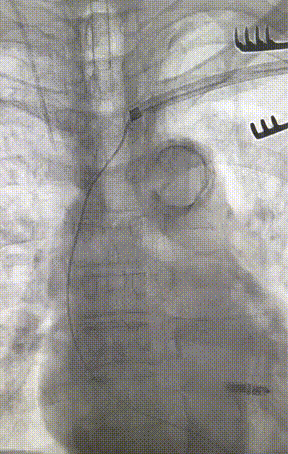
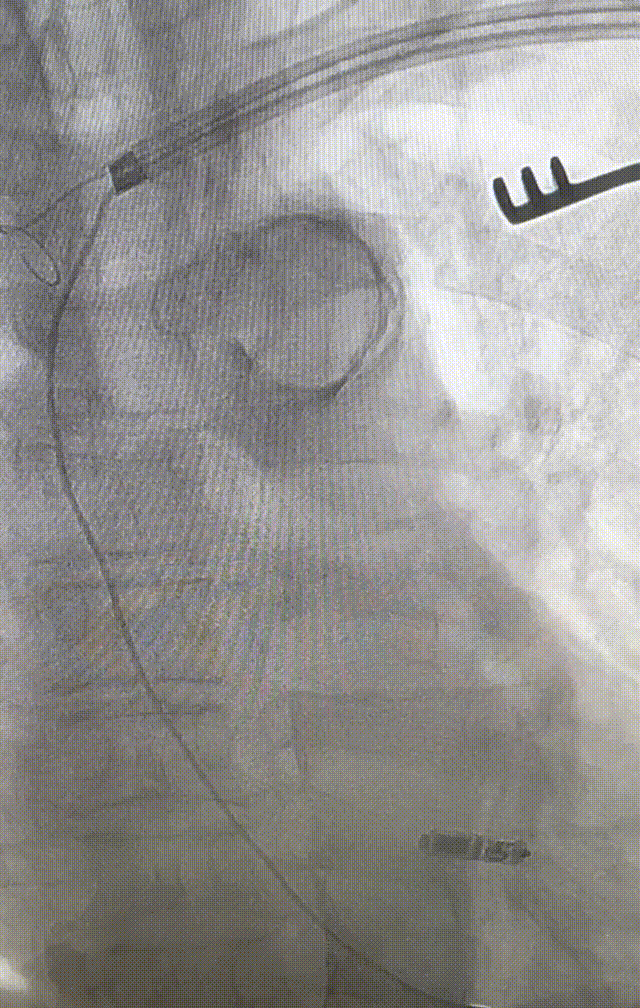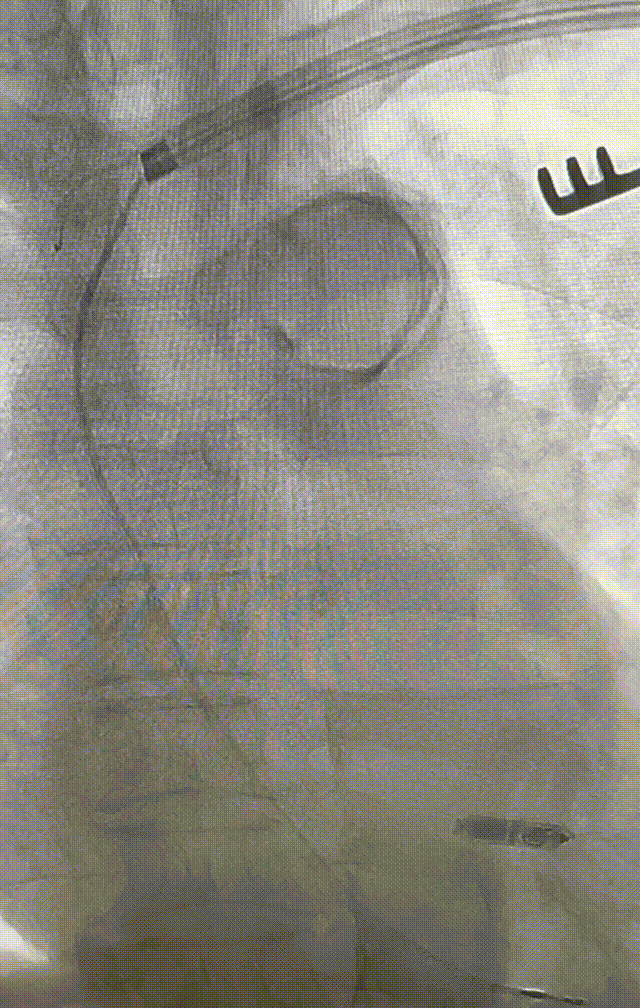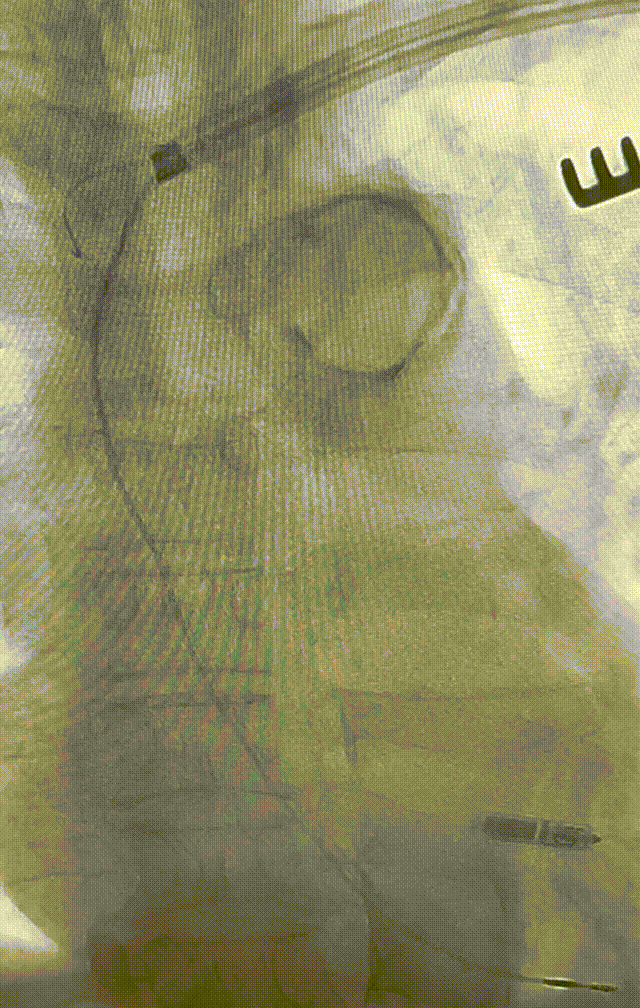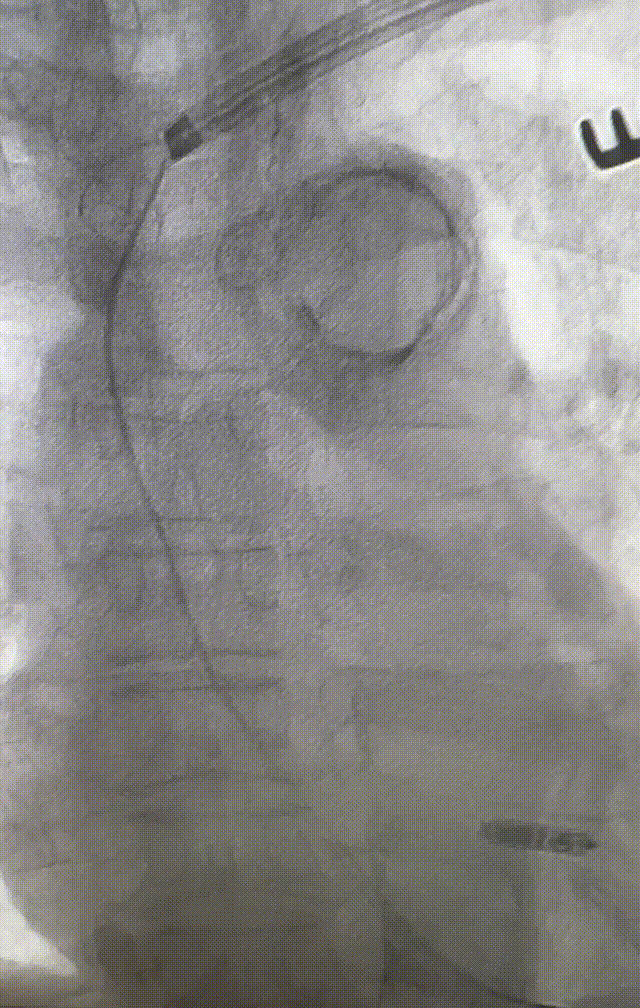
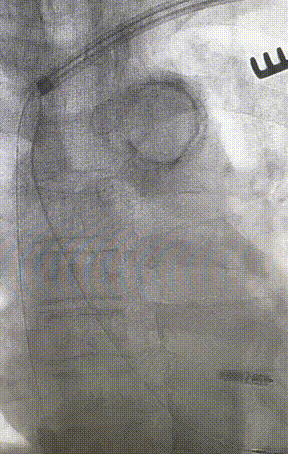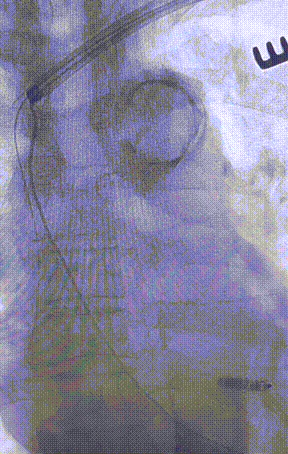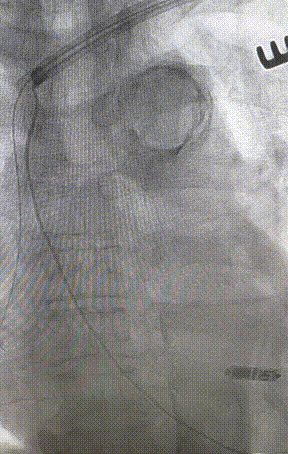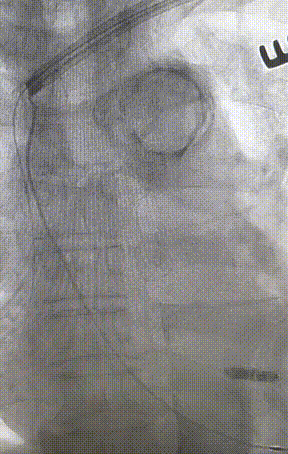
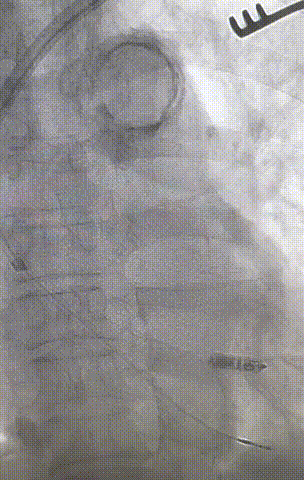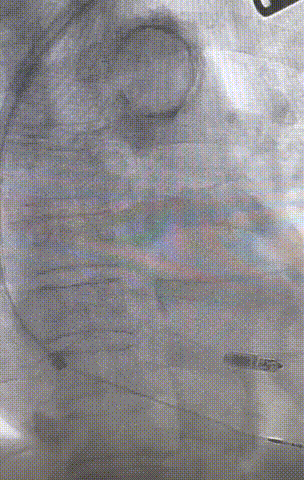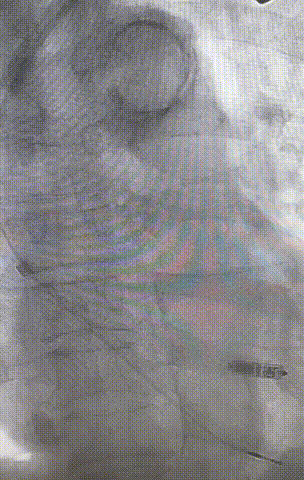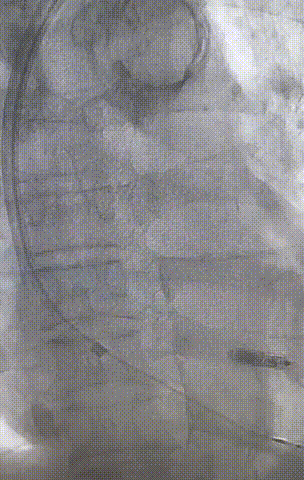
图23-26
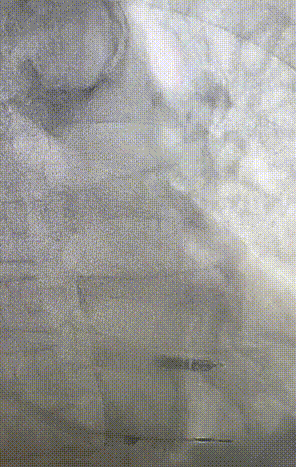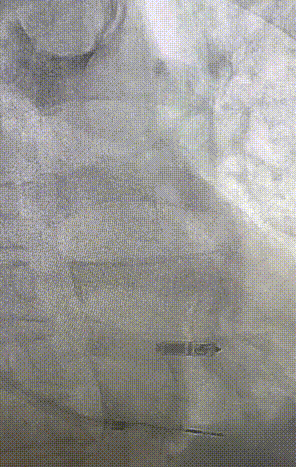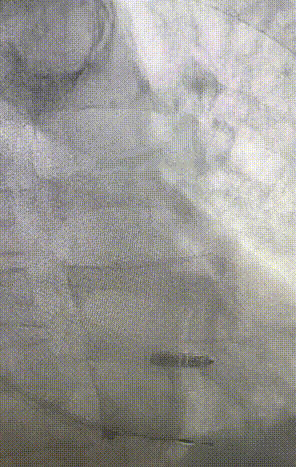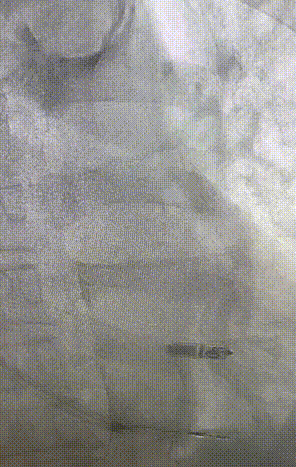



图27-30
手术效果
术后患者感染得到控制,未发生血管撕裂或心脏损伤等并发症。病理证实电极表面存在致密纤维粘连组织。
经验总结
1. 技术创新性:本例首创“外科+激光鞘消蚀”杂交术式,突破传统拔除禁忌,为深埋电极提供新思路。
2. 技术要点:
- 锁紧钢丝可增强脆弱电极的稳定性,但需精准置入;
- 激光鞘与外鞘交替使用,可减少血管损伤风险;
- 术者需熟悉心脏解剖,灵活调整鞘管角度以应对复杂粘连。
3. 临床启示:囊袋感染需彻底移除整套起搏系统,切不可剪断电极导线深埋于锁骨下组织,否则易致感染迁延不愈(如本案例)。
结论
复杂电极拔除需多技术融合与团队协作。激光鞘在低牵引力条件下展现独特优势,但其操作依赖术者经验与耐心。本案例为类似病变提供了可借鉴的解决方案,凸显个体化治疗在起搏器电极导线拔除术中的重要性。