引言:在高血压治疗的药物版图中,α受体阻滞剂犹如一位历经沉浮的“老将”。从20世纪70年代作为一线降压药的辉煌,到ALLHAT研究引发的争议与临床应用低谷,再到近年来随着循证医学证据的积累而重新被认识其独特价值,这类药物的发展历程折射出高血压治疗理念的变迁。《α受体阻滞剂降压治疗中国专家共识》作为国内首部针对该类药物的权威指南,系统梳理了其在难治性高血压、合并症管理及特殊疾病中的应用证据,为临床合理用药提供了重要依据。本文将结合共识内容,深入解析α受体阻滞剂的核心要点,并特别针对临床常见误区进行澄清,以期为广大临床工作者提供全面的用药参考。

《α受体阻滞剂降压治疗中国专家共识》快速理解思维导图
一、历史回顾:从争议到重新定位
1976年,α受体阻滞剂正式开始用于降压治疗,凭借其明确的扩血管机制,迅速跻身六大类一线降压药之列。然而,2000年发表的ALLHAT研究犹如一枚“重磅炸弹”,该研究显示,α受体阻滞剂与噻嗪类利尿剂相比并未显示出明显优势,其临床应用价值因此受到质疑,主要高血压指南不再推荐其作为一线降压药。
近年来,随着对高血压病理生理机制的深入理解及新型研究的开展,学术界对α受体阻滞剂的认识逐渐回归理性。多项研究(如ASCOT-BPLA、PATHWAY-2等)证实,在特定人群中(如难治性高血压、合并良性前列腺增生等),α受体阻滞剂作为附加治疗药物可显著提升降压达标率,且未显著增加心血管风险。
《中国高血压防治指南(2018年修订版)》推荐α受体阻滞剂用于以下强适应证的原发性高血压,包括合并良性前列腺增生、难治性高血压、高脂血症合并高血压等。同时推荐用于继发性高血压,如嗜铬细胞瘤和副神经节瘤等,α受体阻滞剂可抑制这些疾病过程中的交感神经兴奋,起到病因治疗作用,降压效果良好。
2021年《高血压基层合理用药指南》纳入的15种基本降压药中α受体阻滞剂有2种:乌拉地尔与酚妥拉明。乌拉地尔针剂用于高血压危象及重度、极重度、难治性高血压患者紧急快速降压治疗,酚妥拉明针剂用于嗜铬细胞瘤引起的高血压危象。此外,口服乌拉地尔与其他α受体阻滞剂适应证一致,用于原发性高血压、嗜铬细胞瘤导致的继发性高血压及肾性高血压等。

α受体阻滞剂不同剂型的药代动力学特征与用法
二、药理学基础:分类与作用机制的精准解析
(一)分类与药代动力学特征
α受体阻滞剂依据与受体结合时间长短可分为短效与长效两大类:
短效制剂:以酚妥拉明为代表,水溶性高,静脉注射后2分钟达血药浓度峰值,作用持续时间短,主要用于高血压急症(如嗜铬细胞瘤危象)的紧急降压,需持续静脉滴注维持疗效。
长效制剂:包括多沙唑嗪、特拉唑嗪等选择性α₁受体阻滞剂,脂溶性高,血浆半衰期长达10-22小时,缓释剂型血药浓度更平稳,每日给药1次即可实现24小时持续降压,且体位性低血压发生率显著低于短效制剂,成为临床首选剂型。
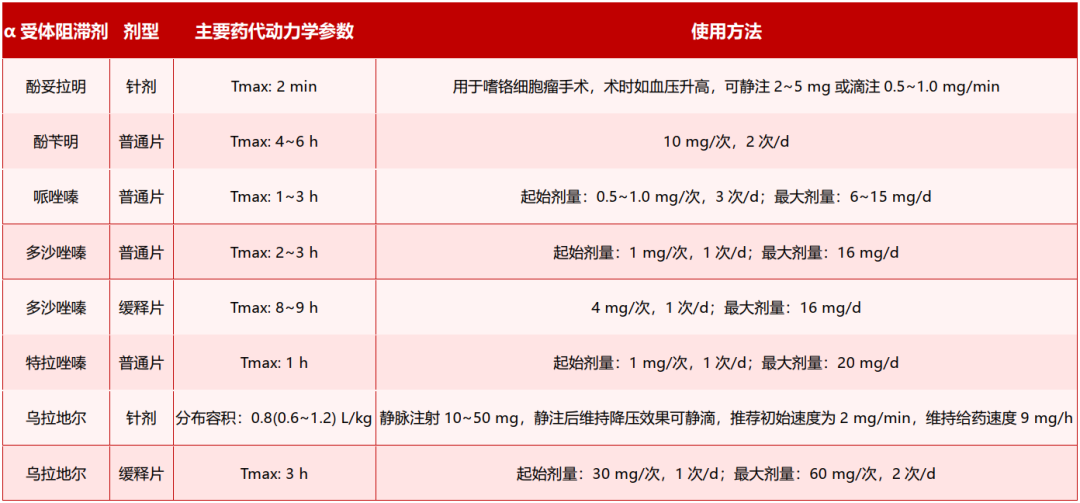
α受体阻滞剂不同剂型的药代动力学特征与用法
(二)作用机制:双重抑制交感神经的独特优势
交感神经激活是高血压发生发展的关键机制之一,α受体阻滞剂通过阻断血管平滑肌α₁受体,直接扩张阻力血管与容量血管,降低外周血管阻力,同时增加肾脏、心脏等器官血流量,改善组织灌注。值得注意的是,乌拉地尔等药物还可通过兴奋中枢5-羟色胺能神经元,抑制中枢交感活性,形成“外周+中枢”双重抑制效应,使其降压效能更优,尤其适用于交感活性过高的高血压患者(如伴心率增快或焦虑状态者)。

常用α受体阻滞剂的药理学特点
三、临床应用场景:从难治性高血压到特殊疾病的多维价值
(一)难治性高血压:联合治疗的关键一枪
难治性高血压定义为在改善生活方式基础上,应用≥3种足量降压药(含利尿剂)且血压仍未达标的情况,其患病率约占高血压人群的10%-15%。α受体阻滞剂在该领域的价值已获多项研究证实:
PATHWAY-2研究:在ACEI/ARB+CCB+利尿剂三联治疗基础上,加用多沙唑嗪作为第四种药物,可使家庭收缩压/舒张压进一步降低8.7/5.1mmHg,达标率提升至41.7%,疗效优于比索洛尔,且安全性良好。
临床观察研究:多沙唑嗪作为附加治疗(2-16mg/d),可使难治性高血压患者收缩压/舒张压平均下降33/19mmHg,因不良反应停药率仅5.2%。
(二)继发性高血压:病因治疗的核心药物
1.原发性醛固酮增多症筛查
醛固酮与肾素比值(ARR)是筛查原醛的关键指标,但β受体阻滞剂、ACEI等药物可干扰检测结果。α受体阻滞剂(如多沙唑嗪)对肾素-血管紧张素-醛固酮系统(RAAS)影响极小,一项纳入230例疑似原醛患者的研究显示,多沙唑嗪对ARR的干扰率仅为-5%,显著低于阿替洛尔(62%),是筛查期间理想的替代降压药。
2.嗜铬细胞瘤
作为嗜铬细胞瘤术前降压的一线药物,α受体阻滞剂(如酚苄明、多沙唑嗪)可通过阻断α受体,对抗肿瘤分泌的儿茶酚胺所致血管收缩,降低血压并扩张血容量,减少术中血压波动及心血管并发症。一项多中心研究显示,酚苄明与多沙唑嗪术前治疗2-3周,两组术中超出靶目标血压的百分比相似(12.2%比11.1%),术后心血管并发症发生率也无明显差异。在手术治疗前,α受体阻滞剂的应用一般不少于2周。对高血压危象患者,可采用速效的α受体阻滞剂酚妥拉明静脉推注,继之以静滴。
(三)特殊类型高血压:合并症管理的“一石二鸟”
1.高血压合并良性前列腺增生(BPH)
我国40岁以上男性BPH患病率达36.6%,其中63.9%合并高血压。选择性α₁受体阻滞剂(多沙唑嗪、特拉唑嗪)可同时作用于前列腺和膀胱颈部平滑肌上的α1受体,实现“降压+改善下尿路症状”双重获益。
2.高血压合并代谢综合征
我国高血压患者合并血脂异常率达58.2%,合并血糖异常率14.7%。α受体阻滞剂在降压的同时具有代谢友好性:
血脂改善: ASCOT-BPLA研究显示其作为附加治疗可使总胆固醇、低密度脂蛋白胆固醇分别降低0.28、0.21mmol/L。
胰岛素抵抗改善:在糖代谢异常患者中,多沙唑嗪可使空腹血糖降低0.23mmol/L,稳态模型胰岛素抵抗指数(HOMA-IR)改善18.2%,联合阿卡波糖治疗可使糖化血红蛋白进一步降低0.6%。
3.高血压合并慢性肾脏病(CKD)
α受体阻滞剂通过扩张出球小动脉,降低肾小球内压,同时增加肾血流量,保护高血压合并CKD患者的肾功能。
四、用药指导:从剂量滴定到不良反应管理
(一)适应证与药物选择
α受体阻滞剂一般不作为高血压一线治疗药物。该类药物的主要特点是没有明显的代谢不良反应,因此可用于合并糖尿病及高脂血症的高血压患者,也可用于合并外周血管病、哮喘的患者。

α受体阻滞剂的适应证
(二)禁忌证与慎用人群
绝对禁忌证:体位性低血压、近期心肌梗死、胃肠道梗阻、喹唑啉类药物过敏。
慎用人群:心力衰竭(因ALLHAT研究提示潜在风险,暂不推荐)、冠心病(避免静脉快速推注,可能诱发心绞痛)、胃炎/胃溃疡(可能加重消化道症状)。
(三)联合用药原则
1. 如患者血压未控制,α受体阻滞剂可与β受体阻滞剂、ACEI、ARB、CCB、噻嗪类利尿剂联合应用,但一般不作为首选,通常在一线降压药物联合治疗血压仍不达标时使用。
2.与β受体阻滞剂联合用于嗜铬细胞瘤患者降压治疗时,应先使用α受体阻滞剂,再使用β受体阻滞剂;停药顺序为:先停用β受体阻滞剂,再停用α受体阻滞剂。
3.难治性高血压患者合并高尿酸血症不宜使用利尿剂时,或长期使用β受体阻滞剂导致男性性功能障碍等不良反应时,均可考虑优先使用α受体阻滞剂作为ACEI+CCB的第三种降压药。
(四)用药时间
1.乌拉地尔等短效α受体阻滞剂应根据临床需要使用,常为短时间内一次性给药;
2.特拉唑嗪、多沙唑嗪等长效α受体阻滞剂应根据剂型不同给药,通常,普通片应在每晚睡前服用,而缓释剂型可根据血压情况在睡前或白天服药。
(五)体位性低血压与处理
α受体阻滞剂在应用过程中可能出现体位性低血压,初次使用或停药后再次使用者要特别注意。预防措施包括睡前服药、避免突然站立、晨起排便时动作缓慢。如若发生体位性低血压,应迅速安排平躺,并可予快速饮水扩大血容量,还可以采取收缩肌肉等措施加大外周血管阻力,增加回心血量,如抬脚趾、双腿交叉收缩、抬腿等。
结语
α受体阻滞剂绝非高血压治疗的“过气药物”,而是在特定领域具有不可替代价值的“精准武器”。尽管其非一线治疗地位明确,但其在难治性高血压的附加治疗、继发性高血压的病因控制、合并BPH/代谢综合征/CKD等特殊人群中的疗效已获充分证据支持。临床实践中,需摒弃“一刀切”的陈旧观念,基于患者病理生理特征、合并症及用药史,合理选择药物种类与剂量,遵循个体化用药原则,同时警惕常见误区,方能最大化发挥其临床价值,为高血压患者带来更优的治疗结局。