
在心血管疾病治疗领域,经皮冠状动脉介入治疗(PCI)是冠心病治疗的重要手段。自2009、2012和2016版中国PCI指南发布以来,国内外又积累了众多临床研究证据,PCI策略和技术进一步完善,欧美也连续更新了指南。在此背景下,中华医学会心血管病学分会介入心脏病学组、中华心血管病杂志编辑委员会组织专家,在既往中国PCI指南基础上,根据国际、国内的最新临床研究结果,参考新近ACC/AHA以及ESC发布的系列指南,结合我国国情及临床实践,更新编写了2025年版《经皮冠状动脉介入治疗指南》(以下简称“2025版指南”),为临床医师提供了更具针对性和实用性的指导。
严道医声网将2025版指南与2016版指南的差异和新增要点进行深入剖析,制作了多幅图表,帮助各位同道快速掌握2025版指南的核心要点。
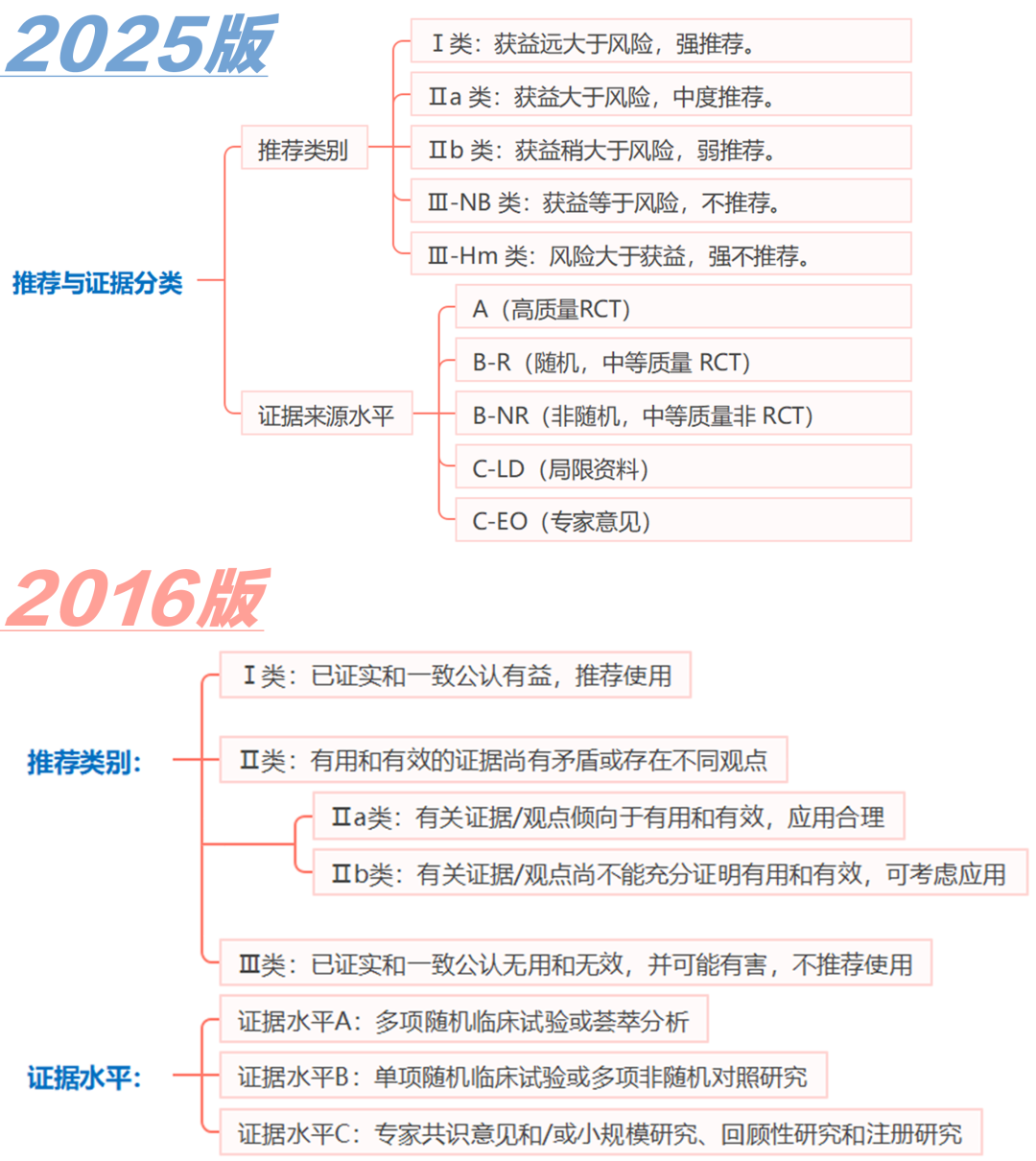
(一)推荐类别与证据水平细化
2025年版指南采用了ACC/AHA新的推荐类别与证据水平标准。推荐类别新增Ⅲ-NB(获益等于风险,不推荐)、Ⅲ-Hm(风险大于获益,强不推荐);证据水平新增B-R(随机证据)、B-NR(非随机证据)、C-LD(局限资料)、C-EO(专家意见)。这一细化使得推荐意见更加精准,有助于临床医生根据不同的证据质量做出决策。
(二)质量控制体系细节
2016 年版:要求PCI中心每年完成心血管疾病介入诊疗病例不少于200例,治疗性病例不少于100例,主要操作者具备资质且每年独立完成PCI>50例,对血管造影并发症发生率和心血管病介入诊疗技术相关病死率提出明确指标。
2025 年版:进一步细化质量控制内容,增加对介入医师规范培训、准入和质量监督制度的要求,强调定期分析本中心所有术者的PCI患者结局数据,引入“心脏团队”会诊机制,并接受区域质量控制专家组随机抽查和讨论。
(三)危险评分系统
2016 年版:提及EuroSCORE Ⅱ、SYNTAX评分、SYNTAX Ⅱ评分等,说明其特点及在血运重建决策中的作用,并指出部分评分系统源于欧美人群,存在一定程度的适用性差异。
2025 年版:除上述评分系统外,新增STS评分,更深入阐述中国NERS Ⅱ评分的优势及应用价值,强调其用于无保护左主干病变,预测主要不良心脏事件优于SYNTAX评分。
1. SYNTAX评分:是依据11项冠状动脉造影显示的病变复杂程度即解剖特点,评价PCI或CABG术后≥1年风险的评分方法。临床主要用于冠状动脉左主干和(或)多支病变患者选择PCI或CABG时参考,是PCI介入医师最常用的风险评分。
2. SYNTAX Ⅱ评分:其在SYNTAX评分基础上,新增了6项临床指标(年龄、肌酐清除率、左心室功能、性别、是否合并慢性阻塞性肺疾病和周围血管病),只用于预测远期死亡率 。
3. STS评分:为(美国)胸外科医师协会的评分系统,本评分从患者基本情况、手术复杂程度、术后预后等3个方面,评估患者在CABG术后住院期间和30d的死亡风险。
4. EuroSCORE Ⅱ评分:为欧洲心脏手术风险评估系统Ⅱ,本评分基于18项临床指标建立,局限于评估CABG术后住院期间和30d的死亡风险。
对于无保护左主干病变患者,中国的NERS Ⅱ评分联合了临床指标和冠状动脉病变解剖学特征,可预测主要不良心脏事件发生率,结果优于SYNTAX评分,>19分是主要不良心脏事件和支架内血栓的独立预测因素。
(四)血运重建策略选择
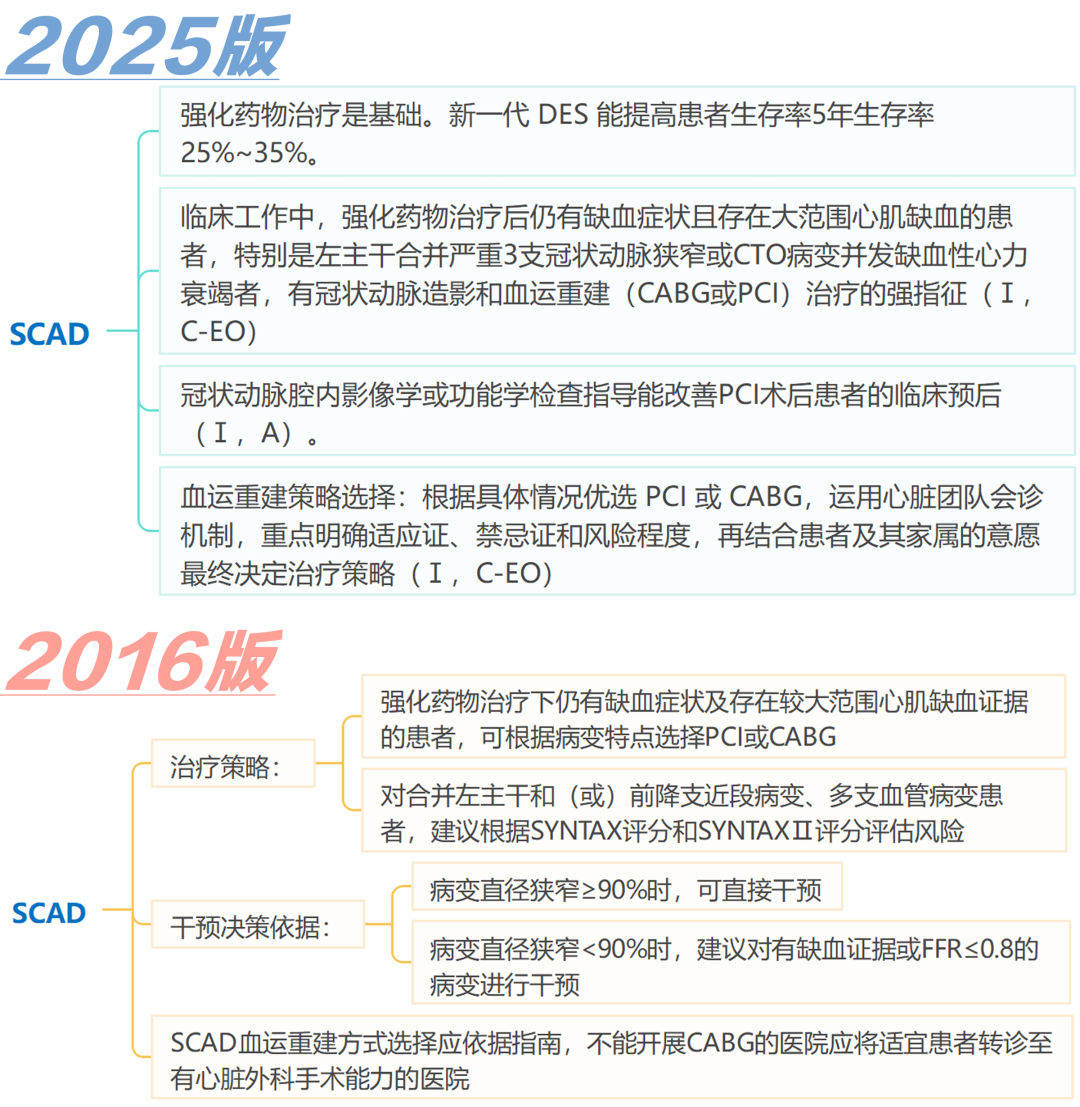
稳定性冠心病(SCAD):
2016 年版:根据冠状动脉病变直径狭窄程度、血流储备分数(FFR)等作为干预决策依据,对不同冠心病程度(解剖/功能)的治疗推荐提供具体建议,如左主干直径狭窄>50%、前降支近段直径狭窄>70%等情况的处理方案,并依据SYNTAX评分和SYNTAX Ⅱ评分评估中、远期风险以选择血运重建策略。
2025 年版:进一步明确SCAD患者强化药物治疗的基础地位,指出新一代药物洗脱支架(DES)的优势,细化血运重建(PCI或CABG)指征,强调冠状动脉腔内影像学或功能学检查指导对改善PCI术后预后的重要性,更全面阐述左主干病变、多支病变合并糖尿病等复杂情况的治疗策略选择,推荐运用心脏团队会诊机制综合考虑多种因素后确定治疗方案。
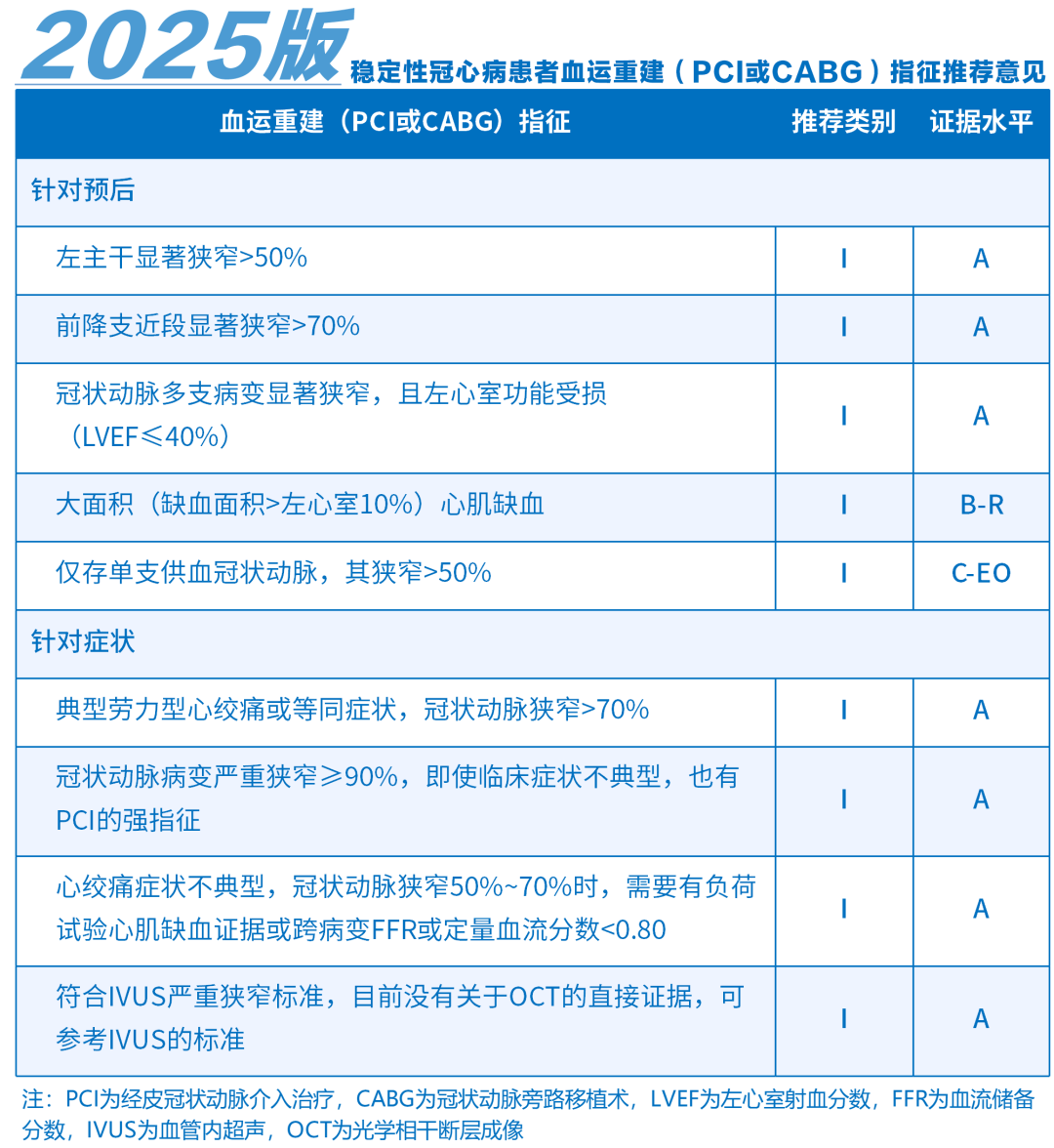
非ST段抬高型急性冠状动脉综合征(NSTE-ACS):
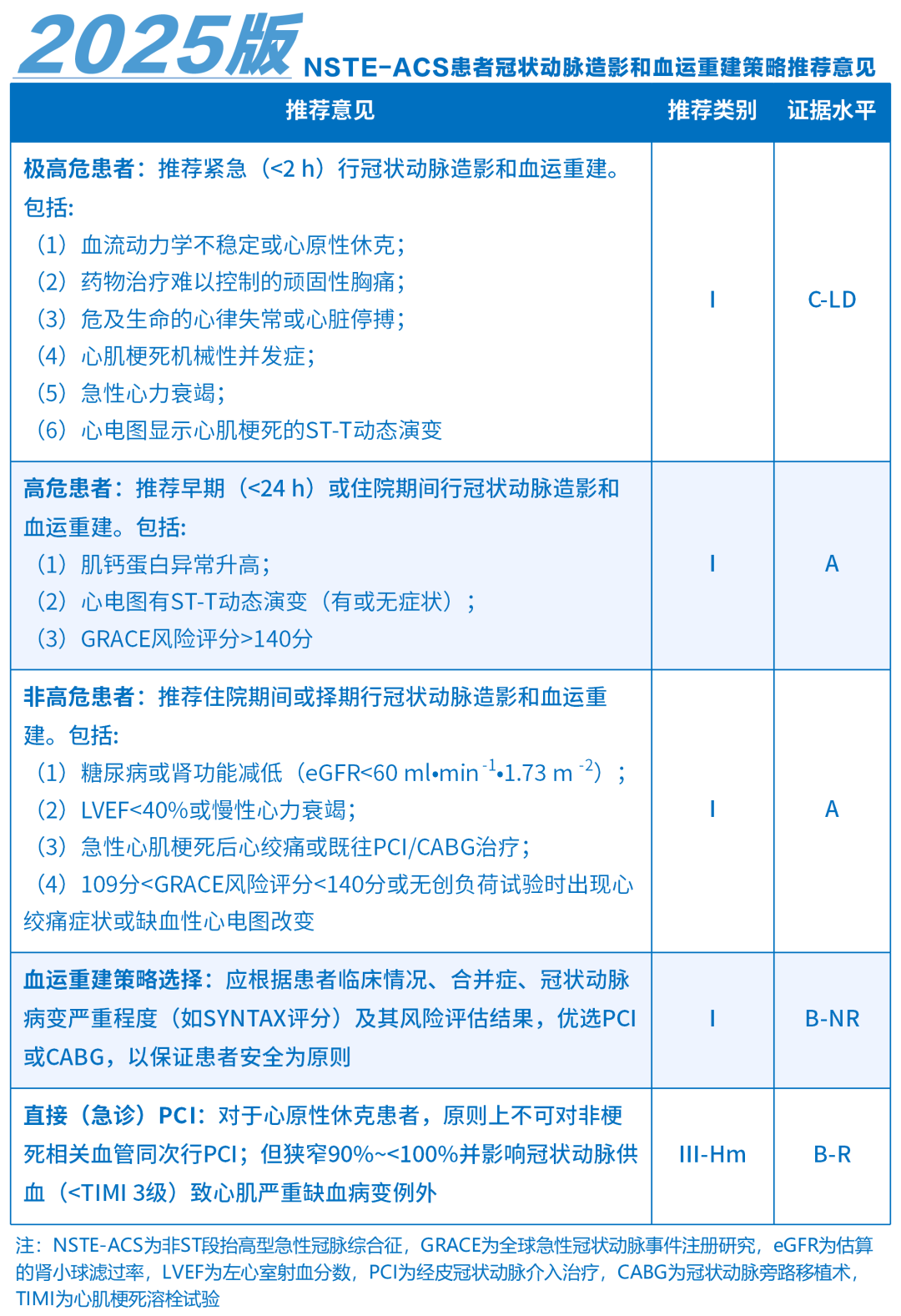
2016 年版:推荐用高敏肌钙蛋白检测作为早期诊断工具之一,根据即刻和1h水平快速诊断或排除NSTEMI,采用GRACE预后评分进行缺血危险分层,并依据分层结果制定不同时间框架内的血运重建策略。
2025 年版:同样强调高敏肌钙蛋白检测的重要性及GRACE评分的应用,但对不同危险分层患者的冠状动脉造影和血运重建时间建议更加细化和精准,如极高危患者推荐紧急(<2h)行相关操作,高危患者推荐早期(<24h)或住院期间进行等,同时更明确地提出血运重建策略选择应综合患者临床情况、合并症、冠状动脉病变严重程度及风险评估结果,优选PCI或CABG,以保证患者安全为原则。对于首诊于非PCI中心的患者,危险分层属于极高危者,建议立即转运至PCI中心行紧急PCI;高危者,建议发病24h内转运至PCI中心行早期(<24h)或住院期间PCI;非高危者,建议转运至PCI中心,住院期间或择期行PCI或CABG,或药物保守治疗。
急性ST段抬高型心肌梗死(STEMI):
2016 年版:着重强调减少时间延误对STEMI实施再灌注治疗的关键性,明确首诊可开展急诊PCI医院的FMC至PCI时间要求(<90min),以及首诊不能开展急诊PCI医院的患者转运时间要求(预计FMC至PCI的时间延迟<120min应转运至有直接PCI条件的医院),对溶栓后PCI的时间窗、适应证及操作建议等进行说明。
2025 年版:在延续上述核心要点的基础上,对不同发病时间范围内的STEMI患者是否行急诊PCI及其优先级做出更详尽的阐述,如发病>12h伴特定高危情况的患者考虑在循环支持下行急诊PCI,发病12~24h病情稳定的患者常规冠状动脉造影必要时开通IRA等,同时增加了对合并多支血管病变的STEMI患者给予完全血运重建策略的推荐,以及对急诊PCI同台对非IRA支架置入的条件和场景的分析。
STEMI患者直接(急诊)PCI策略的推荐意见
对于发病12h以内的所有STEMI患者,均应给予直接PCI (Ⅰ,A);
对于ST段抬高不明显,但存在以下1项及以上严重并发症的患者,也应给予直接PCI(Ⅰ,C-EO):
(1)心原性休克或血流动力学不稳定
(2)持续性胸痛不缓解
(3)致命性心律失常或心脏骤停
(4)心脏机械并发症
(5)急性心力衰竭
(6)间歇性ST-T改变,尤其是回落ST段再抬高
在特定时间范围内,直接PCI优先于溶栓治疗(Ⅰ,A);
对于发病时间>12h(超窗),仍存在心肌缺血的症状或体征、血流动力学不稳定或致命性心律失常的极高危患者,也应考虑在机械循环辅助下,给予直接PCI(Ⅱa,A);
对于发病时间为12~24h且病情稳定的患者,常规冠状动脉造影必要时行PCI开通闭塞的IRA可能是有益的(Ⅱa,A);
对于发病时间24~48h,无缺血症状、证据且病情稳定的患者,原则上不建议给予直接PCI,因为获益/风险不可预测(Ⅱb,A);
对于发病时间>48h,无缺血症状、ST段回落到等电位线且病情稳定的患者,不建议给予PCI,因为即使开通闭塞的IRA,可能有害(Ⅲ-Hm,B-R);
对于首诊于有条件行急诊PCI的医院的患者,确诊STEMI至PCI时间应<60min;对于院前转运来院患者,确诊STEMI至PCI时间应<90min(Ⅰ,A);
直接PCI开通IRA需常规置入DES,血栓性病变或无复流高风险时例外(Ⅰ,A);
对于伴多支冠状动脉病变的STEMI患者,急诊PCI只开通IRA,非IRA原则上行择期PCI或CABG(Ⅰ,A);
对于部分病情稳定、多支病变的STEMI患者,低风险的简单非IRA病变,也可考虑同期PCI(Ⅱa,A);
对于STEMI并发心原性休克患者,只开通IRA,对非IRA不行PCI(Ⅲ-Hm,A)
对于极少数心原性休克患者,只在非IRA严重狭窄已影响供血(狭窄≥90%、血流<TIMI 3级),且为非CTO病变时,才有同期PCI的强指征(Ⅰ,C-EO);
STEMI患者溶栓后PCI策略的推荐意见
对于所有溶栓治疗后患者,均应送至有条件行PCI的中心,及时行冠状动脉造影(Ⅰ,A);
溶栓成功后24h内,应行冠状动脉造影及必要时对IRA行PCI(Ⅱa,B-R);
心原性休克或严重心力衰竭患者溶栓后,应常规行急诊冠状动脉造影并对闭塞的IRA行PCI (Ⅰ,B-NR);
对临床判断溶栓失败者(溶栓后60min ST段下降<50%或仍有胸痛)应行补救性PCI (Ⅰ,A);
溶栓成功后出现再发缺血、血流动力学不稳定、危及生命的心律失常或有再次闭塞证据时需行急诊PCI(Ⅰ,A);
溶栓成功后血流动力学稳定的患者应在2~24h行急诊冠状动脉造影,必要时对IRA行PCI (Ⅱa,A);
STEMI患者院前急救转运和转诊策略的推荐意见
STEMI患者院前转运:应基于区域急救网络,将患者快速就近转运至有条件的中心行急诊PCI(Ⅰ,B-NR);
建立区域急救网络并联通:所有区域内急救系统、医疗中心急诊科、导管室和冠心病监护病房均应依据STEMI指南,与区域急救网络联网,共享有条件PCI中心的24h/7d的急诊响应服务,随时实施急诊PCI(Ⅰ,C-EO);
急救转运绕行:将患者转运至有PCI资质的中心,在能安全对接条件下,可绕行急诊室直接送到导管室行急诊PCI(Ⅰ,B-NR);
无PCI条件医院转入与转诊:若患者就诊于或被转运至无PCI条件的医院时,如预计转运或转诊后能在<120min开通IRA,应于30min内转出至有条件医院行急诊PCI(Ⅰ,B-R);
院前或院内溶栓治疗:STEMI患者在院前或无条件行PCI的医院,若预计转运或转诊至有急诊PCI条件的医院的时间>120min,只要无出血等禁忌证,则应进行院前和院内溶栓治疗,并需<10min启动溶栓(Ⅰ,A);
(五)PCI术中操作及重要技术
介入治疗入路选择:
2016年版:推荐经桡动脉径路作为首选,指出其血管相关并发症少、患者痛苦少的优势。
2025年版:继续推荐经桡动脉入路为首选,同时补充说明经尺动脉和远桡动脉入路可作为补充,经肱动脉入路只在经股、桡动脉均失败后选择(Ⅰ,C-EO),且需高年资(独立术者年限>5年)PCI术者实施或指导实施。
血管内超声(IVUS)和光学相干断层成像(OCT):
2016 年版:阐述IVUS在造影结果不明确或不可靠情况下的应用价值,如对开口病变、血管重叠及分叉病变等的指导作用,以及对支架失败原因的查明和优化支架置入的辅助功能;提及OCT对明确血栓、斑块破裂及支架膨胀不良等的价值优于IVUS,但指出尚无大规模前瞻性随机对照试验探讨OCT指导的PCI治疗。
2025 年版:进一步强调IVUS和OCT对确定临界病变PCI指征界值、指导复杂病变策略选择和优化支架置入的重要性,详细说明IVUS在不同病变类型中的具体应用,如左主干病变、真性分叉病变、长病变等,以及OCT在显示斑块性质、纤维帽厚度、支架贴壁情况等方面的优势,并提出相应的操作建议和推荐级别。
对于解剖复杂病变,特别是左主干病变、真性分叉病变和长病变,推荐应用腔内影像(包括IVUS或OCT)指导PCI以减少缺血事件(Ⅰ,A)。
对复杂CTO病变,IVUS有助于明确闭塞入口、判断导丝走行在血管壁结构内或真腔,提高PCI成功率和安全性(Ⅱa,C-EO)。
为预防血栓,IVUS指导下的支架理想置入标准(MUSIC标准)为:
(1)支架完全贴壁
(2)支架内最小管腔横截面积≥平均远端参考血管横截面积的90%
(3)偏心指数≥0.7
IVUS预测DES置入后远期不良事件的独立危险因素有:MLA≤5mm²、支架边缘斑块负荷≥50%、支架边缘夹层、弥漫的支架贴壁不良。
OCT在明确显示STEMI患者IRA内造影无法识别的斑块破裂、微血栓和斑块侵蚀,钙化病变形态、范围和厚度甚至钙化结节,以及置入支架贴壁情况方面比IVUS价值更高(Ⅱa,B-R)。
血流储备分数(FFR)和定量血流分数:
2016年版:肯定FFR在反映心外膜下冠状动脉狭窄功能学严重程度方面的作用,对SCAD患者在特定情况下进行FFR评估的推荐,以及FAME研究、FAME2研究等对FFR指导PCI的意义。
2025年版:补充定量血流分数的优势,即无需额外器械和给药,与FFR界值相同,并强调两者指导的PCI均能改善患者预后,同时对FFR在不同病变类型中的应用提供更明确的建议,如左主干临界病变的评估等。
支架选择:
2016年版:对比第一代和新一代DES的特点,推荐新一代DES在多种情况下的应用,提及完全生物可降解支架的发展方向及初步临床试验结果。
2025年版:更深入地分析新一代DES的优势,如新材料、新抗增生药物、生物相容性更好涂层材料的应用等,明确其作为PCI常规使用的支架地位,并对生物可吸收支架(BRS)的临床应用提出更具体的要求,术者需严格掌握BRS适应证,避免在小血管、严重钙化病变、弥漫长病变等复杂病变中使用,规范的操作(充分的预处理、合适的支架直径及适宜的后扩张)是成功的关键,并建议在腔内影像学指导下置入(Ⅱa,C-EO)。
药物洗脱球囊:
2016年版:推荐药物洗脱球囊治疗BMS或DES支架内再狭窄病变,并提及对小血管病变等的疗效。
2025年版:继续推荐其作为DES支架内再狭窄的首选治疗方式,同时指出对小血管、分叉或多分支病变和高出血风险患者的优势,并对CABG静脉桥血管病变的治疗提出可能的替代方案及相应的推荐级别。
药物洗脱球囊通过在局部释放球囊表面载药(紫杉醇、西罗莫司、优美莫司等)达到抗内膜增值效果,是DES支架内再狭窄的首选治疗方式(Ⅰ,A)。
对小血管、分叉或多分支病变和高出血风险患者具有优势。
对于CABG静脉桥血管病变,理论上比支架置入并发无复流的风险更低(Ⅱb,C-EO)。
血栓抽吸装置:
2016年版:基于多项试验结果,不推荐直接PCI前进行常规冠状动脉内手动血栓抽吸,但对于血栓负荷较重、支架内血栓等特殊情况可选择性使用或作为应急手段。
2025年版:明确不应常规行冠状动脉内血栓抽吸,但对于血栓负荷较重、支架内血栓以及血栓性静脉桥血管病变仍应使用,以降低冠状动脉栓塞和无复流的风险,并给出相应的推荐级别(Ⅱa,C-EO)。
冠状动脉斑块旋磨术:
2016年版:对无法充分扩张的纤维性或严重钙化病变,推荐置入支架前采用旋磨术,但不推荐对所有病变常规使用。
2025年版:在保留上述要点的基础上,补充说明严重钙化病变的处理需用IVUS或OCT评价钙化程度(截面弧度、厚度和长度),对不同程度钙化病变提出相应的处理方法,如轻、中度钙化使用非顺应性、切割或棘突球囊等充分扩张并置入支架,严重钙化需旋磨或联合其他技术,并指出冠状动脉旋磨、准分子激光冠状动脉斑块消蚀术和冠状动脉血管内碎石术对钙化斑块作用的机制不同、各有所长,可根据钙化病变特点单独或联合使用。
机械循环辅助:
2016年版:对STEMI合并心原性休克患者,不推荐常规应用主动脉内球囊反搏(IABP),但对特定情况可用IABP支持,提及体外膜肺氧合(ECMO)等左心室辅助装置在有条件时可选用。
2025年版:更广泛地涵盖机械循环辅助装置的应用场景,强调对高危患者实施PCI时常规使用机械循环辅助装置的重要性,详细阐述IABP在不同情况下的具体应用指征和效果,同时对ECMO、导管轴流泵等装置的作用、适应证及临床研究结果进行说明,并给出相应的推荐级别。
对有心原性休克、失代偿性心力衰竭、血流动力学不稳定、严重心律失常甚或心肺复苏史等极高危患者实施PCI,应常规使用机械循环辅助装置(Ⅱa,C-EO)。
IABP能降低左心室后负荷、增加心脏每搏量并能优先为心脑供血。
对STEMI并发心原性休克患者,对升压药物治疗效果不佳、血流动力学不稳定或并发了急性左心衰者,均应从速使用IABP支持(Ⅰ,C-EO);
STEMI机械并发症患者,发生血液动力学不稳定、心原性休克、急性左心衰时,也均需IABP支持(Ⅰ,C-EO);对直接PCI术中出现任何并发症致血流动力学不稳定者,也应立即给予IABP支持(Ⅰ,C-EO);
对于反复心肌缺血发作药物难以控制,以及心功能严重低下患者,无论是急诊还是择期PCI时,也应予以IABP循环支持(Ⅱa,C-EO);
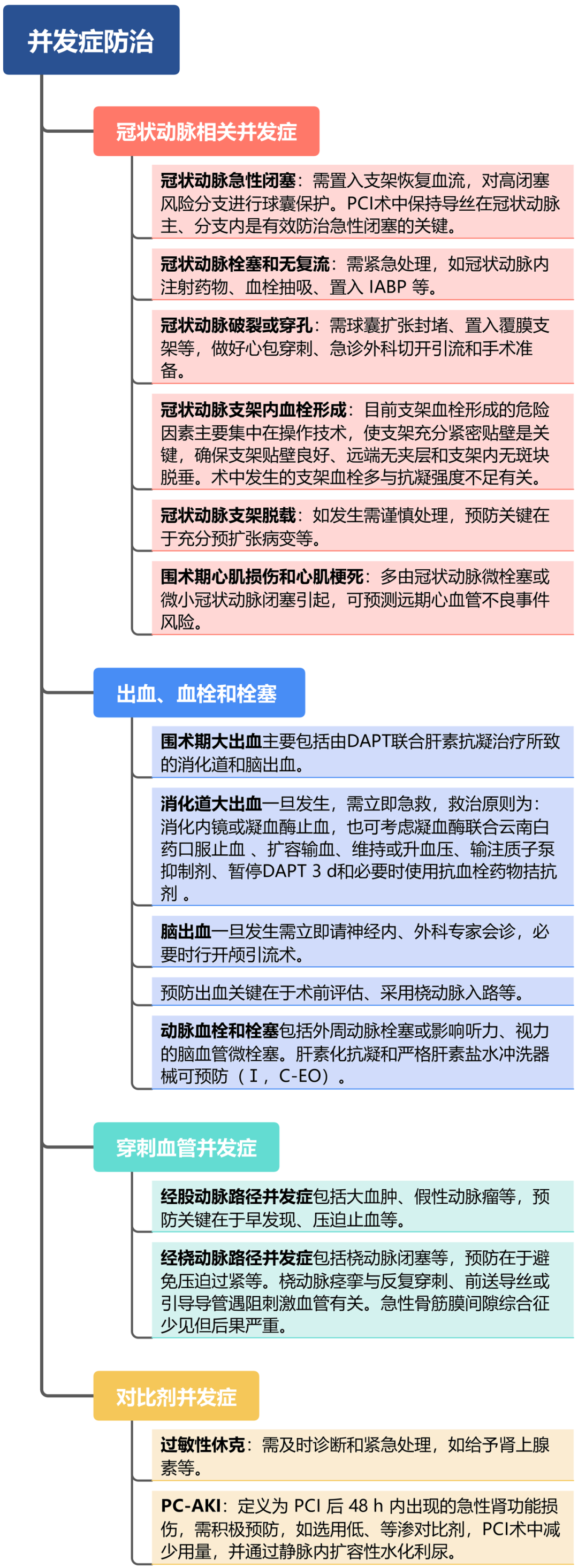
(六)PCI主要并发症防治措施
2016 年版:简要提及PCI主要并发症的可能原因和紧急处理原则等。
2025 年版:进一步细化PCI主要并发症的处理措施,并发症防治策略更为完善:
对比剂肾损伤防治:在对比剂相关肾损伤方面,2025版指南将其定义更新为PC-AKI(对比剂诱导的急性肾损伤),并细化了风险分层。推荐使用等渗对比剂以降低肾损伤风险,同时新增无对比剂PCI(IVUS指导)这一策略,为高风险患者提供了新的选择。
冠状动脉穿孔处理优化:对于冠状动脉穿孔这一严重并发症,2025版指南进一步强调对小穿孔和大穿孔的不同处理策略,以及在准备外科手术过程中如何保障心肌供血的措施,新增了微导管远端供血预防心肌缺血的方法,同时补充明胶海绵颗粒糊剂等封堵材料的应用。
无复流治疗强化:在无复流的治疗上,2025版指南强调紧急处理方法。冠状动脉无复流一旦发生,需紧急处理,立即于冠状动脉内注射钙通道阻滞剂、硝酸酯类、硝普钠、替罗非班等药物;或使用血栓抽吸(Ⅱa,C-EO)并置入IABP以稳定血流动力学。经微导管在冠状动脉内靶病变以远局部给药效果更好;将微导管前送至冠状动脉末梢负压抽吸微栓子更有效(Ⅱa,C-EO)。冠状动脉气栓一旦发现,需紧急处理:从引导导管抽取动脉血8~10ml(避免从Y阀再抽入气体)快速推入冠状动脉内,连续操作10~15次,可有效逐出微血管的气栓(Ⅰ,C-EO);禁止推注对比剂或生理盐水,因有大面积心肌缺血致死风险(Ⅲ-Hm,C-EO)。
(七)PCI围术期抗栓治疗
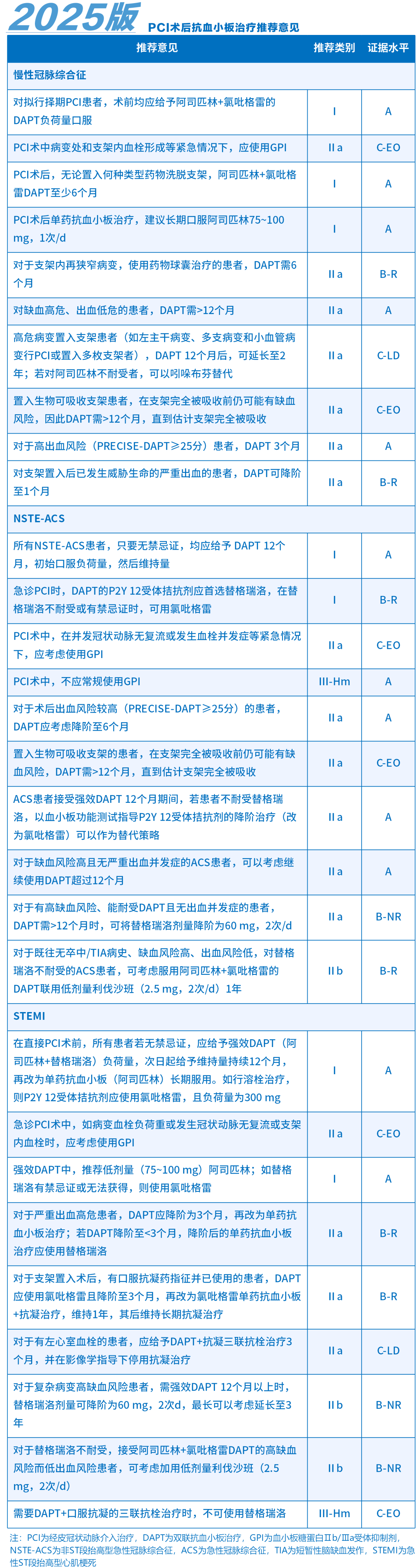
抗血小板治疗:
2016年版:详细介绍不同类型冠心病患者(如SCAD、NSTE-ACS、STEMI)在PCI术前、术中、术后的抗血小板治疗方案,包括药物选择、剂量、疗程等,提及替格瑞洛在中国人群中的良好疗效及安全性,以及高出血风险患者的处理建议。
2025年版:在延续上述要点的同时,根据新的循证医学证据和临床实践,对DAPT方案、维持时间和降阶治疗进行更新和细化。例如,对不同类型的冠心病患者(如慢性冠脉综合征、NSTE-ACS、STEMI)的DAPT药物选择、负荷剂量和维持剂量重新明确,强调根据患者的具体情况(如缺血和出血风险)个体化调整DAPT时长,对高出血风险患者提出更具体的降阶治疗策略,如缩短DAPT时间、降阶为单药抗血小板治疗等,并对特殊人群(如高龄患者、合并糖尿病、CKD、氯吡格雷抵抗等)的抗血小板治疗提供更具针对性的建议。
抗凝治疗:
2016年版:对比不同抗凝药物(如普通肝素、比伐芦定等)在PCI术中的应用,分析其优缺点,并根据临床研究结果提出相应的使用建议,如对欧美指南中比伐芦定与肝素的争议进行阐述,同时介绍中国BRIGHT研究的发现及其对临床实践的指导意义。
2025年版:继续深入探讨抗凝治疗在PCI围术期的应用,结合新的研究成果进一步明确不同抗凝药物的适用场景和优势。例如,对高危NSTEMI患者使用依诺肝素的方案进行细化,强调比伐芦定在高出血风险患者PCI术中的优先选择地位,并更新其在不同临床情境下的具体用法和剂量,同时对PCI术后抗凝治疗的必要性和时长进行更精准的指导。
特殊人群的抗栓治疗:
1.高龄(≥75岁)冠心病患者:冠状动脉病变往往严重而复杂,呈多支、弥漫和严重钙化伴心功能差者多见,对PCI技术要求高、风险大,缺血和出血风险均高。建议DAPT选择阿司匹林+氯吡格雷,标准疗程为12个月,可根据患者缺血与出血风险缩短或延长。
2.合并糖尿病患者:多支、弥漫、严重和小血管等复杂病变多见,缺血风险高。建议DAPT首选阿司匹林+替格瑞洛,至少12个月;对无严重出血并发症的患者,DAPT可延长至12个月以上(替格瑞洛应降阶减量),最长不应超过3年。
3.合并CKD患者:CKD患者是血栓和出血风险均高危的人群,DAPT首选阿司匹林+替格瑞洛,后者受肾功能影响小。PIANO-3ESRD研究显示,接受血液透析的患者,替格瑞洛抗血小板作用较氯吡格雷更强,能够减少不良心血管事件的发生,且不增加出血风险。但对CKD 5期(eGFR<15 ml·min -1·1.73 m -2)患者,尚无证据。
4.冠状动脉复杂病变患者:对大隐静脉桥血管病变尤其是退行性桥堵塞病变的PCI,冠状动脉慢血流甚至无复流并发症的发生率高达近50%,这是由血栓和(或)斑块碎屑栓塞所致,需常规使用滤网导丝保护装置,能有效预防(Ⅰ,C-EO)。与冠状动脉其他复杂病变如多支血管、弥漫性、左主干和分叉等病变一样,DAPT建议首选替格瑞洛。
5.氯吡格雷抵抗患者:即CYP2C19慢代谢型或血小板功能检测提示有残余高反应患者,应选替格瑞洛(Ⅰ,C-EO)。
6.接受非心脏外科手术患者:主要是外科手术出血和冠状动脉血栓风险的冲突。对需尽早行择期外科手术如肿瘤且心血管事件低危患者,术前5~7d开始停用DAPT,可给予GPI或低分子肝素“桥接”,术后保证无出血风险时恢复用药。
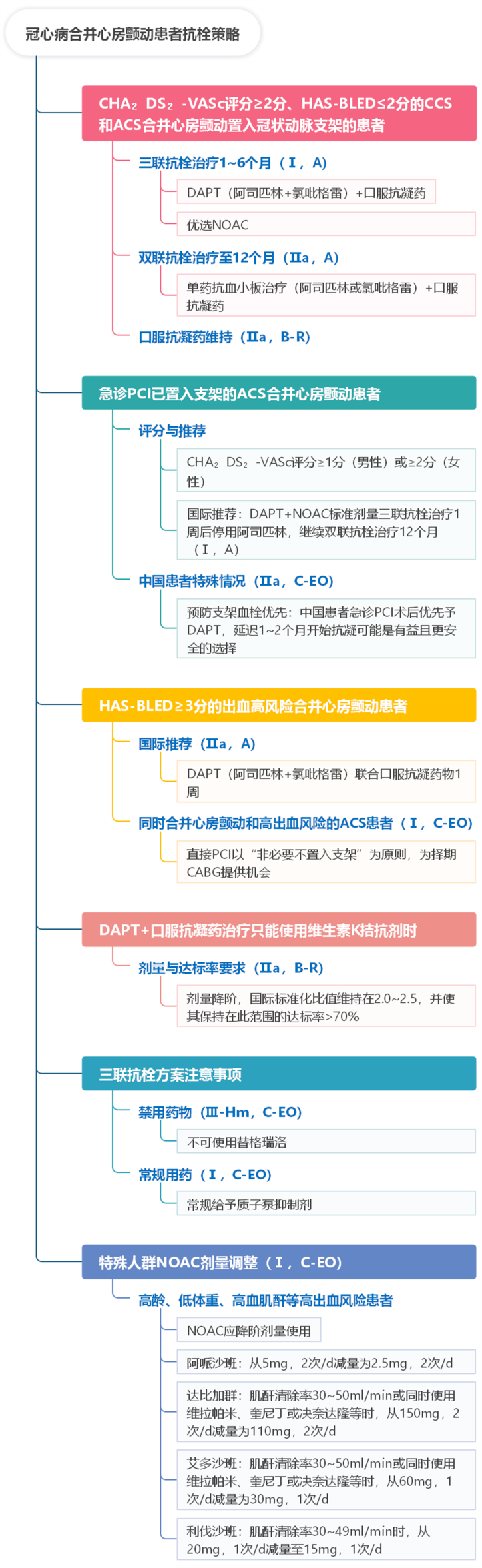
7.合并心房颤动患者:均应根据缺血与出血风险大小,给予个体化治疗方案。
(八)其他围术期药物治疗及术后管理
冠心病合并高血压、糖尿病、心力衰竭等特殊情况的处理:
2016年版:对冠心病合并高血压、糖尿病、心力衰竭等不同情况的药物治疗原则进行概括性说明,如控制血压、血糖、心力衰竭的药物选择和目标值等。
2025年版:对上述特殊情况的处理建议更加详尽和具体,如对冠心病合并高血压患者,详细阐述不同年龄段、不同病情阶段的降压目标值及药物选择顺序;对合并糖尿病患者,强调降糖药物的新选择(如SGLT2抑制剂等)及其心血管保护作用;对合并心力衰竭患者,根据心功能状态和病因等因素,推荐更为精准的药物治疗方案,包括新型药物的应用等。
调脂治疗:
2016年版:推荐对ACS患者无论是否接受PCI治疗,均应及早服用他汀,但指出亚洲与我国的研究结果显示PCI术前使用负荷剂量他汀不优于常规剂量,不建议术前使用负荷剂量他汀,同时强调长期服用他汀类药物使LDL-C<1.8mmol/L,对不同冠心病患者类型的调脂治疗建议。
2025年版:在原有基础上,进一步强调ACS或CCS患者PCI术后常规给予强化降脂治疗并达标维持的重要性,首选他汀类药物,并在必要时联合依折麦布或PCSK9抑制剂,以降低心血管事件残余风险并预防复发,同时对ACS患者的调脂目标值进行更新,指出若2年内再发血管事件,应将LDL-C目标值降至<1.0mmol/L。
康复治疗:
2016年版:简要提及康复治疗包括运动、合理膳食、戒烟、心理调整和药物治疗等方面,对ACS患者PCI后实施心脏康复治疗的推荐,以及对冠心病患者心理状态的关注和调整建议。
2025年版:更全面地阐述心脏康复的内容和重要性,强调其在提高运动耐量、生存质量及减少心血管事件中的作用,具体说明运动康复的实施方式(如合理运动为主)对改善PCI术后患者焦虑抑郁状态的益处,同时细化合理膳食、戒烟限酒、体重管理等方面的要求,并强调对患者心理状态的科学评估和针对性干预,包括药物治疗和宣传教育等措施。
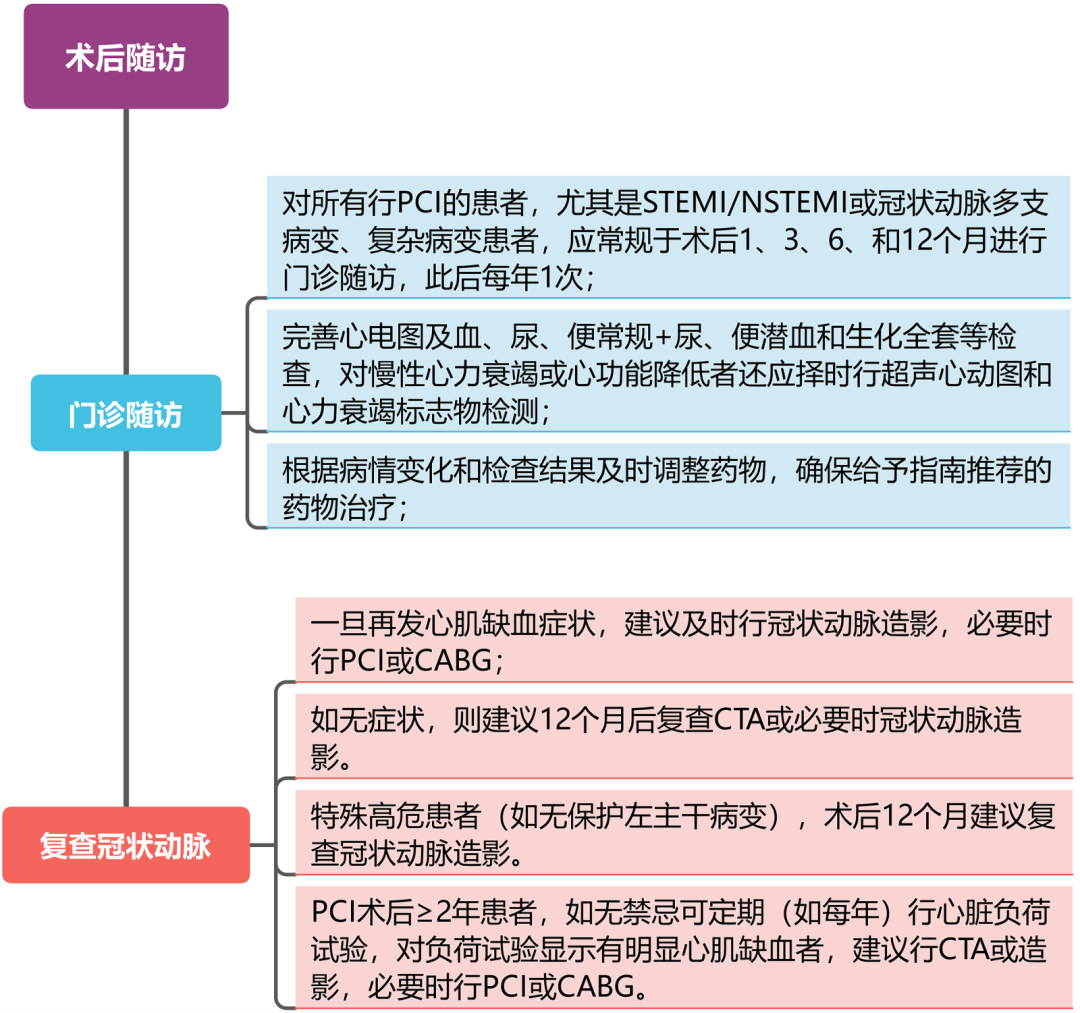
术后随访:
2016年版:建议PCI术后患者定期复查,对特定患者(如从事危险行业、需参与高耗氧量娱乐活动等)早期复查冠状动脉造影或CT血管成像,以及PCI术后>2年患者的常规负荷试验和必要时的进一步检查。
2025年版:进一步明确术后随访的时间节点(术后1、3、6和12个月,此后每年1次)、检查项目(心电图、血尿便常规、生化全套等),以及对不同病情患者的随访重点和处理措施,如对慢性心力衰竭或心功能降低患者的超声心动图和心力衰竭标志物检测,对无症状患者的冠状动脉CT血管成像或造影建议,以及对特殊高危患者(如无保护左主干病变)术后12个月复查冠状动脉造影的要求等。
2025年版《经皮冠状动脉介入治疗指南》在多个方面进行了更新和完善,为临床医生提供了更科学、更精准、更个性化的治疗指导。在临床实践中,应严格遵循指南推荐,结合患者的具体情况,制定最佳的治疗方案,以提高PCI的治疗效果,改善患者的预后。