

ROSS手术是治疗年轻患者(特别是小儿患者)主动脉瓣严重病变的重要手术治疗方式,自体肺动脉瓣移植能够解决早期主动脉瓣病变处理的难点,但ROSS术后远期肺动脉带瓣管道衰败相关的主肺动脉及肺动脉瓣膜病变发生率非常高,多数需要再次手术处理。以往外科再次手术是主要的治疗方式,但此类患者再次开胸体外循环手术创伤大、风险高、预后差,因此,愿意再次接受外科手术的患者并不多。经皮肺动脉瓣置换(TPVR)手术是针对右心系统术后肺动脉瓣反流的创新治疗方式,该手术不必开胸、创伤小、恢复快,虽然临床病例不多,但它已在治疗肺动脉瓣反流,特别是法乐四联症等先心病术后患者的相关问题方面,被临床专家和患者广泛接受。临床中用于该手术的介入瓣膜主要分为两类,一种是自膨式长支架肺动脉瓣,例如美敦力Harmony、启明Venus-P,另一种是球扩式的短支架瓣膜,如美敦力Melody、爱德华Sapien系列等。
ROSS术后肺动脉瓣关闭不全能够通过TPVR手术获得较好的治疗效果,但ROSS手术后肺动脉带瓣管道衰败的形态各异,部分患者除了肺动脉瓣膜衰败反流,还常见肺动脉主干严重狭窄,特别是长段肺动脉主干狭窄,应用常规自膨式支架肺动脉瓣,术后可能出现严重的支架膨胀不良,应用短支架球扩瓣膜则很难有效解决长段的肺动脉主干狭窄问题,对于此类患者临床处理比较棘手。本期故事会为大家分享一例ROSS术后主肺动脉狭窄合并肺动脉瓣大量反流患者应用CP覆膜支架+S3球扩瓣膜重建肺动脉主干和肺动脉瓣膜的病例,期待大家共同讨论。
患者基础信息
王某某,男,60岁,主诉:间歇性胸闷、气短17年,加重1年。Ross+室间隔缺损修补术后20+年。
术前超声评估
室间隔连续完整;卵圆孔未闭,房水平双向分流;主动脉瓣上血流速度略加快;肺动脉内可见往返血流信号,血流速度加快Vmax357cm/s,PGmax51mmHg,肺动脉瓣反流(17ml);二尖瓣反流(4.0ml);三尖瓣反流(49ml);主动脉:瓣环28mm,窦部40mm,升主动脉50mm,肺动脉主干内径8mm,长度约31mm。EDV 85ml,ESV 38ml,EF 55%,FS 29%,SV 47ml。
术前诊断
ROSS术后,主肺动脉狭窄,肺动脉瓣关闭不全;二尖瓣关闭不全;三尖瓣关闭不全;升主动脉瘤样扩张;心功能IV级(NYHA分级)
术前CT评估
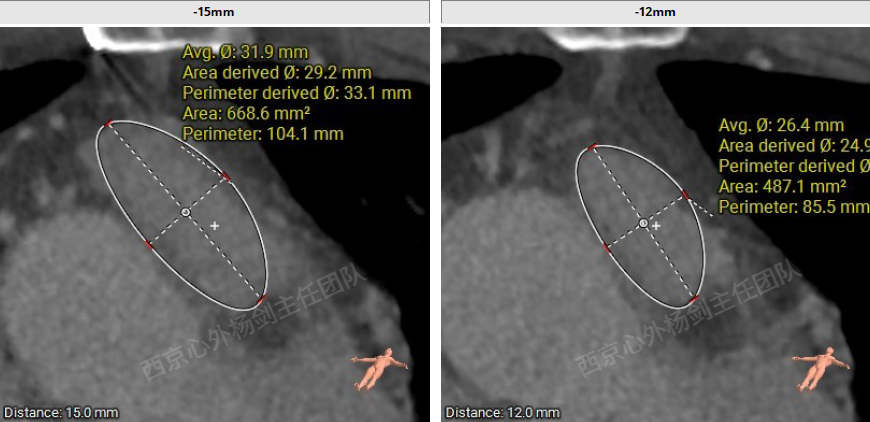
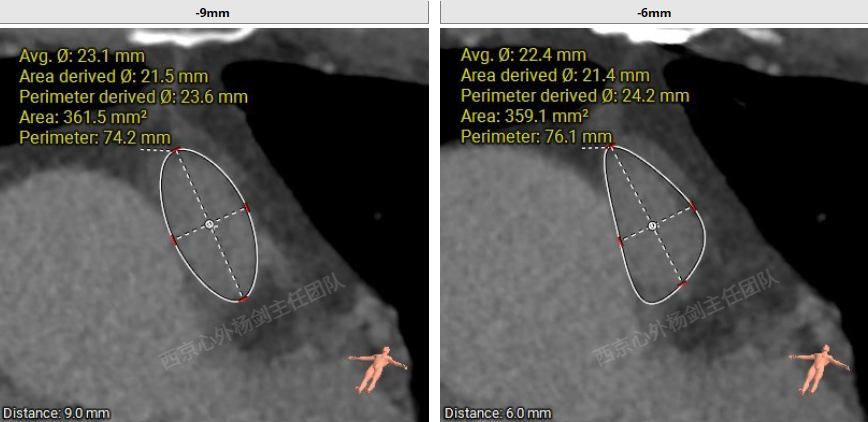
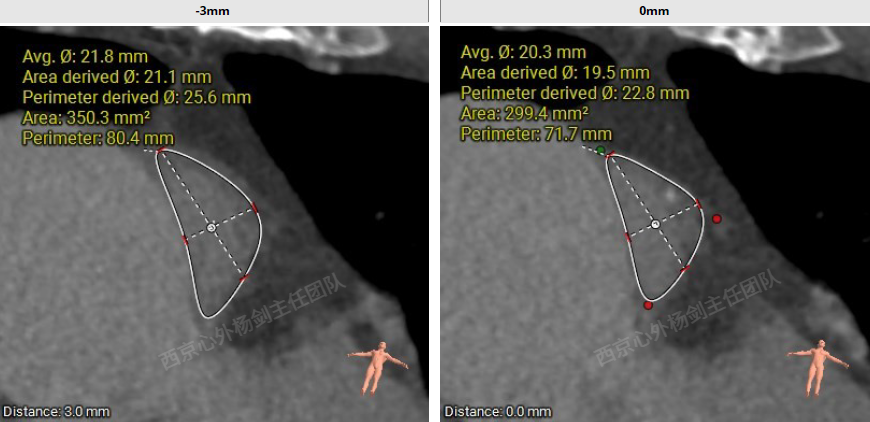
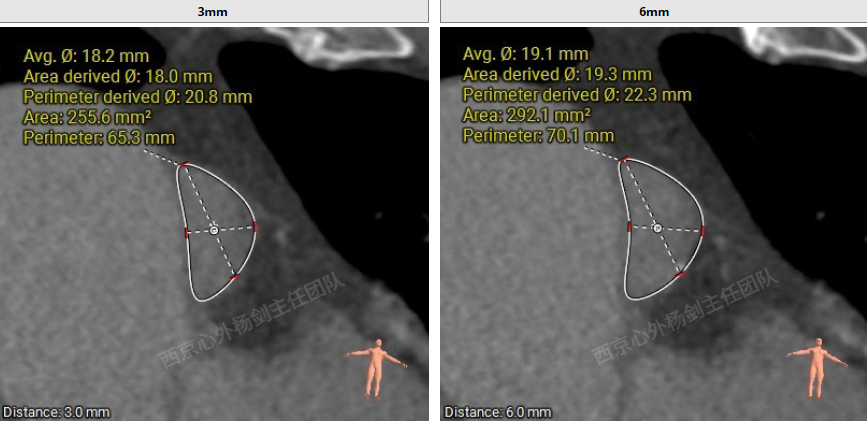
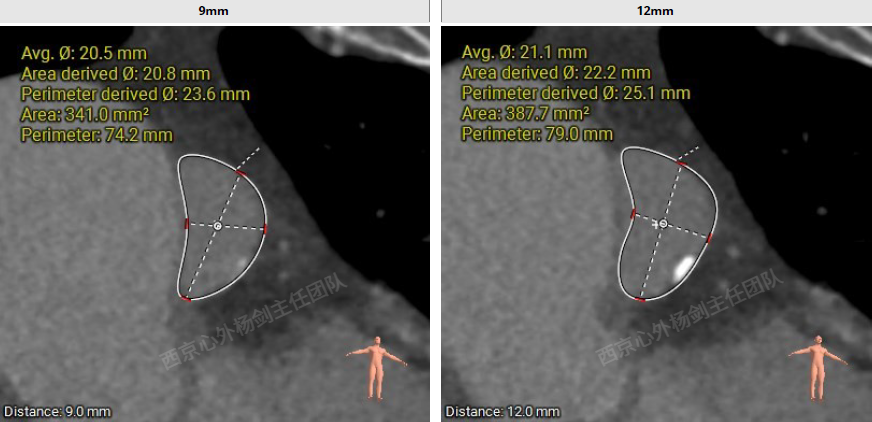
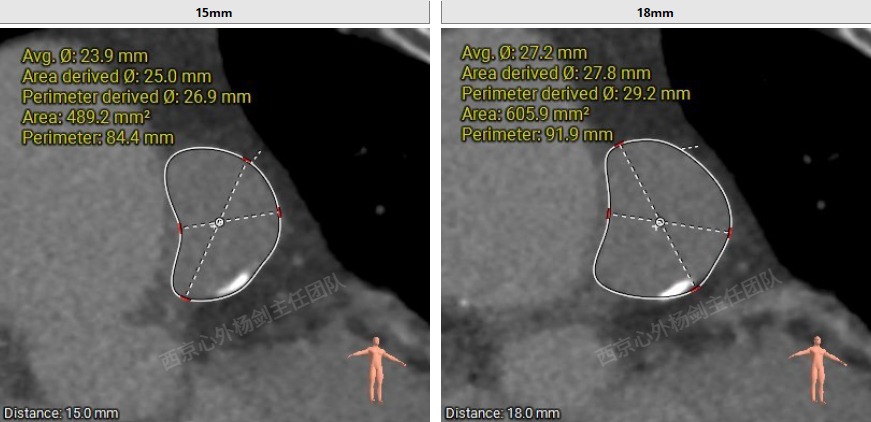
多平面测量显示瓣环平面上方3mm处最窄,面积255.6mm2,面积折算直径约18mm
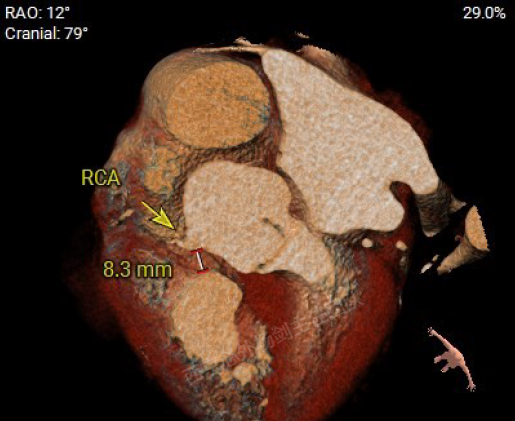
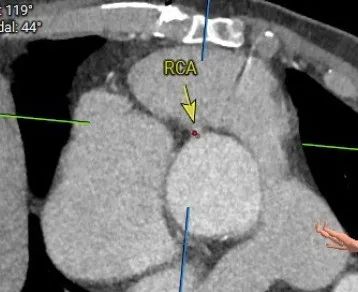
右冠状动脉(RCA)距离右室流出道8.3mm
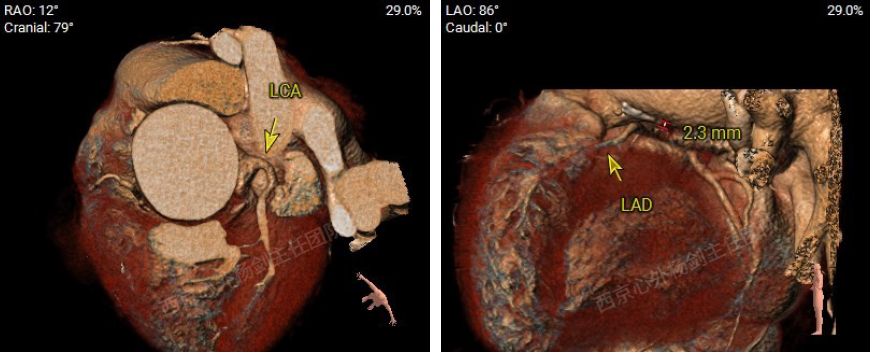
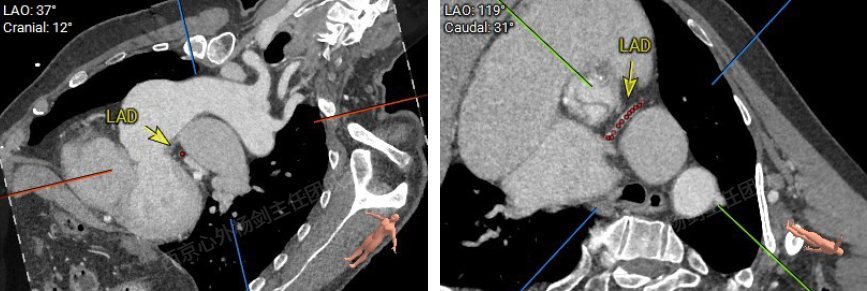
左前降支(LAD)距离肺动脉约2.3mm
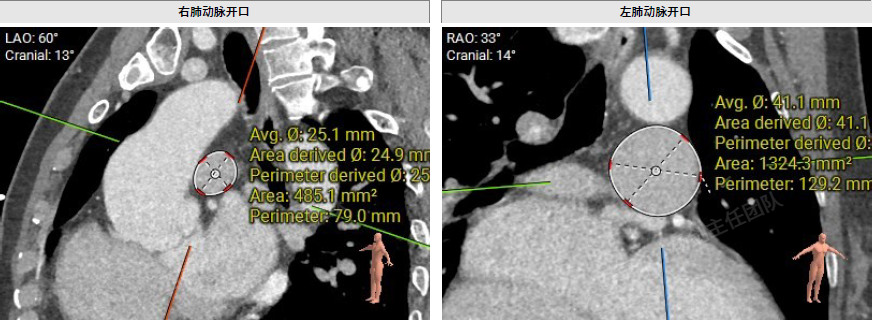
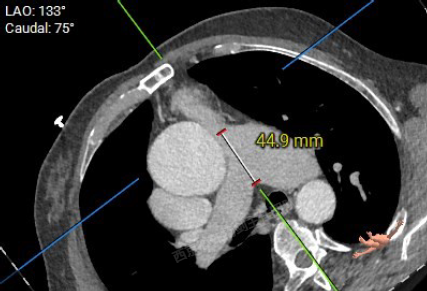

术前3D数字模型
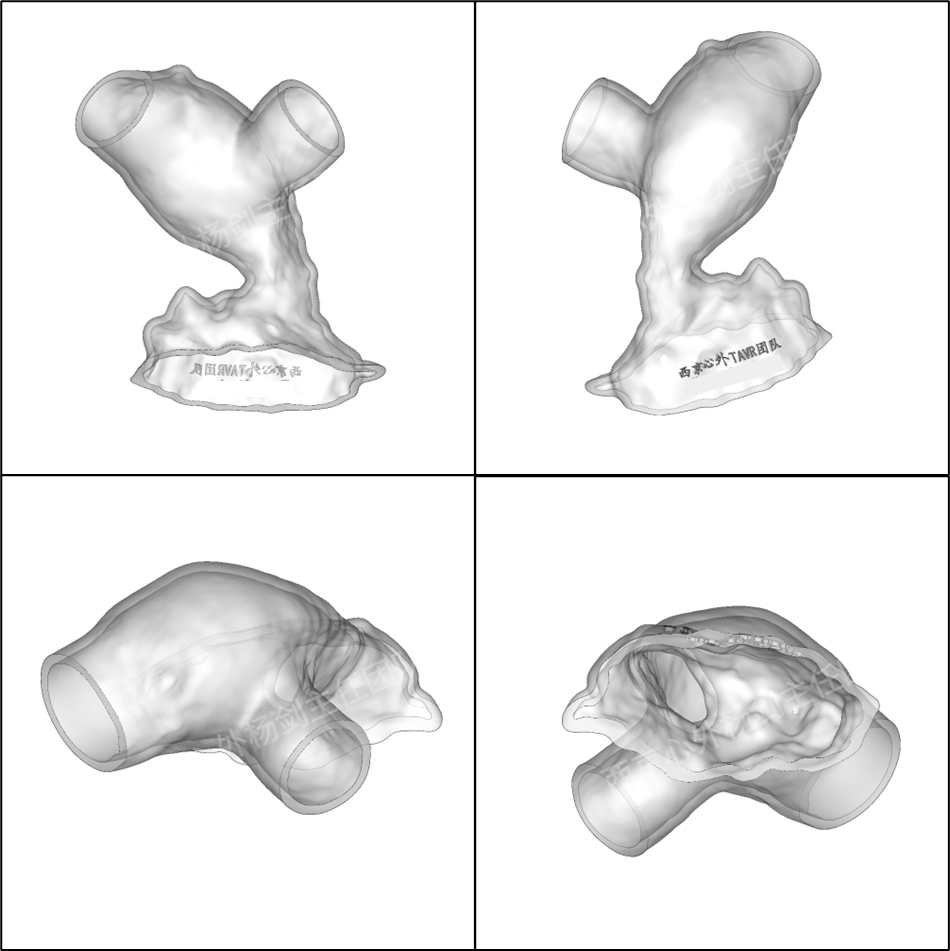
手术策略
CP支架植入术+经导管肺动脉瓣置换术:
肺动脉主干狭窄,形态不规则,近端远端均有扩张,在狭窄肺动脉主干位置预先置入39mmCP支架,并用22mm BIB球囊进行扩张,重建主肺动脉。
CP支架内植入S3瓣膜,考虑到瓣膜选择过大时,可能存在压迫前降支或右冠状动脉的风险,选择23mm Sapien 3 +2cc。
术中操作
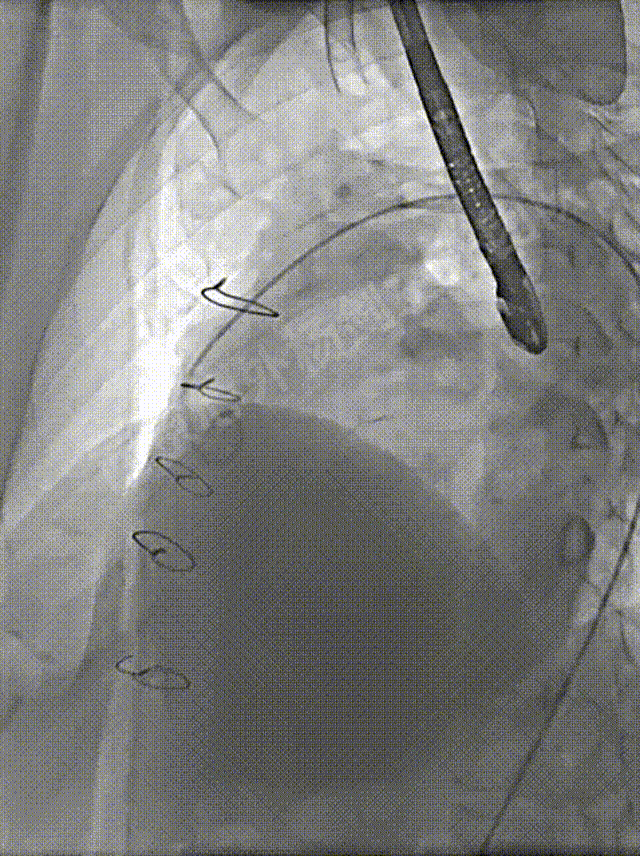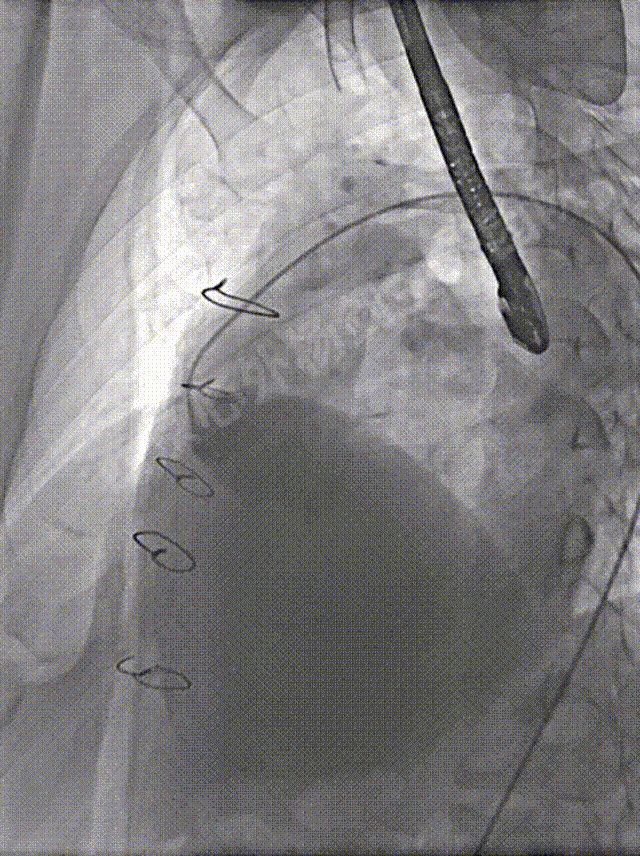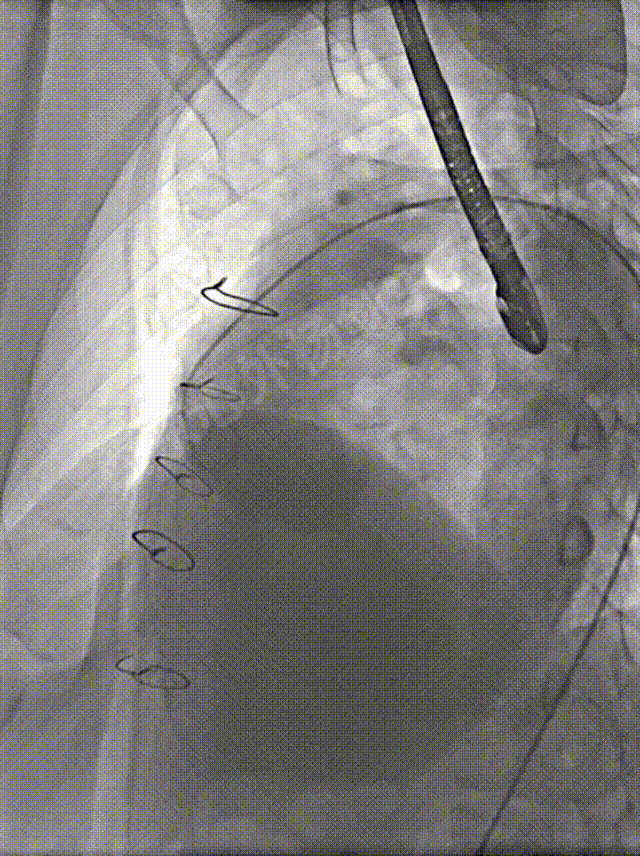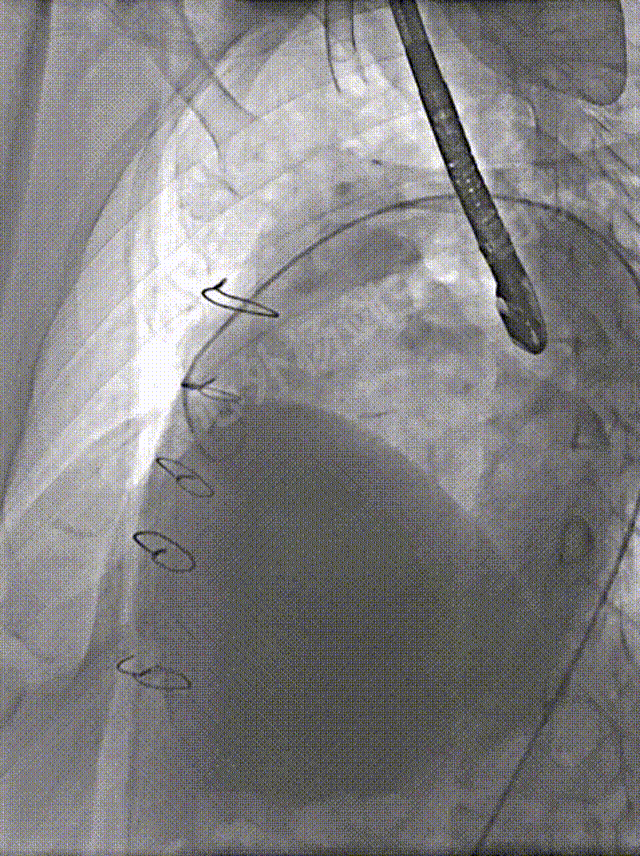
术前造影显示左冠、前降支显影正常
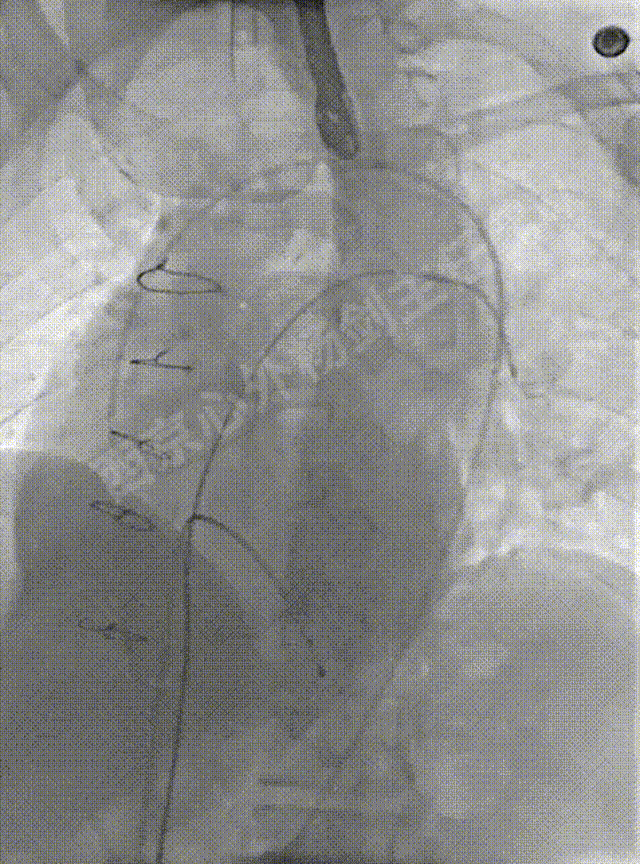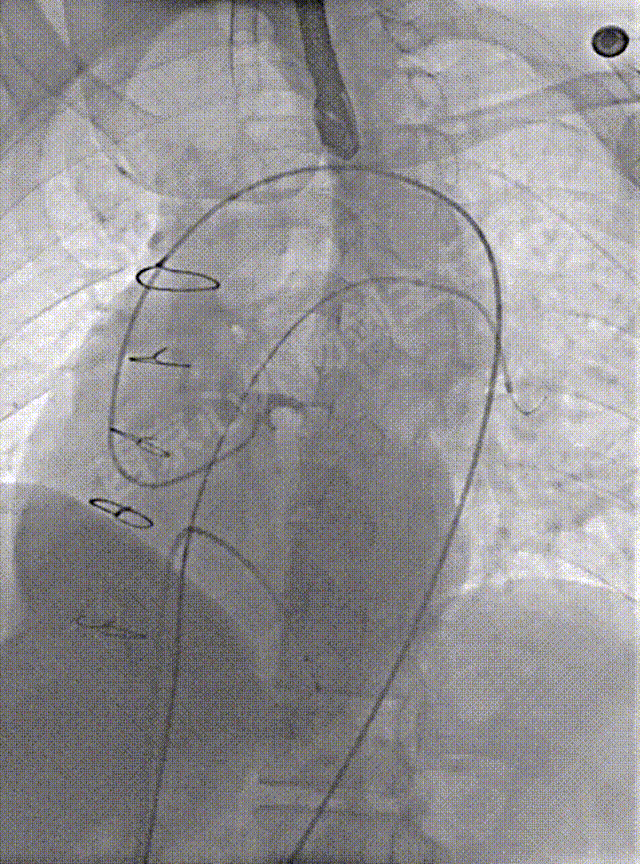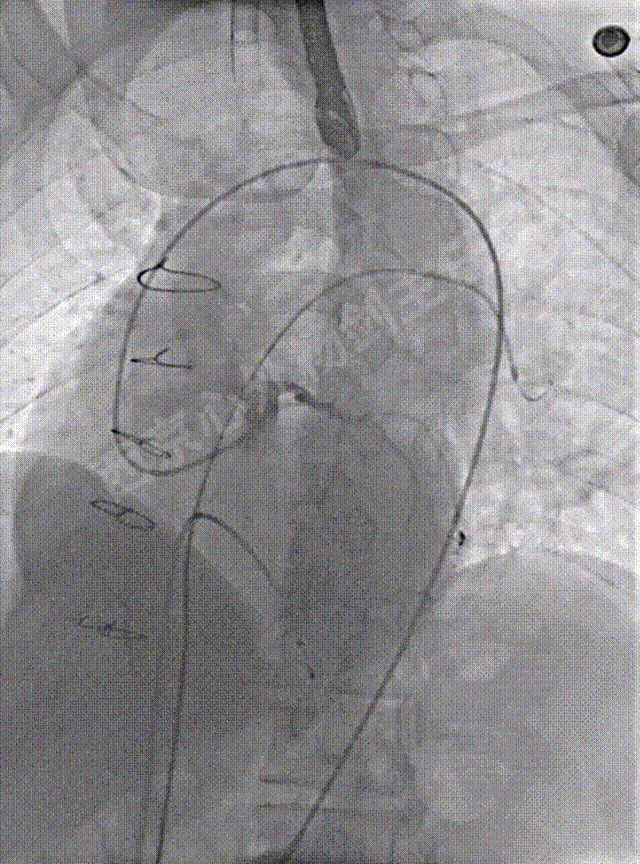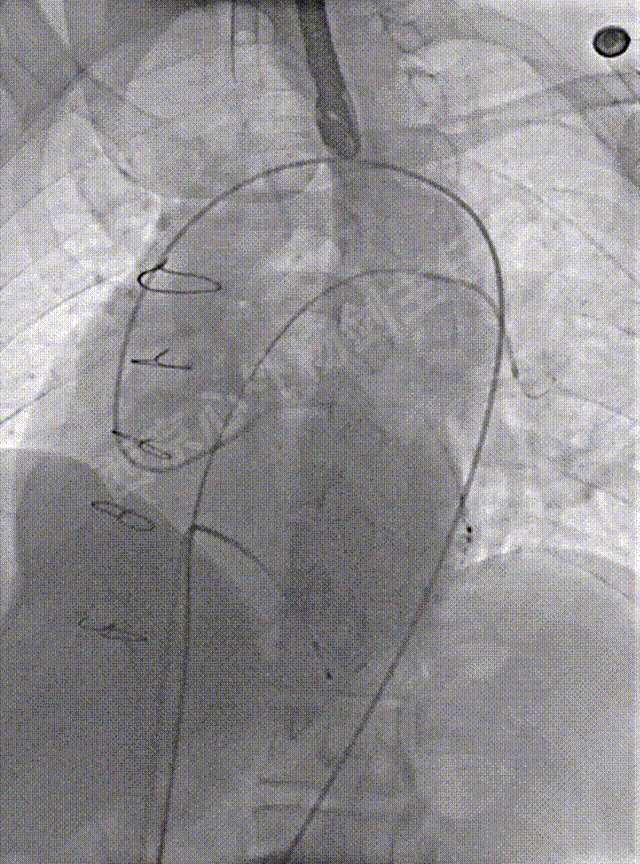
左冠脉造影确定位置,经右侧股静脉建立至左肺动脉远端轨道,左侧股静脉预置右心室临时起搏备用。心导管检查,测量左心房压力69/22mmHg, 肺动脉压42/24mmHg
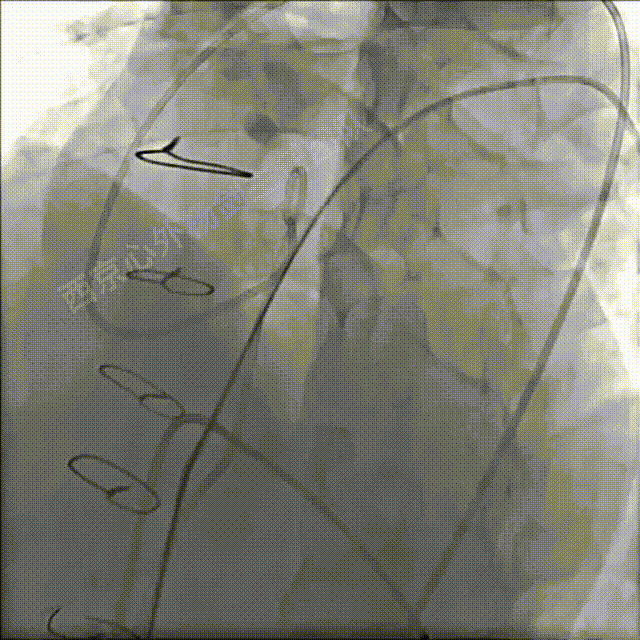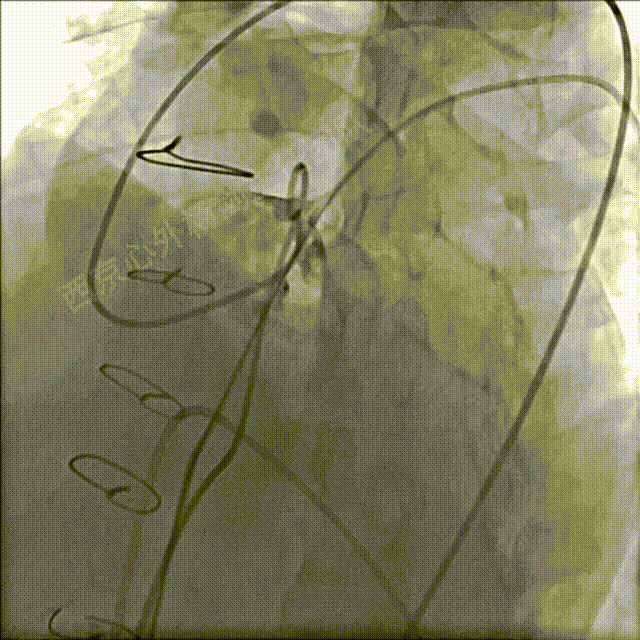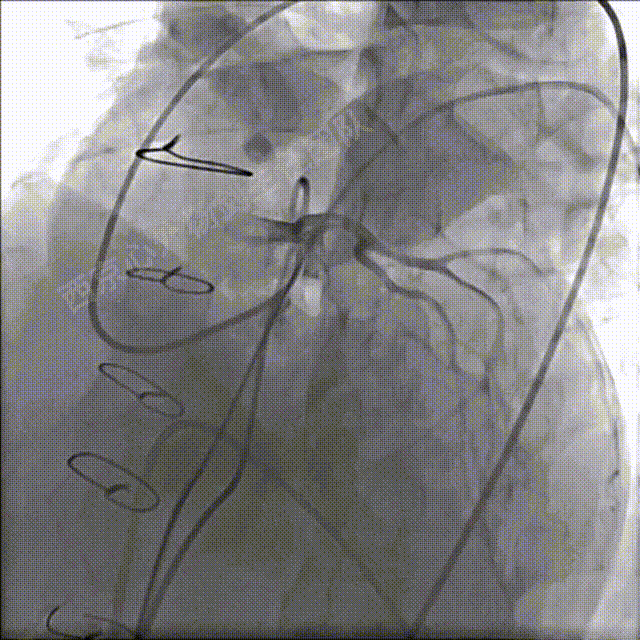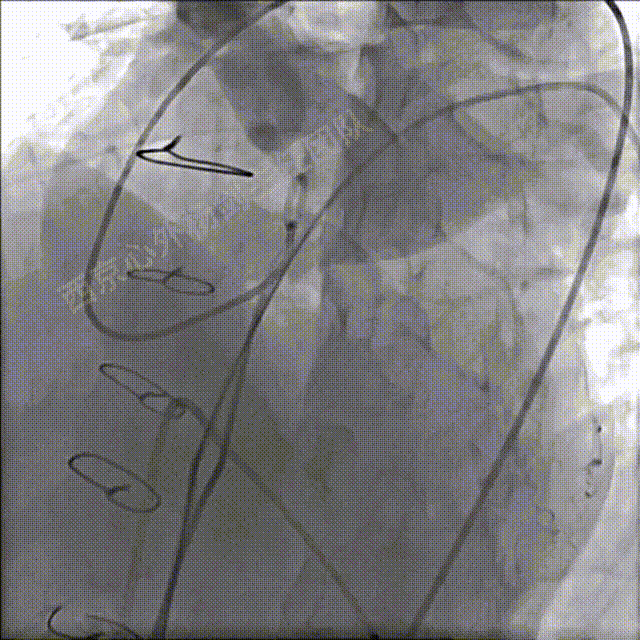
肺动脉主干及左冠脉处同时造影确定相对位置
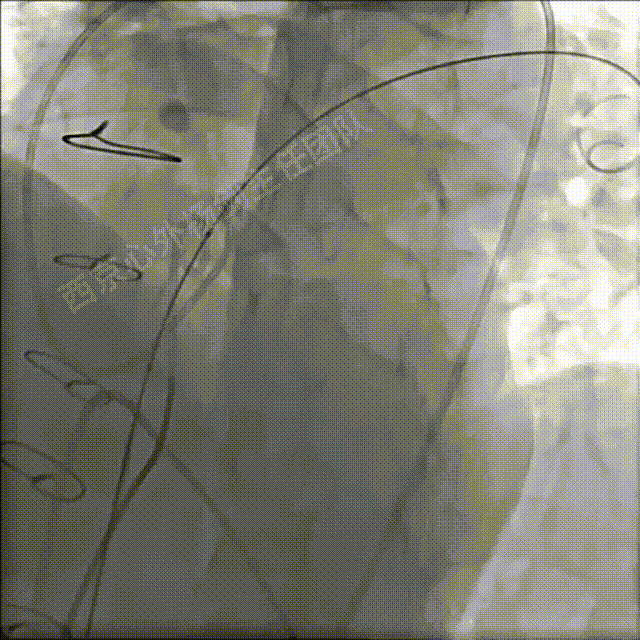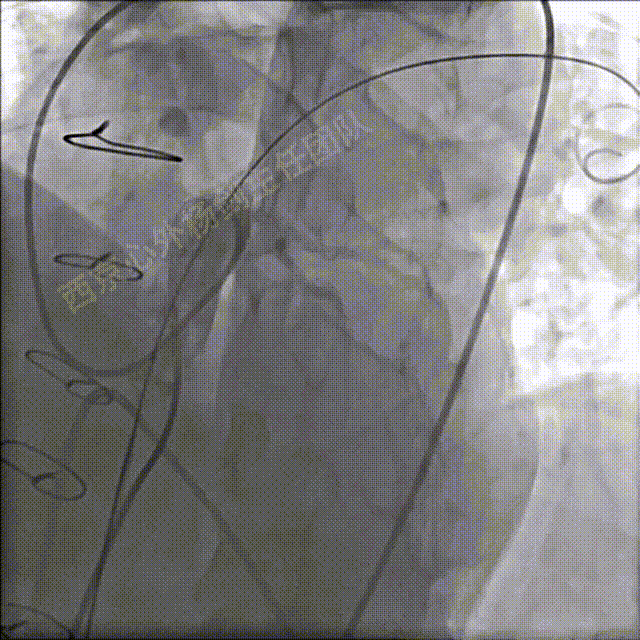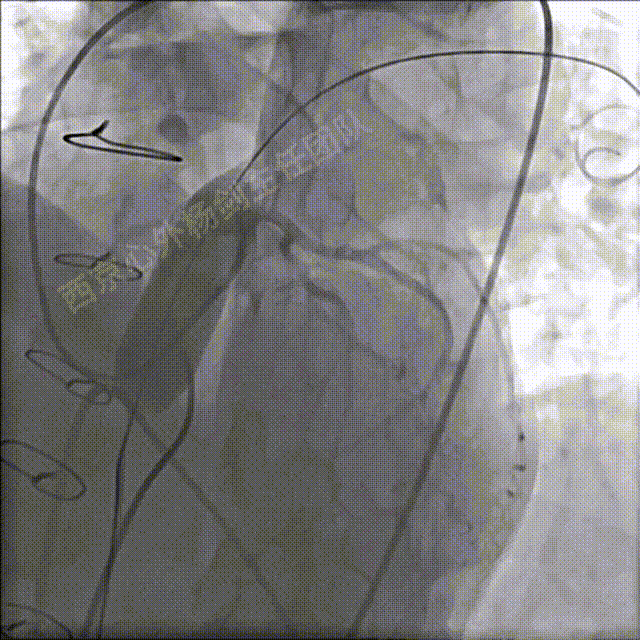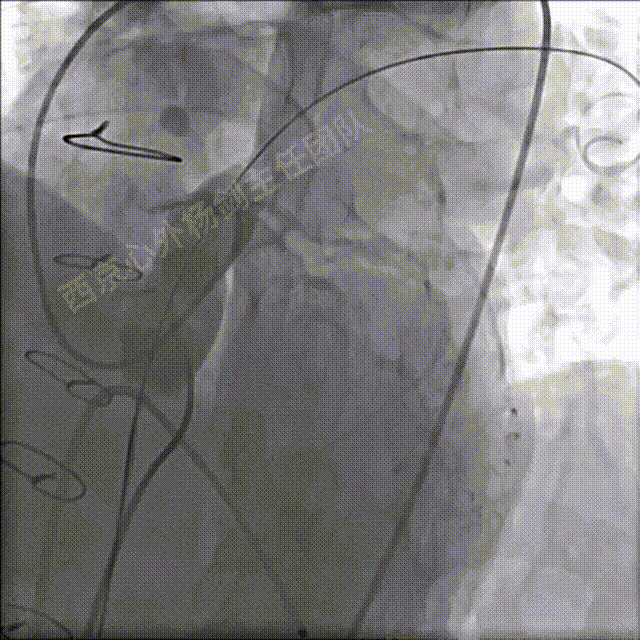
送入22mm球囊扩张测试是否压迫冠脉,DSA显示冠脉显影正常,无压迫
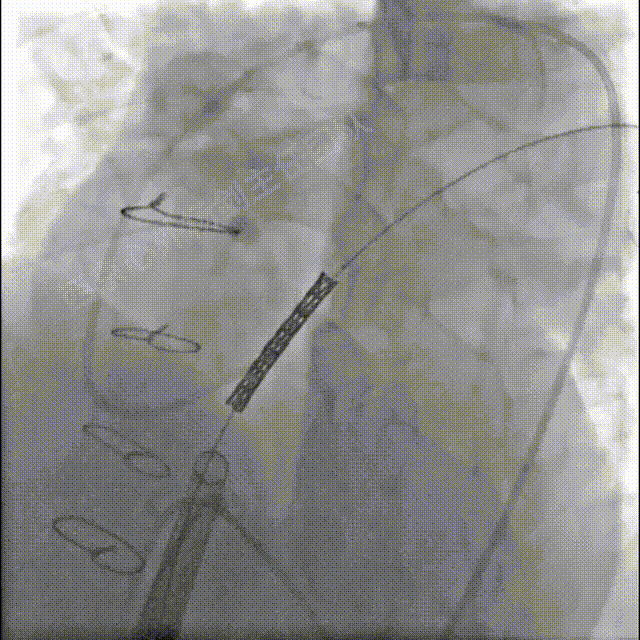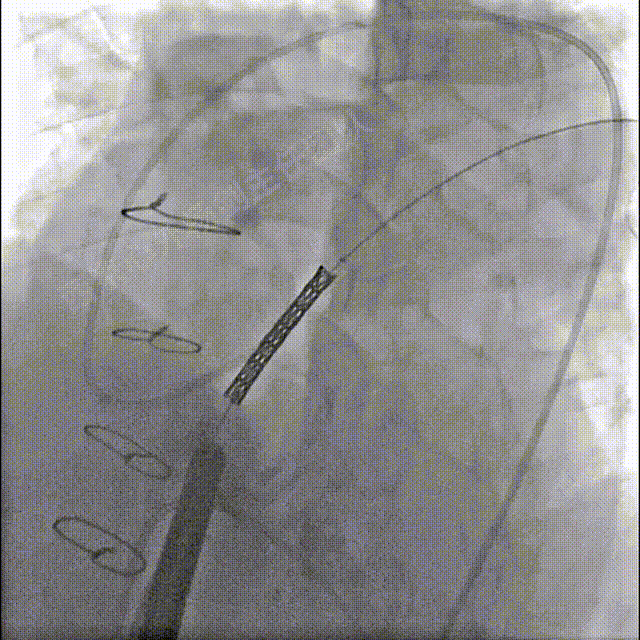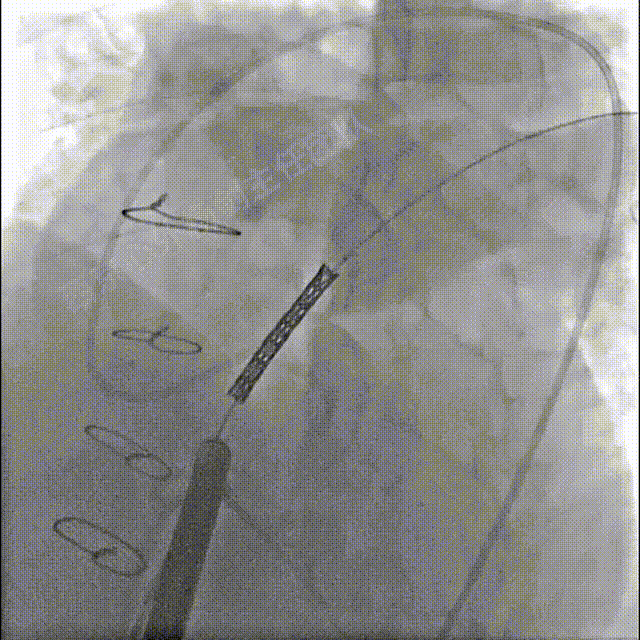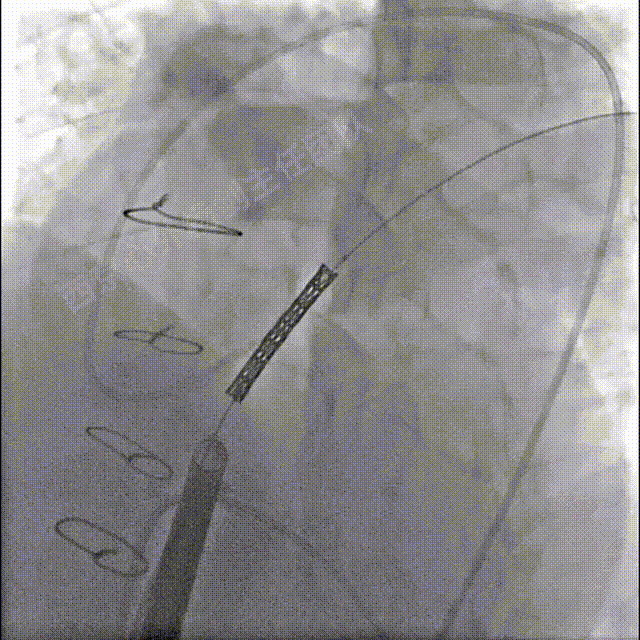
送入装载22mmBIB球囊及39mmCP支架系统至狭窄的肺动脉主干,造影并调整支架初始位置
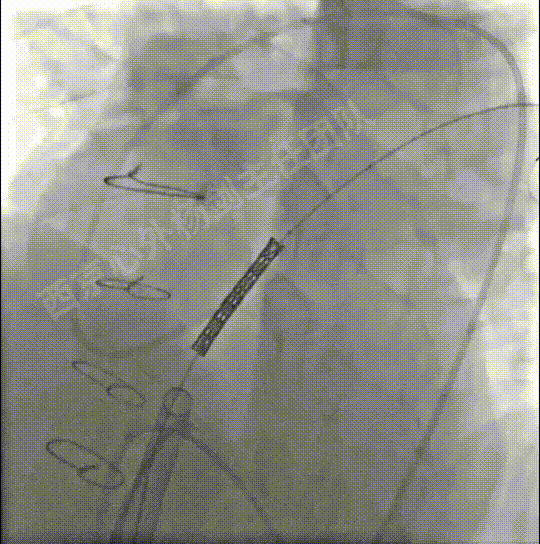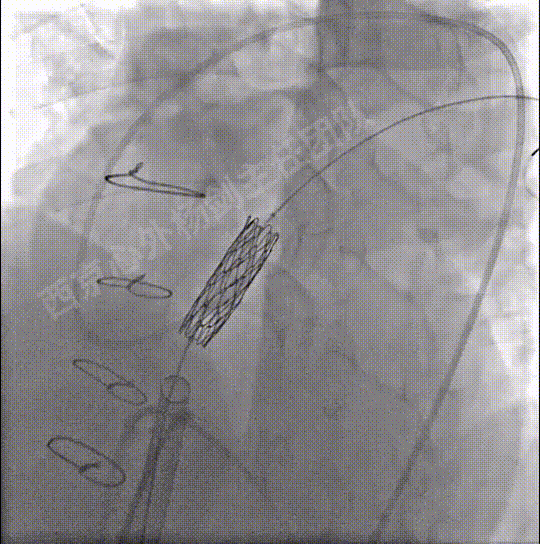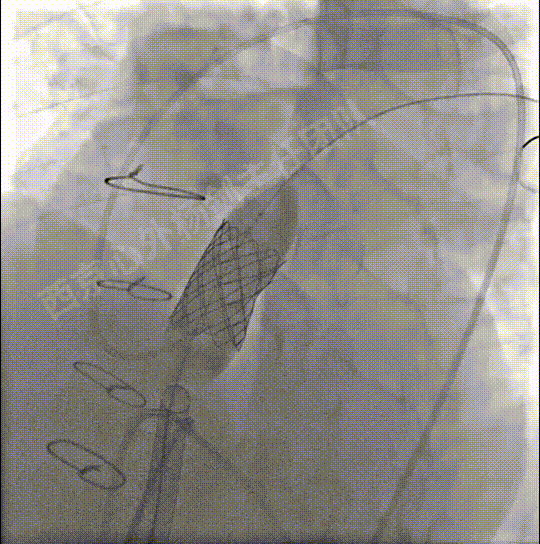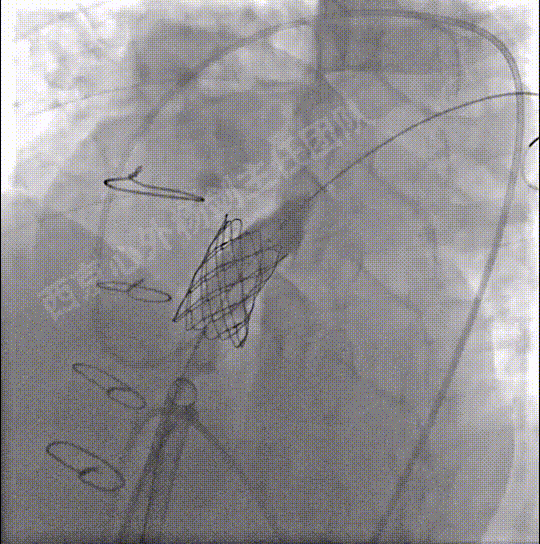
扩张释放CP支架重建肺动脉主干
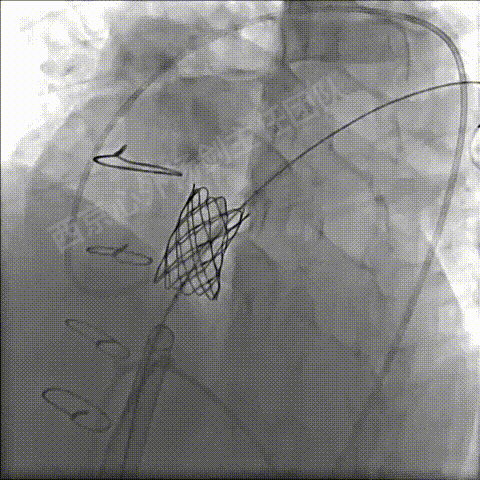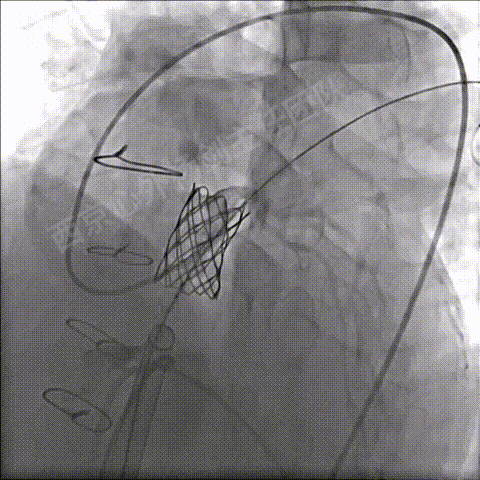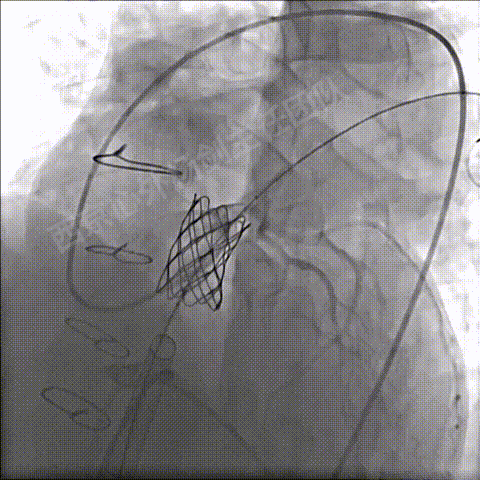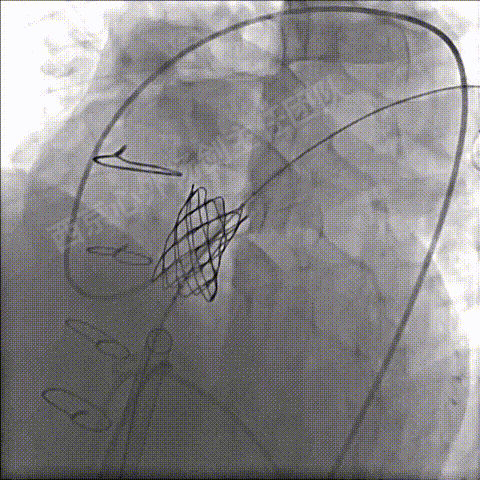 左冠造影确定CP支架顶端未压迫左冠状动脉
左冠造影确定CP支架顶端未压迫左冠状动脉
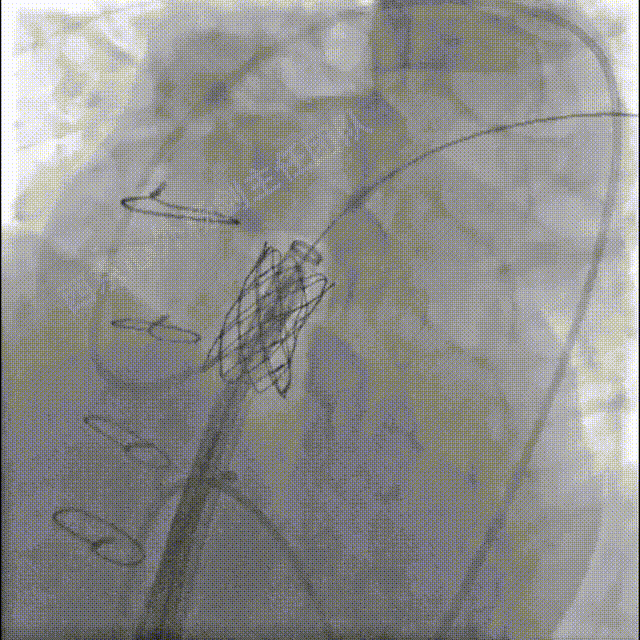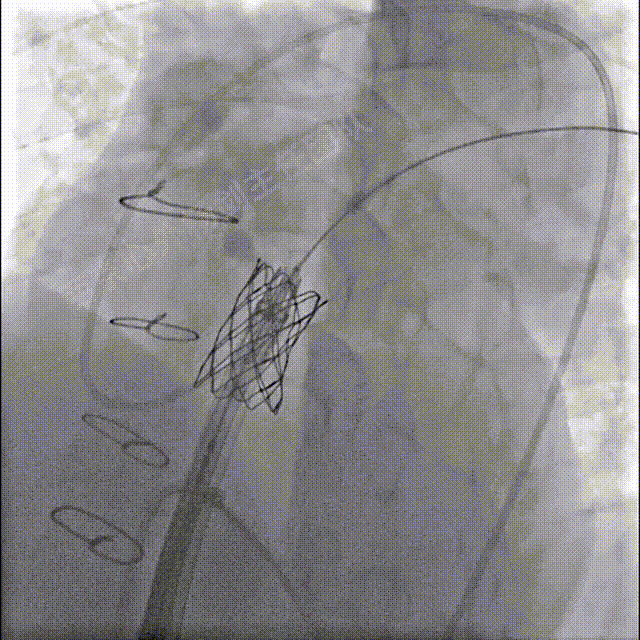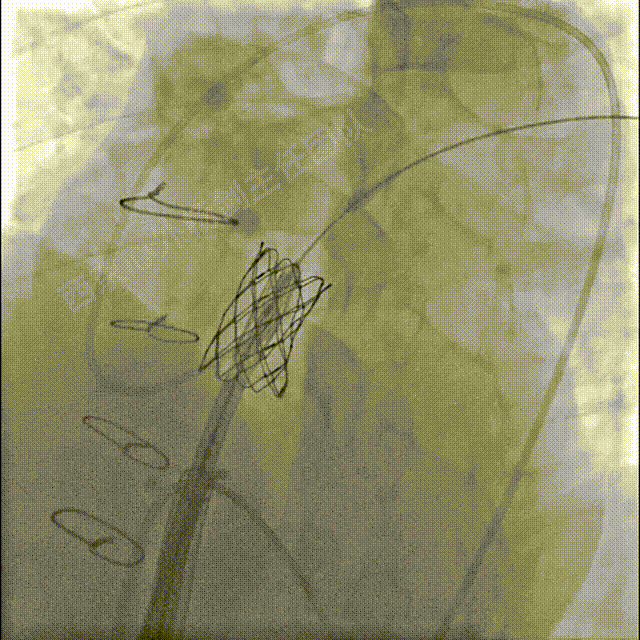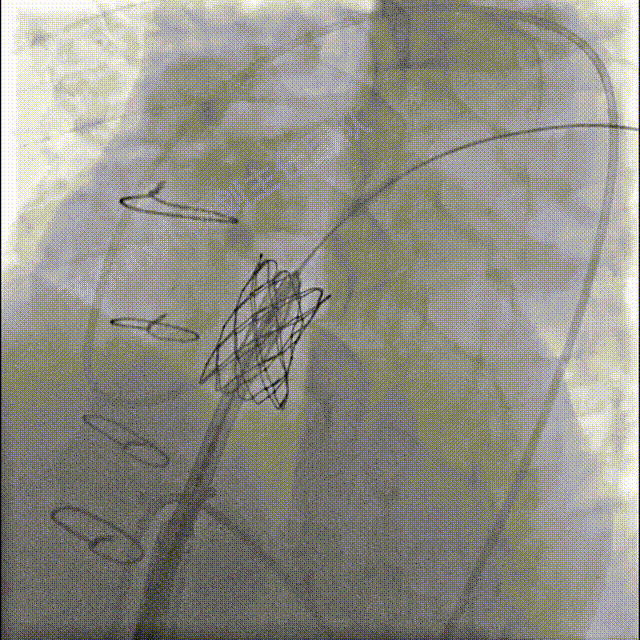
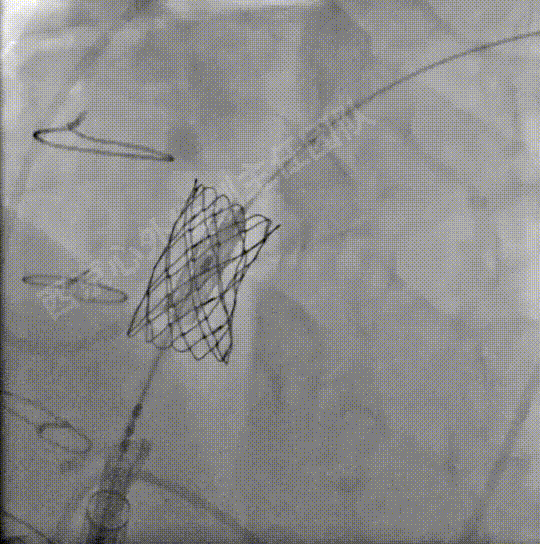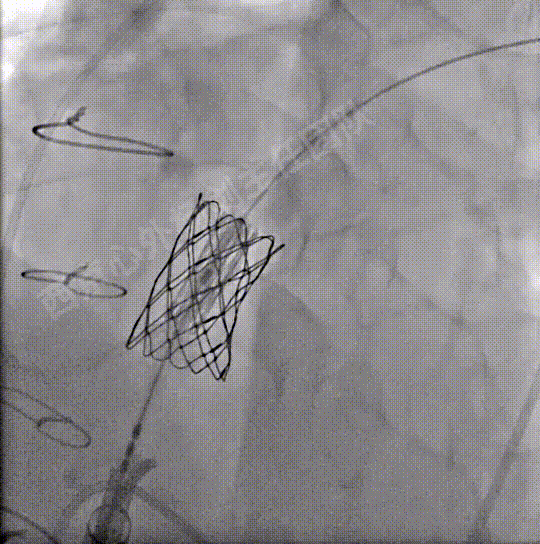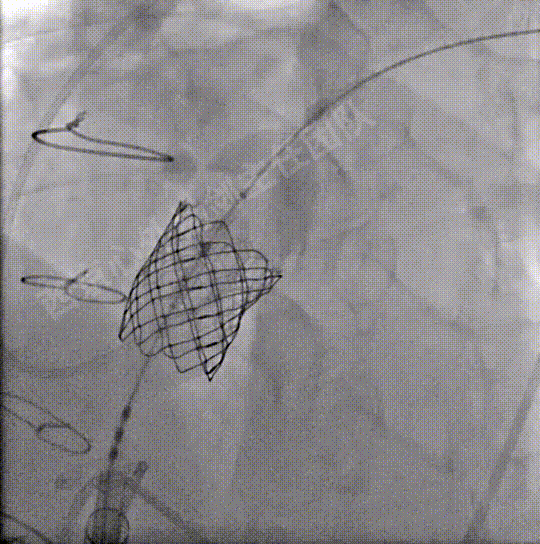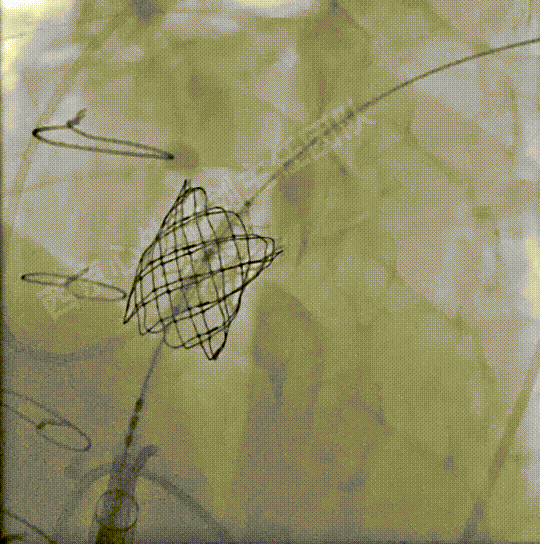
送入S3瓣膜,容量23mm+2cc策略,释放S3瓣膜
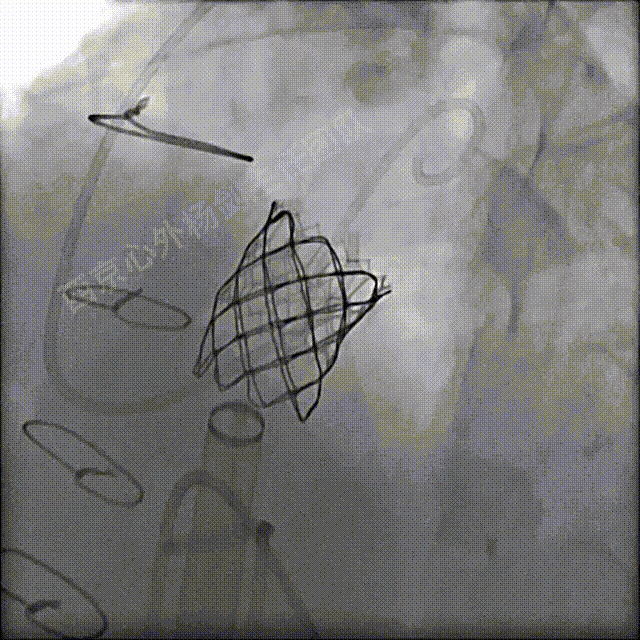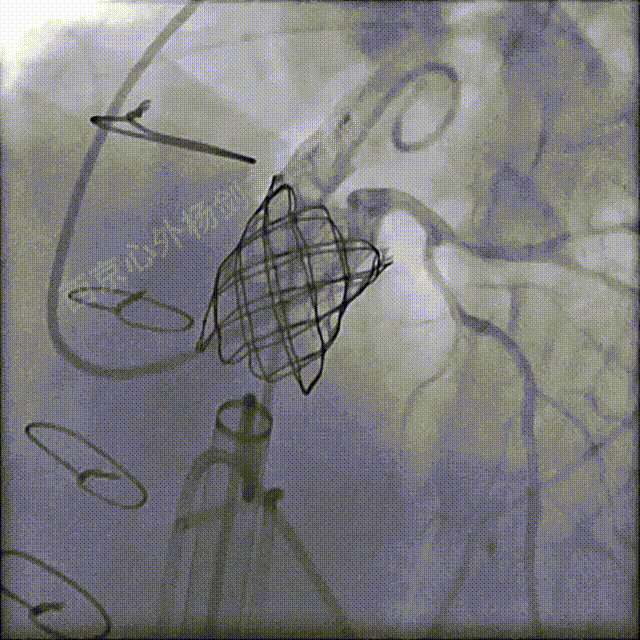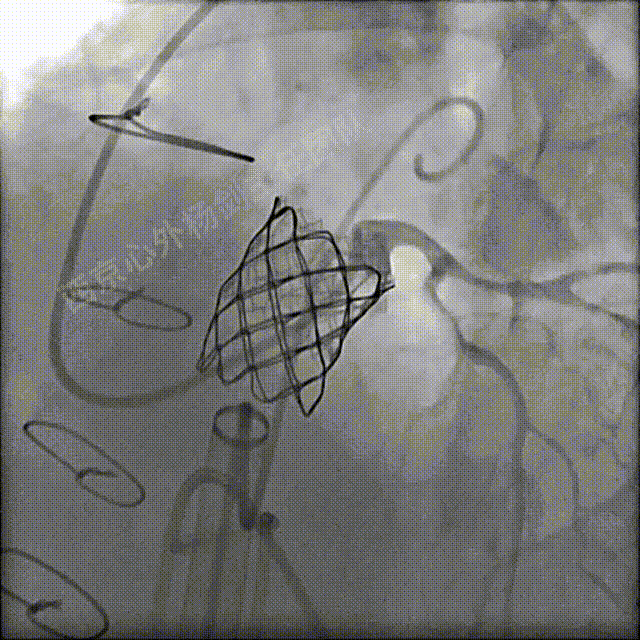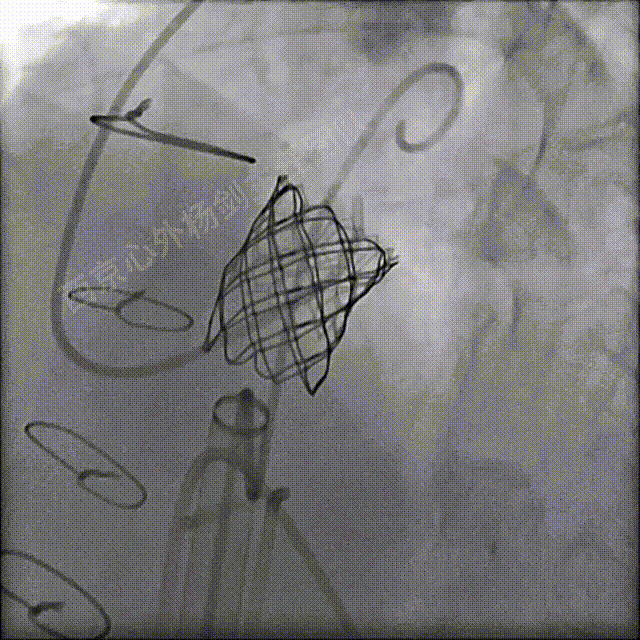
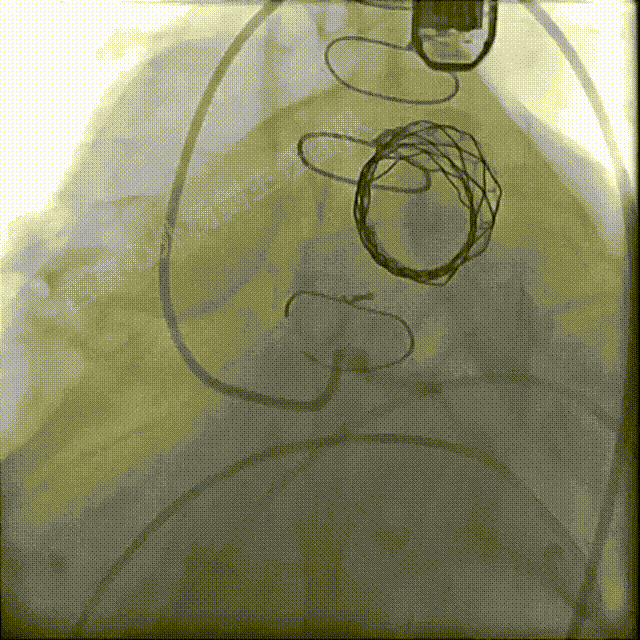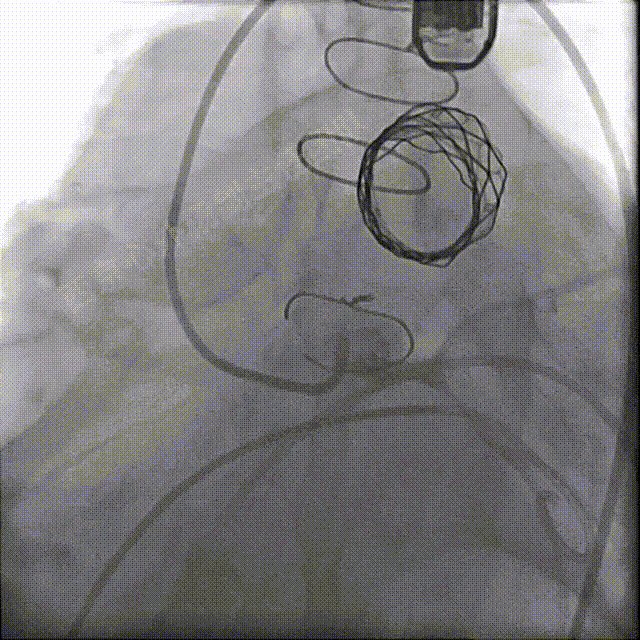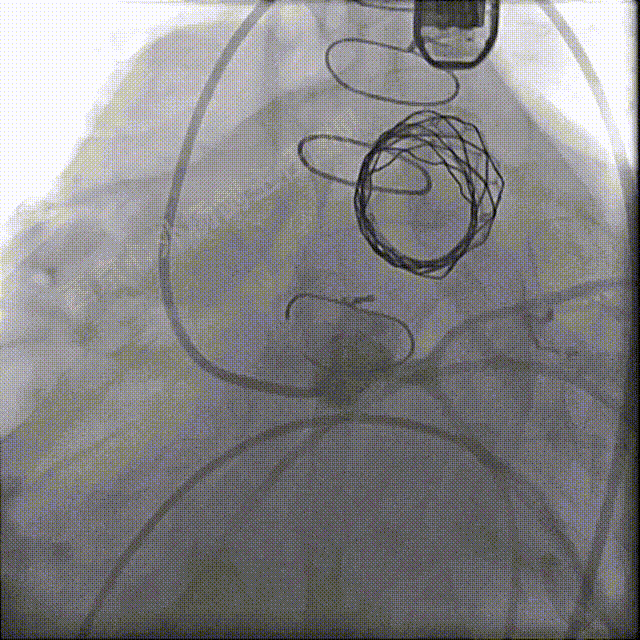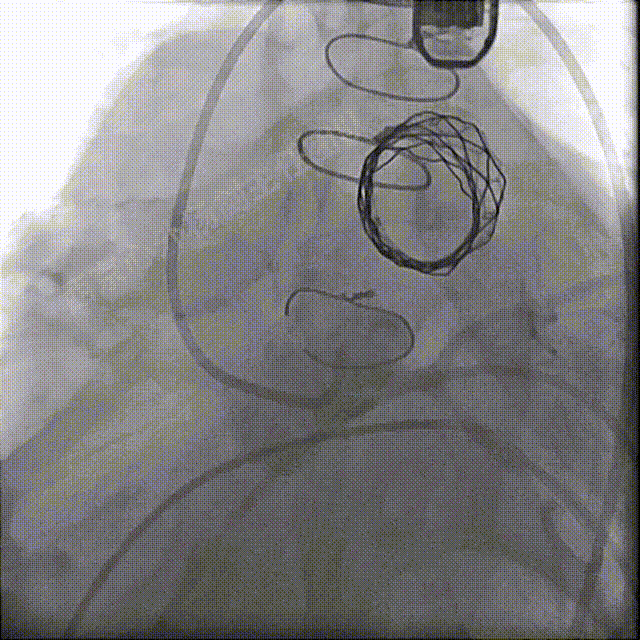
左冠及肺动脉造影显示肺动脉瓣无反流,左冠充盈正常未压迫
术后导管测量肺动脉压43/21mmHg, 右心室压47/27mmHg
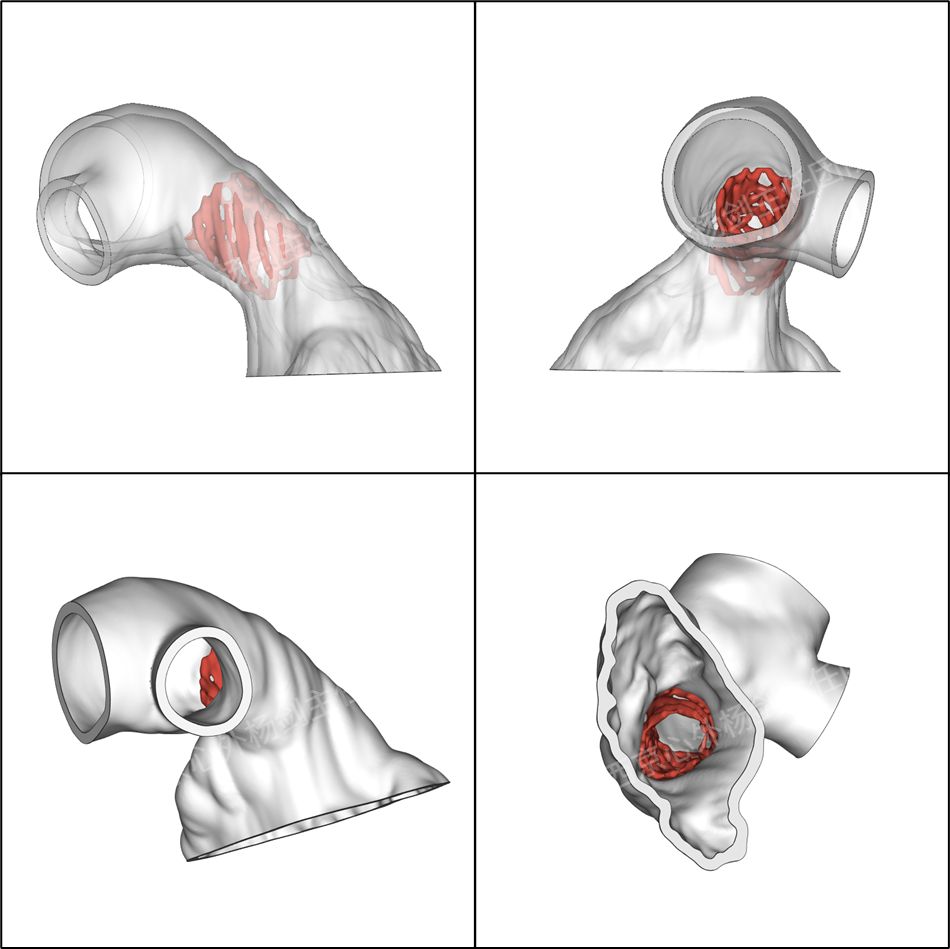
术后3D数字模型
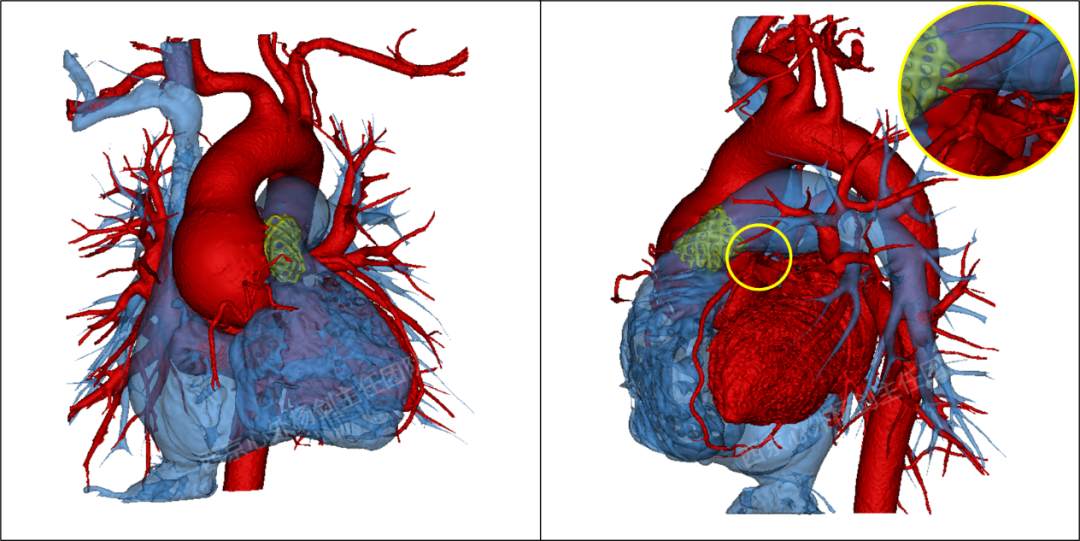
心脏组织3D数字模型(红色组织为左心系统,蓝色半透明组织为右心系统,黄色组织为CP支架及Sapien 3瓣架)
右图黄圈位置显示:CP支架及Sapien 3瓣架术后对前降支无压迫
小结
1.ROSS手术或其他应用带瓣管道行右心流出道重建的手术,术后患者均面临带瓣管道衰败问题,不同于单纯生物瓣衰败,带瓣管道衰败可能合并肺动脉主干扭曲、钙化狭窄。因此,此类患者再次干预需综合考虑右心流出道、肺动脉主干及肺动脉瓣膜重建;
2.经皮肺动脉瓣置换已成为临床上处理术后肺动脉瓣反流的重要手段,较传统外科再次手术创伤小、风险低,临床专家和患者接受度较高。但对于肺动脉主干狭窄患者,选择自膨瓣可能出现支架膨胀不良的情况。本例患者肺动脉主干狭窄,采用CP支架重建主肺动脉,S3球扩瓣CP支架内植入,达到了理想的矫治效果;
3.术前使用患者的3D数字及打印模型,可引导探索介入系统的新型治疗方式,为复杂术后的肺动脉狭窄患者选择合适的介入瓣膜、可视化确定假体最佳着陆位置以及预测并发症等方面发挥重要作用;
4.肺动脉狭窄患者行经导管肺动脉瓣置换术前的影像学评估,需要重点分析主肺动脉形态、右室流出道结构、以及左右冠脉与肺动脉的相对距离等,综合评价确定球扩瓣的植入策略。
参考文献:
⇅ 向上滑动阅览
