
2025年7月4-6日,第十九届中国中西部心血管病学术会议在成都如期召开。在大会第二日的“经导管瓣膜病介入治疗论坛”上,四川大学华西医院陈茂教授作了题为《经导管二、三尖瓣介入治疗的国内外现状及进展》的专题报告,系统回顾了当前结构性心脏病领域中最具前景的两大技术热点——二尖瓣与三尖瓣介入治疗的最新循证证据、器械进展与临床应用现状,尤其聚焦国内从“可用”走向“可及”的转化路径,引发现场强烈共鸣。

01
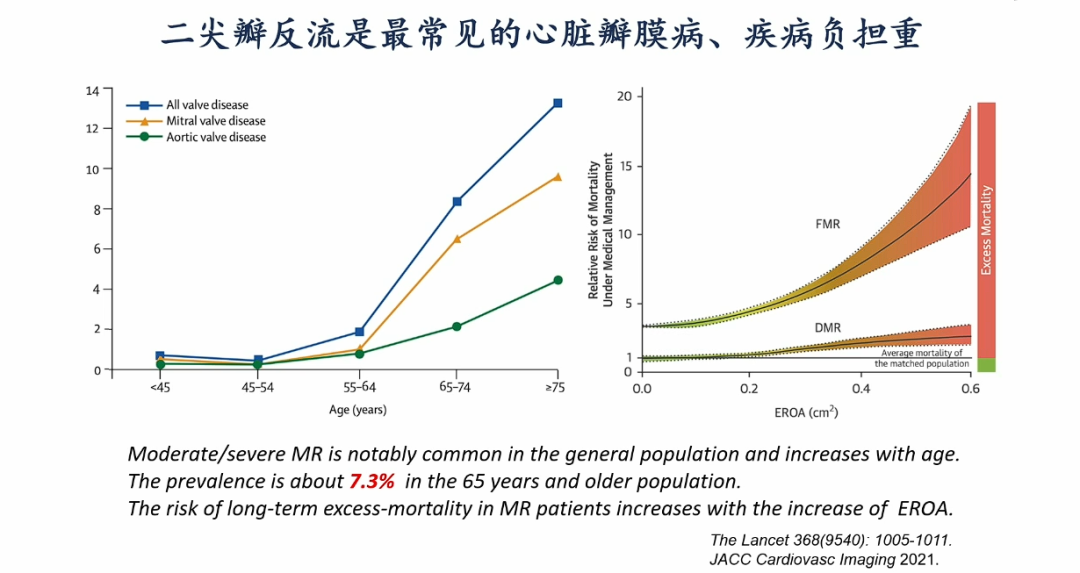
疾病负担:结构性瓣膜病的临床挑战
近年来,二尖瓣反流(mitral regurgitation, MR)和三尖瓣反流(tricuspid regurgitation, TR)作为心力衰竭常见伴随的瓣膜病变,其高发病率和低干预率之间的巨大落差,日益受到全球心血管界关注。
二尖瓣反流是最常见的瓣膜病之一,在65岁以上人群中中重度MR的患病率达7.3%。伴随反流程度的加重,患者全因死亡风险显著上升。尽管临床负担沉重,但实际接受外科手术的比例仍远低于应有水平——数据显示,继发性MR(secondary MR, SMR)患者终生接受外科干预的比例不到5%,而器质性MR(organic MR, OMR)也仅有约三分之一的患者接受治疗。
结构性心脏病介入技术正是在这一背景下迅速崛起,已成为推动二尖瓣治疗格局重构的关键力量。
02
TEER技术:二尖瓣介入治疗的重要路径
在讲座中,陈茂教授梳理了TEER技术的诞生背景与循证路径。
该技术其灵感来源于传统外科Alfieri缝合法,经过系统工程优化后发展出MitraClip和PASCAL等成熟系统。早期的EVEREST II研究在5年随访中已验证了MitraClip在退行性MR治疗中的长期稳定性,后续的CLASP IID研究则显示PASCAL系统在退行性MR人群中疗效不劣于MitraClip,且两者均可显著降低MR程度并提升患者生活质量。这些研究为TEER在原发性MR(PMR)治疗中的广泛应用提供了坚实基础。
然而,对于数量更为庞大的继发性MR患者而言,TEER的疗效呈现出“高度依赖患者选择”的特征。经典的MITRA-FR与COAPT研究揭示了这一点:虽然两者研究设计类似,但结果却截然不同。MITRA-FR研究中,TEER联合药物治疗在2年内未显著优于单纯药物治疗,可能与纳入患者的反流严重程度不足及心衰管理不到位有关;而COAPT研究则纳入了反流程度更重、心衰状态更严重的患者,结果显示TEER可显著降低死亡及心衰住院风险。随后开展的RESHAPE-HF2和MATTERHORN研究进一步深化了“精准筛选”对于TEER疗效的决定性作用,强调反流严重程度、瓣叶解剖结构、左室功能状态等因素应成为术前评估的关键指标。
陈茂教授指出,基于这些研究成果,TEER在SMR患者中的选择策略逐渐明确:
解剖评估方面,瓣叶长度不足、瓣叶对合高度低、前外侧瓣环扩张以及显著左房扩大等因素均提示术后高残余MR风险,需谨慎对待。
功能评估上,EROA超过0.3 cm²、NT-proBNP水平显著升高且LVEF保持在30-50%范围、临床症状仍明显者,是TEER最有可能获益的人群。相反,LVEF低于30%且伴终末期心衰者,或右心功能显著减退者,其受益尚存争议,需结合影像与心衰团队共同评估。

03
经导管二尖瓣置换(TMVR)技术进展
TEER技术目前是二尖瓣介入的主流路径,但其疗效高度依赖瓣膜解剖结构,对于瓣叶拴系严重、对合高度不足或瓣环重构显著的患者,可能面临残余MR及复发风险。因此,经导管二尖瓣置换(TMVR)逐渐成为复杂解剖患者的替代路径之一。
在TEER与TMVR对比总结中,陈茂教授指出,MR具有高度异质性,目前无论TEER或TMVR均难以完全覆盖所有解剖类型,但TEER在患者适应症覆盖范围上仍较TMVR更广。TEER的优势在于操作安全性高、近期疗效稳定;但其局限也明显:其效果依赖术者经验与瓣膜结构,远期可能存在MR复发风险,且若需再次介入治疗,TEER后的解剖空间较为有限。
相比之下,TMVR的优势在于几乎可实现MR的完全消除,可能更有利于逆向重构(reverse remodeling),同时为未来再介入(如ViV)保留空间。但其也存在明确局限:当前TMVR技术仍仅适用于少数患者,常因左室流出道梗阻(LVOTO)、瓣环大小等因素被排除;术中需穿隔,造成的房间隔缺损大于TEER;此外,也存在一定瓣膜血栓风险和操作风险。
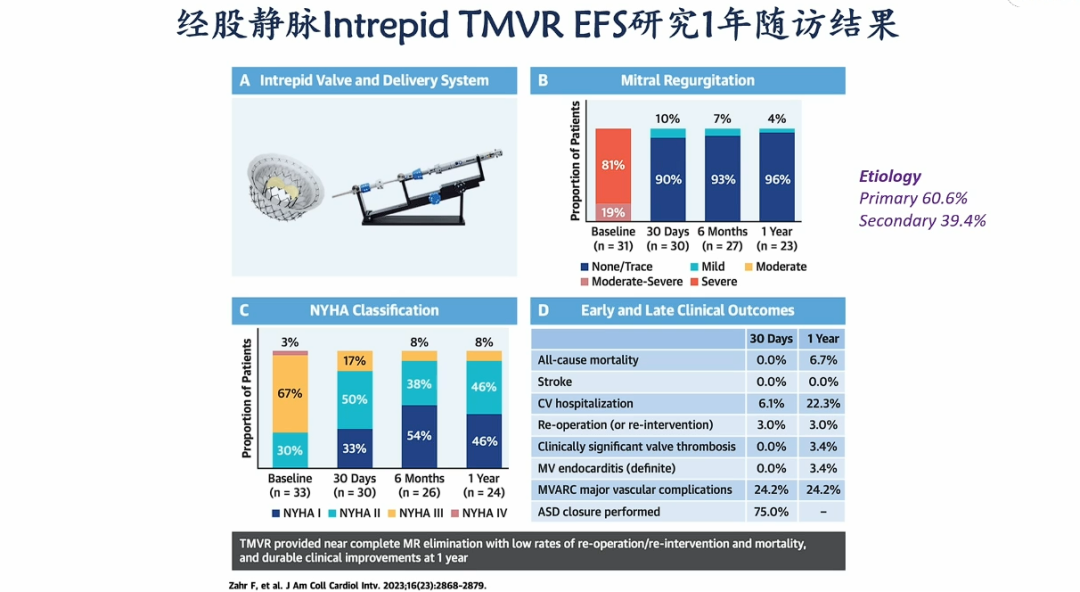
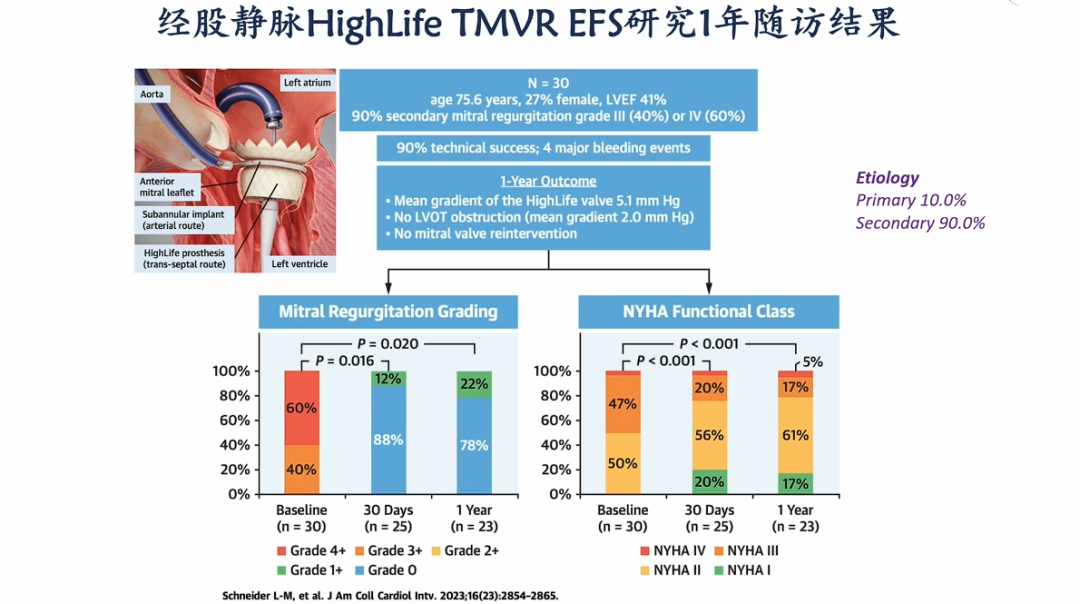
目前国际上已有多个TMVR系统进入临床试验阶段,其中Intrepid系统和Highlife系统较为领先:
Intrepid系统(美敦力 Medtronic)采用“双层结构”设计,外层支架贴合原生瓣环,内层承载生物瓣膜,已完成多个早期试验,初步证实其在选定解剖患者中具有良好封合性与安全性。
Highlife系统(HighLife Medical)则为环绕式锚定结构,具备经导管经股通路的可行性,适用于不规则瓣环患者,目前也进入多中心评估阶段。
随着临床数据积累与器械代际更新,TMVR有望逐步扩展适应人群。国产方面亦有企业在积极推进早期TMVR系统开发,但尚处于临床前验证或初期临床阶段,仍需更大样本和长期随访支持其安全性与有效性。
04
三尖瓣介入:新兴技术的突破与挑战
在总结二尖瓣部分后,陈茂教授将目光延伸至近年来逐渐从边缘走向核心的三尖瓣介入治疗领域。
TR在心衰患者中发病率极高,长期被忽视的“第三瓣膜”如今迎来技术爆发期。他介绍,近年来TTVI(经导管三尖瓣介入治疗)技术类型日益丰富,主要包括TEER(T-TEER)、瓣环成形术和经导管三尖瓣置换术(TTVR)。
在T-TEER方面,TRIUMPHATE研究作为NEJM发表的里程碑式RCT,证实了T-TEER在重度TR患者中可显著降低反流、改善症状,且安全性良好。瓣环成形术则通过收紧扩大的三尖瓣环改善反流,数据显示术后一年内,86%以上患者TR可控制在2+以下,疗效持久稳定。更为激进的TTVR技术,如EVOQUE、Lux-Valve系统,也展现出对复杂TR解剖更强的适应性,在TRISCEND与TRAVIE等研究中取得高达98%以上的轻度残余TR控制率,并显著改善6分钟步行距离和KCCQ评分。
然而,三尖瓣治疗面临的挑战也不容忽视。大规模评估数据显示,在潜在接受TTVI治疗的患者中,仍有近四成因解剖或临床原因被排除,包括右房过度扩张、瓣叶牵拉、肺高压或临床虚弱等。因此,如何根据患者特征匹配最佳介入路径,如何发展更“包容性”的器械技术,是未来TTVI能否从“试验路径”走向“常规治疗”的关键。
05
国产创新:推动“可及性”转化
结构性瓣膜介入器械创新已成为我国心血管技术发展的重点方向。
在二尖瓣领域,各国产系统正逐步完成临床试验评估,进入市场应用,解决当前进口系统成本高、适应症限制等问题。
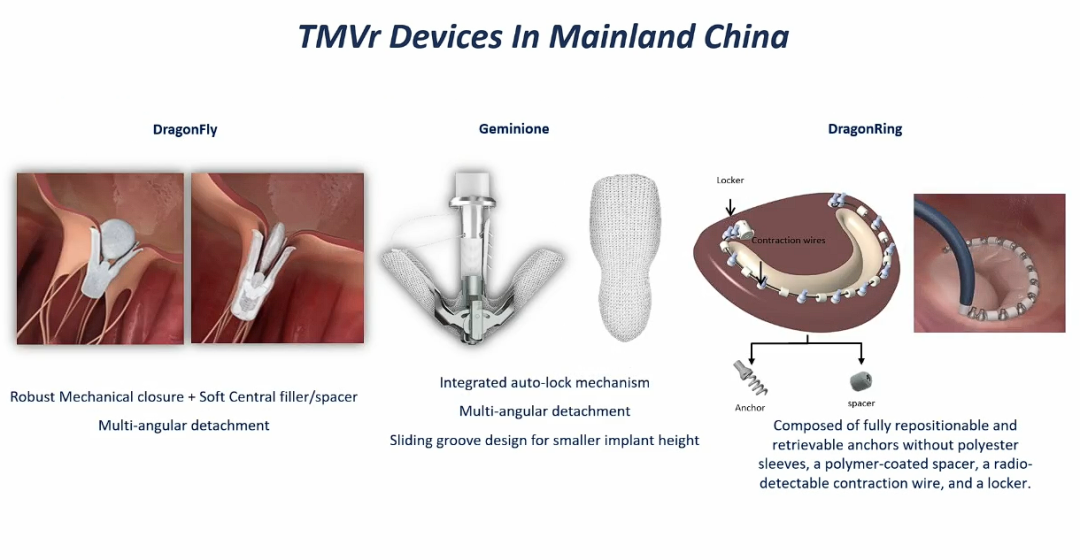
置换方面,国内多个企业推出的置换系统已开展多中心临床研究,数据显示器械成功率高,术后返流和心功能改善显著,安全性良好。
最后,陈茂教授强调,无论是TEER、TTVR还是新兴的经导管置换技术,都体现了结构性心脏病治疗从“外科时代”迈入“微创个体化时代”的整体趋势。在这一过程中,中国不仅是技术引进者,更正加快步伐成为解决方案贡献者。
未来,在完善影像-临床一体化评估模型的基础上,通过自主器械创新、国际多中心研究参与和真实世界路径构建,中国器械将在结构性瓣膜病领域起到越来越重要的作用。
专家简介

识别二维码
进入专家个人主页查看更多信息