

8月21日,“超级心声2.0第六期:TEER进阶技巧——多维度优化手术效果”成功在线上举行。本期会议聚焦二尖瓣经导管缘对缘修复术(TEER)的临床难点与进展,汇聚国内多位心脏介入领域权威专家,为与会医师系统梳理了TEER技术在超声评估、麻醉管理、围术期策略及并发症处理等方面的最新理念与实操要点。会议旨在通过多学科视角的深入交流,助力临床医生进一步提升TEER手术的精准度和安全性,优化患者治疗效果,推动该技术在我国规范化应用与创新发展。
名家汇聚 倾囊相授
▼▼▼

本次会议由中国医学科学院阜外医院段福建教授和上海交通大学医学院附属瑞金医院方跃华教授联合主持,邀请了中国医学科学院阜外医院龚俊松教授、复旦大学附属中山医院李伟教授进行专题授课。同时,会议还特邀了曲靖市中心医院陈玲教授、湖南省人民医院傅庆华教授、江西省人民医院顾平教授、济南市中心医院荆立华教授、西安交通大学第一附属医院王顺教授及北京医院钟优教授作为讨论嘉宾,共同探讨TEER手术的多维度优化策略与临床实践经验。

在开场致辞中,段福建教授回顾了“超级心声2.0”往期活动的亮点,涵盖了二尖瓣解剖知识、超声评估方法、TEER手术流程及术中操作技巧等内容。他指出,本期会议将进一步深入分享TEER手术的丰富临床经验,聚焦手术实操细节和优化策略,旨在帮助临床医生提升手术水平、优化患者治疗效果。
专家讲堂——TEER技术优化新视野与临床探索
▼▼▼
李伟教授:通过瓣叶质地评估优化患者选择

李伟教授在报告开篇便抛出了瓣叶质地评估的核心问题:瓣叶组织是否能够耐受M-TEER修复器械的夹合?如何通过质地评估来预测手术的成功率及并发症风险?他指出,瓣叶质地的本质是对瓣叶“组织健康”的关注,它直接决定了修复术后的有效性、耐久性与安全性。

瓣叶质地是指瓣叶组织的物理学特性,包括柔韧性、厚度、纤维化和钙化程度。二尖瓣的三层组织结构中,海绵层富含蛋白多糖,质地疏松,起缓冲作用,使瓣叶保持弹性与柔顺;纤维层则富含致密的胶原蛋白纤维,是主要的承重层,赋予瓣叶足够的韧性和结构强度。

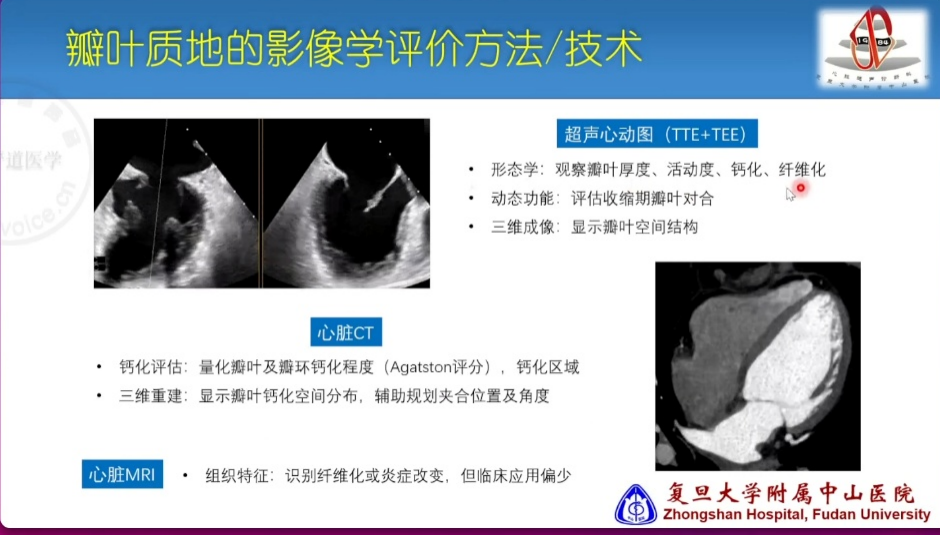
在影像学评估方面,常用的技术包括超声心动图(TTE与TEE)、心脏CT及心脏磁共振(CMR)。超声成像中一些特征性表现能够提示瓣叶质地问题,例如“折臂征”显示瓣叶组织连续性中断,提示TEER相关瓣叶存在易损高危;而“僵块征”则反映瓣叶弹性与柔顺性丧失,对合功能受限,从而导致TEER疗效欠佳。还解读了不同增益对瓣叶评估的影响。
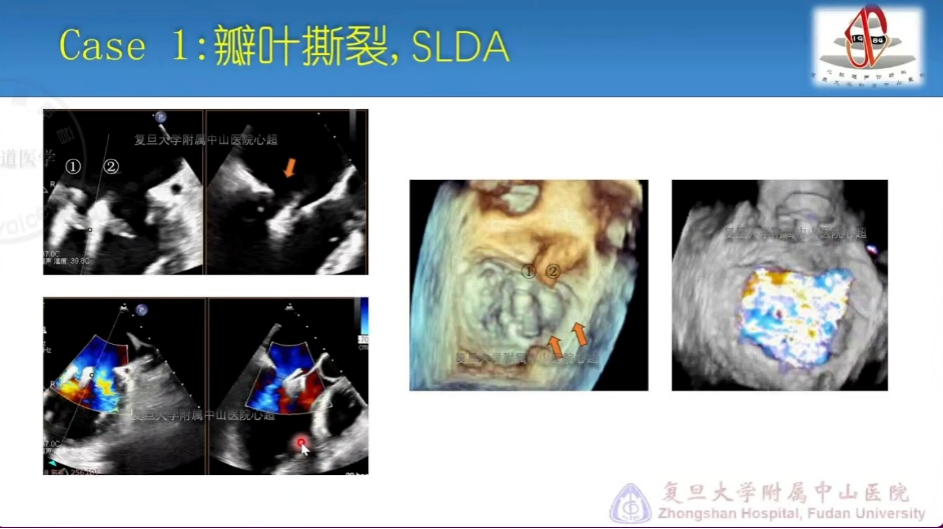
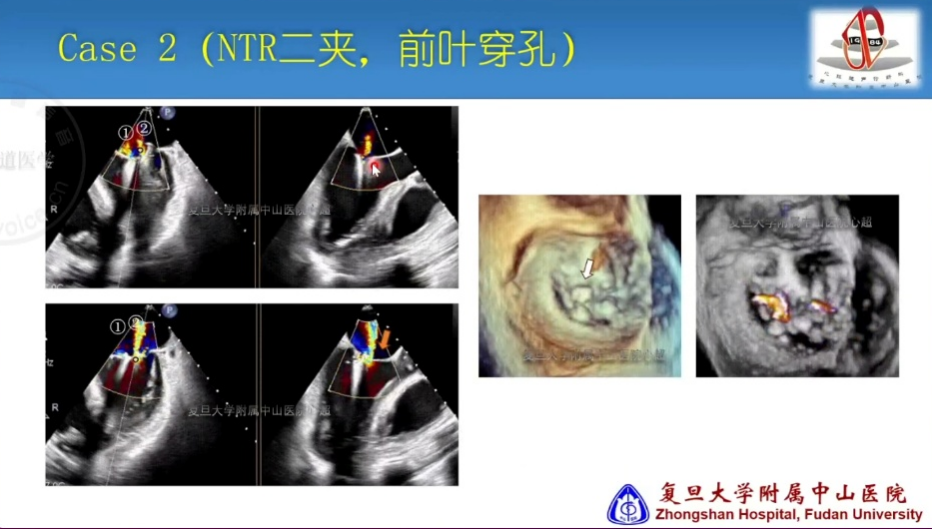
在最后的两则病例分享中,李伟教授还特别提到,糖皮质激素可能通过调节胶原代谢、改变组织结构完整性,进而降低瓣叶弹性与强度,对瓣叶质地及功能造成不利影响。
龚俊松教授:TEER术中麻醉精准控制

龚俊松教授在报告中深入阐述了TEER手术麻醉所面临的挑战、管理难点以及优化策略。TEER手术多在导管室进行,麻醉工作区域有限且伴随辐射风险,这对麻醉管理提出了特殊挑战。由于多数手术可在镇静镇痛下完成,麻醉医生需熟练掌握不同镇静深度下的呼吸与循环调控,但患者常为仰卧位且手术台活动受限,一旦发生气道紧急情况处理难度显著增加,且导管刺激、球囊扩张或快速起搏等操作均可能诱发严重血流动力学波动。


为确保安全,术前必须进行全面评估,包括心脏功能、瓣膜病变严重程度、合并症及全身状态,并在心衰患者中优化容量与药物管理,合理制定抗凝方案。麻醉方式方面,不同于TAVI,目前全球范围内TEER仍以全身麻醉气管插管为主,诱导药物选择需谨慎,同时必须备齐全套抢救药物与气管插管设备,以便应对镇静失败或突发情况。术中管理重点在于全面监测,例如精准控制血流动力学,维持足够心排量的同时避免加重二尖瓣反流,并兼顾心肌收缩力与外周阻力平衡;


呼吸管理需根据患者具体情况个体化调整,抗凝监测以ACT为核心。术后则应加强心功能、肾功能及潜在出血风险的监测,确保平稳过渡。龚教授最后强调,TEER术中麻醉的核心在于对病理生理和解剖学的深刻理解、对循环系统的精准掌控以及与TEE团队的无缝协作,而个体化的麻醉方式选择、并发症的快速识别与及时处理,是保障手术成功与患者安全的关键。
专家讨论——共探TEER多维度优化精要
▼▼▼
陈玲教授:对于心肌梗塞患者,如出现细小腱索断裂、二尖瓣脱垂并伴有大量反流的情况,这类患者是否适合接受TEER手术?在超声评估时,除了关注二尖瓣本身,还需要在心脏功能、室壁运动等方面有哪些特别的注意事项?
李伟教授:一般来说,如果是急性心梗出现乳头肌断裂,患者病情危急,在血运重建后仍无法改善时,可以考虑行急诊TEER手术,作为桥接治疗的手段。如果病程已过一段时间,通常在两周以后,待急性水肿期过去,也同样可以实施TEER手术。对于存在腱索断裂并伴随室壁运动异常的“混合型”患者,也可以选择TEER。需要特别注意的是,术前必须充分评估心功能情况,同时对心腔内血栓、室壁瘤以及房间隔高度进行全面评估,这些因素对手术安全性和成功率都至关重要。
王顺教授:在讨论中回顾了自己中心的两个病例。第一个病例为瓣叶脱垂患者,手术时夹合可能过紧,术后出现瓣叶穿孔,不得不转至心外科行瓣膜置换手术。这提示我们在TEER操作中需高度重视瓣叶质地的评估,因为过紧的夹合可能导致瓣叶张力过大,从而增加并发症风险。第二个病例是一位ICU内的急性心梗重症患者,团队为其实施TEER手术,术后患者成功脱离IABP及ECMO支持,但在一周后出现大量反流,最终仍需转外科治疗。该病例提示TEER在某些危重患者中可作为桥接手段,不仅能够为患者赢得时间,也为后续心外科手术创造了更好的条件。
顾平教授:在老年性二尖瓣病或粘液性病变患者中,如何评估瓣叶质地?又如何判断其是否适合接受TEER手术?
李伟教授:对于多区段病变,首先要关注瓣叶厚度是否均匀。此类患者常表现为瓣叶冗长,如果瓣叶较厚,可以适当多夹合,一般不必过于担心瓣叶撕裂;但若瓣叶厚度不足,则需要高度警惕撕裂风险,操作上必须更加谨慎。
顾平教授:对于接受钳夹术后复查时出现反流增多的患者,在评估过程中应重点关注哪些方面?
段福建教授:需要重点评估夹子的形态和位置,同时明确反流量的大小,并追踪残余反流的起源,以判断问题所在。
顾平教授:作为超声医生,在术中如何就潮气量的调节与麻醉医生进行沟通?
龚俊松教授:超声医生应主动与麻醉医生沟通,以保障手术顺利进行。例如,在CDS进入左房调整位置或测试弹道后,可建议麻醉医生适当增加5-10mmHg的PEEP,以减少静脉回心血量、缩小左房容积,从而减小二尖瓣前后叶的对合间隙,更利于夹持操作。对于高龄或循环状态不稳定、无法耐受较高PEEP的患者,可考虑采用小潮气量通气策略(建议潮气量约为5ml/kg),在尽可能减少循环干扰的同时,也有助于实现更稳定的夹持条件。
傅庆华教授:病人在术中用二维很难判断是穿孔还是局部瓣叶菲薄,三维增益后也无法看清,遇到这种情况应如何调整,使用什么夹合策略?
李伟教授:判断是否穿孔,首要观察夹子的形态,若Arm一端明显高出瓣叶平面,且瓣叶连续性中断,则提示穿孔。二维超声相比三维超声更易识别穿孔,因三维图像受分辨率和增益限制,常难以清晰显示细微结构,其主要作用在于判断反流来源。若已发生穿孔,但总体反流量不大且夹子稳定,可进一步评估瓣叶张力。若瓣叶质地本身无法改变,则应设法降低张力。具体操作上,可在夹子夹合后先将夹臂关至60°,观察瓣叶张力及前后叶夹合程度。若无异常,则可缓慢关闭夹子,同时将夹子稍向心室侧推送,以释放张力。若关闭后残余反流增加,则需在旁边加置一枚夹子,注意两夹对称排列,避免造成瓣叶扭曲。
荆立华教授:对于急性心梗伴乳头肌功能不全的患者,在急性期是否可以积极干预二尖瓣反流?
方跃华教授:对于处于急性期的急性心梗患者,首先要评估血流动力学是否稳定。如果血流动力学稳定,则不必立即处理,很可能属于功能性反流。若患者出现乳头肌断裂,急性期往往伴随血流动力学不稳定、肺水肿或心源性休克,此时无法立即进行外科手术,可以选择TEER作为桥接治疗,以稳定血流动力学、实现平稳过渡,为后续心外科手术创造条件。
荆立华教授:测量二尖瓣厚度时,应采用经胸还是经食道超声?是否存在测量误差?增益应设置多少合适?
李伟教授:建议采用经食道超声评估瓣叶厚度,因为分辨率更高。测量时以瓣叶体部为主,增益一般设置在60左右较为合适。
钟优教授:对于同时具备心内科和心外科手术指征的患者,有哪些特点可以判断应先行内科干预还是外科手术?
方跃华教授:对于一些急性期患者,往往暂时不具备外科手术条件,此时可先行TEER作为桥接治疗。此外,对于合并多瓣膜病变的患者,可以根据具体瓣膜病变的类型和严重程度,选择分期手术或一站式手术策略等等。
会议总结——TEER优化之路聚力前行
▼▼▼

本次会议立足多学科融合视角,系统探讨了TEER手术从术前评估、术中操作到麻醉管理的多维度优化策略,为提升手术安全性与有效性提供了全面而实用的临床指导。方跃华教授在总结中指出,非常荣幸邀请到两位讲者进行授课。在此次报告中,李伟教授强调了瓣叶质量对于TEER手术成功的重要性,分享了二尖瓣瓣叶质地的解剖特点、手术难度评估及手术策略优化。龚俊松教授系统介绍了麻醉团队在TEER手术中的工作重点,包括术前评估、术中麻醉管理细节以及术后管理措施。在讨论环节中,与会专家重点交流了急性心梗伴乳头肌断裂患者的手术策略,探讨了不同病程和病情下的TEER干预时机及桥接手术方案,为临床实践提供了丰富经验和指导。