

2025年8月29日,欧洲心脏病学会(ESC)与欧洲动脉粥样硬化学会(EAS)在马德里年会重磅发布《2019ESC/EAS血脂异常管理指南:2025重点更新》。这版指南在全球心血管疾病负担持续加重的背景下,以更精准的风险分层、更灵活的联合策略和更前瞻的治疗理念,为临床医生提供了全新的实践框架。
本文将深入解析指南核心更新,系统梳理14种降脂药物联合方案的临床要点。
风险评估体系的革命性升级
2025版指南最显著的变革在于引入新型风险预测模型——SCORE2与SCORE2-OP。与2019版相比,新模型不仅预测10年心血管死亡风险,更纳入非致命性事件发病率评估,其中SCORE2-OP专为70-89岁人群定制,解决了老年患者风险评估失真的临床痛点。这种精细化分层直接推动治疗策略的个体化调整,使临床医生能更科学地决定干预时机和强度。
指南对极高危人群的定义进一步扩展,除传统的ASCVD患者外,家族性高胆固醇血症(FH)、慢性肾病(CKD)4-5期、糖尿病合并靶器官损害等人群均被纳入强化治疗范畴。特别值得注意的是,指南推荐所有成年人一生中至少检测一次脂蛋白(a)[Lp(a)],对FH患者、早发ASCVD家族史者等高危群体更强调定期监测,因为Lp(a)升高是独立的心血管危险因素,其水平与终生心血管事件风险呈正相关。
风险评估的革新直接影响治疗目标设定。指南根据不同风险等级确立了更严格的LDL-C目标值:超高危人群需降至<1.0mmol/L且较基线降低≥50%;极高危人群需降至<1.4mmol/L且较基线降低≥50%;高危人群<1.8mmol/L且较基线降低≥50%;中危人群<2.6mmol/L。这种阶梯式目标体系为联合治疗提供了明确的实施依据,也解释了为何指南对多药联合策略的推荐力度显著增强。
以他汀类药物为基础的治疗方案
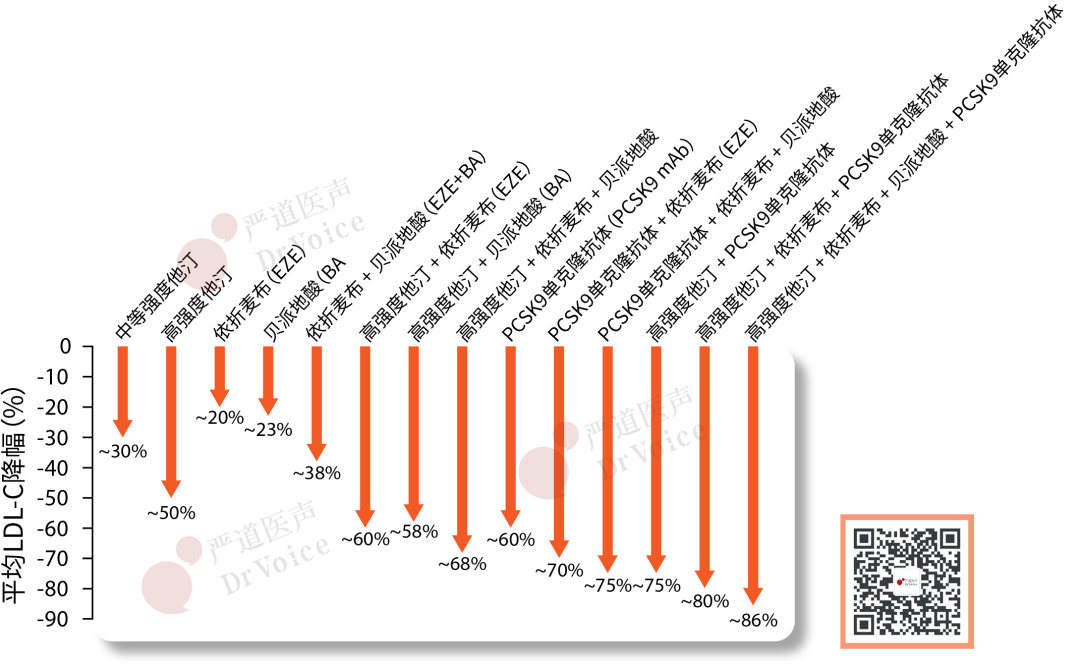
中等强度他汀(如阿托伐他汀20mg、瑞舒伐他汀10mg)仍是中低危人群的初始治疗选择,其可降低LDL-C约30%,安全性良好。
高强度他汀(如阿托伐他汀40-80mg、瑞舒伐他汀20-40mg)适用于高危及以上人群,单药可降低LDL-C约50%以上。但需注意亚洲人群对高强度他汀的耐受性可能较差,临床应用时应密切监测肝酶和肌酸激酶(CK)水平。指南特别指出,HIV感染者和化疗相关心脏损伤高风险的癌症患者也应考虑他汀治疗,打破了传统上对这些人群使用他汀的顾虑。
指南强调,不同个体对特定降脂药物或药物联合治疗的LDL-C降低反应存在显著差异,因此在启动或调整任何降脂治疗后,均需监测治疗效果。如2019年ESC/EAS指南所述,应在启动或强化降脂治疗后4~6周检测LDL-C水平。
非他汀类药物的单药与双联策略
依折麦布(EZE)作为胆固醇吸收抑制剂,单药可降低LDL-C约20%,但其临床价值主要体现在联合治疗中。对于他汀不耐受或单药未达标的患者,依折麦布是理想的联合伙伴,因其不增加肝脏负担和肌病风险。
贝派地酸(BA)作为新型ATP柠檬酸裂解酶抑制剂,为他汀不耐受患者提供了重要选择。单药可降低LDL-C约23%,其独特优势在于通过肝脏特异性代谢,避免了他汀常见的肌毒性——因骨骼肌缺乏其活化所需的ACSVL1酶,故肌肉相关不良反应发生率与安慰剂相当。CLEAR-OUTCOME研究证实,贝派地酸在他汀不耐受人群中可降低主要心血管事件风险13%,为其单药使用提供了循证依据。指南指出,由于贝派地酸会导致尿酸轻微且可逆性升高,因此有痛风病史的患者需谨慎使用,但痛风并非贝派地酸治疗的绝对禁忌证。
依折麦布+贝派地酸(EZE+BA)的固定剂量组合是指南推荐的无他汀方案,尤其适用于完全不耐受他汀的患者。两者机制互补——贝派地酸抑制肝脏胆固醇合成,依折麦布减少肠道吸收,联合可降低LDL-C达38%,且不影响血糖代谢,适合糖尿病患者。但需注意该组合的降脂强度仍不及他汀联合方案,故主要用于他汀禁忌证患者。
他汀与非他汀的双联联合方案
高强度他汀+依折麦布(EZE)是指南推荐的一线联合策略,可降低LDL-C约60%。IMPROVE-IT研究的长期数据显示,该组合在ACS患者中较单用他汀进一步降低主要终点事件6.4%,且获益随时间延长而增加,6年后统计学差异显著,两组肌病、肝酶升高发生率无显著差异。对于基线LDL-C较高的极高危人群,建议起始即采用该联合方案,而非逐步升级。

高强度他汀+贝派地酸(BA)的组合可降低LDL-C约58%。贝派地酸的抗炎特性(降低hs-CRP)可能带来额外心血管获益,但目前缺乏该组合与他汀+依折麦布的头对头比较数据。
三联联合方案
高强度他汀+依折麦布+贝派地酸的三联组合可实现LDL-C降幅达68%左右,适用于中等强度联合治疗未达标的高危患者。该方案的优势在于全口服给药,患者依从性可能优于包含注射剂的方案。但需注意,目前支持该组合的心血管结局数据有限。
PCSK9单克隆抗体(PCSK9 mAb)单药可降低LDL-C约60%,推荐用于他汀和依折麦布均不耐受的特殊情况。其临床价值主要体现在对极高危人群的强化干预。依洛尤单抗和阿利西尤单抗的起效迅速,可在4-7天内使LDL-C降至最低水平,为ACS等急性场景提供快速控制手段。
PCSK9 mAb+依折麦布(EZE)的无他汀组合适用于他汀完全不耐受的极高危患者。两者机制协同,可降低LDL-C约70%,且不增加肝肾负担。
PCSK9 mAb+依折麦布+贝派地酸的三联无他汀方案是他汀绝对禁忌患者的终极选择,可降低LDL-C达75%以上。因缺乏长期心血管结局数据,且成本较高。临床应用时需严格评估患者的风险-获益比。
包含PCSK9抑制剂的强化联合方案
高强度他汀+PCSK9 mAb可使LDL-C降低约75%,适用于极高危人群中基线LDL-C显著升高者。FOURIER研究显示,该组合较他汀单药进一步降低主要终点事件15%,且获益在7-8个月即显现。对于极高危患者,可考虑早期启动该联合方案以快速稳定斑块。

高强度他汀+依折麦布+PCSK9 mAb是高强度口服+注射联合方案,LDL-C降幅可达80%左右。ODYSSEY OUTCOME研究证实,在近期ACS患者中,该方案较他汀联合依折麦布进一步降低MACE风险14.4%。对于FH患者和多次复发的ASCVD患者,建议尽早采用该方案以实现深度降脂目标。

高强度他汀+依折麦布+贝派地酸+PCSK9 mAb的四联方案代表当前最强效的降脂策略,LDL-C降幅可达86%,主要用于难治性病例。临床应用中需注意,四联方案的长期安全性数据有限,应在专科中心由经验丰富的医生实施。
单克隆抗体依维库单抗(evinacumab)
对于纯合子家族性高胆固醇血症(HoFH)患者,指南指出,他汀类药物和PCSK9抑制剂疗效有限,可能不足以充分降低LDL-C水平;而针对血管生成素样蛋白3(ANGPTL3)的单克隆抗体依维库单抗(evinacumab)已显示出潜在获益,可使LDL-C降低近50%。
2025版指南的发布标志着血脂管理进入"精准分层、联合制胜"的新时代。其核心价值体现在三个维度:一是风险评估的精细化,SCORE2/OP模型与Lp(a)筛查的结合,使临床决策从经验医学迈向精准医学;二是治疗策略的多元化,贝派地酸和新型依维库单抗(evinacumab)的引入,为他汀不耐受患者和纯合子家族性高胆固醇血症(HoFH)患者提供了有效选择;三是治疗目标的严格化,更具挑战性的LDL-C目标值推动了联合治疗策略的广泛应用。临床医生应深入理解指南精髓,将其转化为改善患者预后的实际行动,最终实现心血管疾病防治的宏伟目标。