
转甲状腺素蛋白淀粉样变性(ATTR)是一种进行性、危及生命的全身多系统疾病,心脏是其最常累及的器官之一。由于其临床表现异质且缺乏特异性,加之我国临床医务人员认知不足,导致该病漏诊、误诊及诊疗延迟率极高,患者预后差。早期诊断与治疗能显著改善患者预后,因此,提升对ATTR的识别能力,特别是对以心脏表现为首诊症状患者的识别,已成为心血管内科医师必须掌握的关键技能。
近日,国家放射与治疗临床医学研究中心组织多领域专家,基于最新循证医学证据和最佳临床实践,撰写了《转甲状腺素蛋白淀粉样变性多学科协作筛查与诊断路径专家共识(2026)》,发表在最新一期《中华心血管病杂志》上。本共识旨在制定一套契合中国临床实践的多学科协作筛查与诊断路径,以推动ATTR的早期确诊与及时治疗。
01
ATTR不只是心脏的疾病,而是全身系统性问题
分型与流行病学:
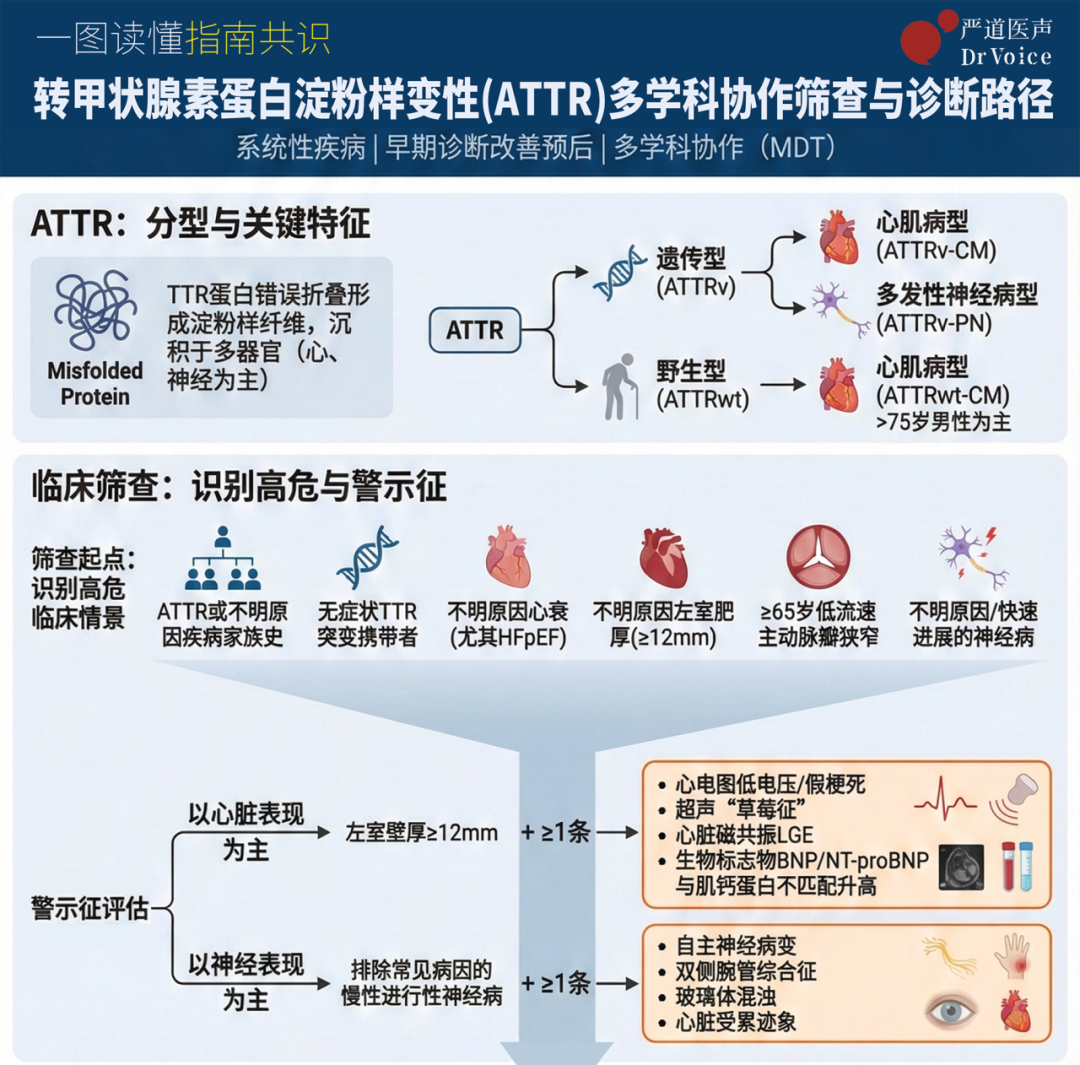
ATTR的根本病因在于可溶性转甲状腺素蛋白(TTR)错误折叠形成淀粉样纤维,沉积于全身多个器官并造成损伤,其中心脏和周围神经是最常见的受累部位。根据是否存在TTR基因突变,可将ATTR分为遗传型/突变型(ATTRv)和野生型(ATTRwt)两大类,结合临床表现还可对两型进行进一步细分:ATTRv可分为心肌病型(ATTRv-CM)、多发性神经病型(ATTRv-PN)和混合型,ATTRwt则分为心肌病型(ATTRwt-CM)和混合型,基因型与临床表型存在明确的对应关系。
根据是否存在TTR基因突变,两大类型临床特点如下:
遗传型/突变型(ATTRv):呈常染色体显性遗传。全球报道约5万例,目前已发现超过130种TTR基因致病突变。中国最常见突变为Val30Met和Ala97Ser。未经治疗的患者中位生存期因突变类型和主要受累器官而异,例如遗传型心脏淀粉样变性(ATTR-CM)患者中位生存期约为2.6至5.8年。
野生型(ATTRwt):无基因突变,与年龄密切相关。全球患者数量估计在20万至30万例。在老年人群中患病率不容忽视(例如,65-90岁人群中约0.46%)。尤其需要警惕的是,射血分数保留的心力衰竭(HFpEF)合并左心室壁增厚(≥12mm)的50岁以上患者中,野生型ATTR-CM的患病率可高达13.4%。未经治疗的ATTRwt患者中位生存期约为3.6至4.8年。
从心血管内科临床视角来看,ATTR-CM是临床最需关注的表型,其中ATTRwt-CM患者确诊年龄多介于47~94岁,以75岁以上人群为主,且男性占比达80%~90%;ATTRv-CM患者确诊年龄多为60岁以上,男性占比70%,这一性别和年龄特征可为临床初步识别提供参考。
关键提示:ATTRwt在中国尚无确切流行病学数据,且临床确诊患者极少,这恰恰提示存在大量未被识别的病例,是漏诊的重灾区。
临床表现
ATTR可累及心脏、周围神经、中枢神经、胃肠道、骨骼肌肉、肾脏及眼等多个系统,起病隐匿,因受累器官不同呈现出复杂多样的临床表现,且缺乏特异性。对于心血管内科医师而言,需跳出单纯心脏病的思维定式,关注多系统线索。
心脏表现:心力衰竭(尤其是HFpEF)、主动脉瓣狭窄、心律失常、心原性栓塞、晕厥及心脏性猝死。
其他系统伴随表现:在接诊疑似患者时,以下合并情况需高度警惕ATTR可能:
o 周围神经受累可出现体位性低血压、性功能障碍、出汗障碍等自主神经症状,以及肢体麻木疼痛、肌肉无力等多发性感觉运动神经病症状;
o 胃肠道受累表现为腹泻与便秘交替、持续恶心呕吐、不明原因体重下降等;
o 骨骼肌肉受累可见双侧腕管综合征、肱二头肌肌腱断裂(大力水手征)、腰椎管狭窄及关节疼痛;
o 还可累及肾脏(蛋白尿、肾功能不全)、眼部(瞳孔异常、玻璃体混浊)、中枢神经(脑出血、脑梗死)等。
02
诊断路径:从疑诊到确诊
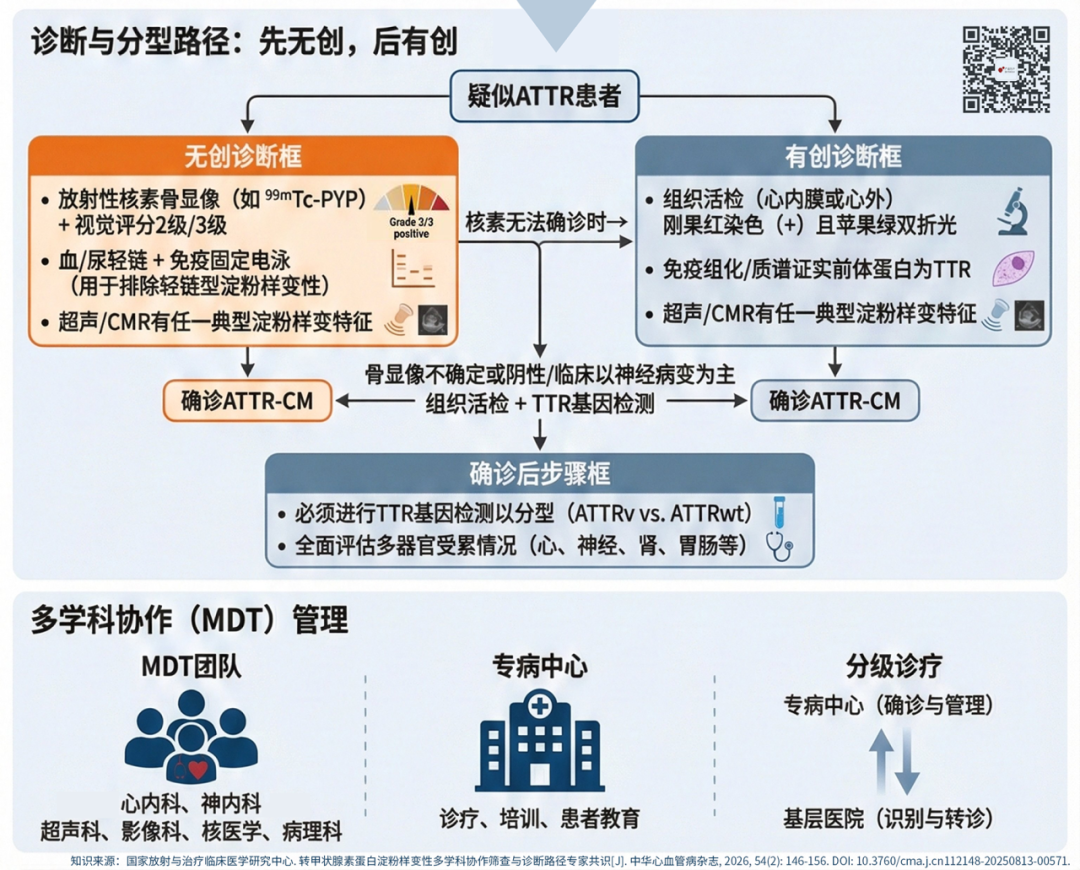
ATTR的诊断需依托多种检查方法的互补与联合应用,遵循“先无创、后有创”的基本原则,核心检查手段包括生物标志物检测、无创多模态影像检查、组织活检及基因检测。超声心动图和心脏磁共振是心血管内科医师诊断心脏淀粉样变性的核心无创影像手段,共识明确要求,若上述检查发现典型心脏淀粉样变性特征,需在报告中明确提示,以启动后续确诊流程。
辅助检查
共识详细列出了各项检查的典型表现,心内科医师应重点关注以下内容:
生物标志物:
o 利钠肽(BNP/NT-proBNP):呈现与心力衰竭严重程度不呈比例的升高。
o 高敏心肌肌钙蛋白T(hs-cTnT):表现为持续、低水平的升高,与急性心肌梗死的快速剧烈升高模式不同。
o 单克隆球蛋白筛查:血清游离轻链比值及血清/尿蛋白免疫固定电泳是鉴别ATTR与轻链型淀粉样变性(AL)的关键。ATTR患者上述指标通常在正常范围且未检出单克隆蛋白。
无创多模态影像检查:
o 心电图:ATTR-CM患者的心电图具有特征性改变,且与超声心动图表现存在矛盾性,是重要的初筛线索:肢体和/或胸导联无QRS高电压表现,但超声心动图示左心室肥厚;可见Q波或T波的假性梗死征象、胸导联R波递增不良;合并各类心律失常,如心房颤动、室内传导阻滞等。
o 超声心动图:是心血管内科诊断ATTR-CM的核心检查,典型心脏淀粉样变性特征为诊断的重要依据,典型特征包括:
1. 不明原因左心室壁厚度≥12mm;
2. 舒张功能障碍≥2级,判定标准为e′减低(按年龄划分临界值)、E/e′比值增加(间隔≥15或侧壁≥13或平均值≥14)、三尖瓣反流速度≥2.8cm/s或肺动脉收缩压≥35mmHg三项指标均超临界值,其中E/A比值<2.0为2级,≥2.0为3级;
3. 组织多普勒s′、e′和a′降低(<5cm/s);
4. 左心室整体纵向应变绝对值<15%,尤其存在“心尖保留”征象(左心室心尖部平均纵向应变/(基底段+中间段平均纵向应变)比值>1.0),即“草莓征”,该征象对ATTR-CM具有较高的特异性。
5. 其他征象:还可出现心肌“颗粒状闪光”外观、双心房扩大、左心室相对室壁厚度>0.6、房室瓣及房间隔增厚、心包积液等辅助征象。
共识强烈建议:超声医生在报告中若发现典型心脏淀粉样变性特征,应明确提示,以启动临床确诊流程。
o 心脏磁共振:是诊断ATTR-CM的重要补充手段,典型特征包括:电影成像序列中左心室壁厚度≥12mm;弥漫性心内膜下或透壁性钆对比剂延迟增强(LGE),且不符合冠状动脉供血分布特征;固有心肌T1值异常升高,或钆动力学异常;左心室心肌细胞外容积(ECV)>40%,该指标对诊断具有强支持作用。同时可伴随双心房扩大、左心室异常纵向应变、房间隔及瓣膜增厚等表现。
o 放射性核素骨显像(如99mTc-PYP显像):对ATTR-CM的诊断具有重要价值,采用视觉评分法分为4级:0级为无心肌摄取,仅正常骨摄取,可排除ATTR-CM;1级为轻度心肌摄取(低于肋骨摄取),需进一步评估;2级为心肌与肋骨摄取量相当;3级为心肌摄取量大于肋骨摄取量,可作为ATTR-CM的诊断依据。平面显像半定量分析法可作为补充,1h图像心脏与对侧肺的摄取比值(H/CL)>1.5或3h图像H/CL>1.3,即可判定为阳性。同时,需确保单克隆球蛋白筛查阴性以排除AL。
o 神经电生理检查:主要用于评估周围神经受累情况,表现为以轴索损害为主的感觉运动神经病、感觉神经及复合肌肉动作电位波幅下降,针极肌电图可见四肢远端肌肉神经源性损害,交感皮肤反应潜伏期延长、波幅降低,可为ATTR的分型诊断提供依据。
有创检查:
o 组织活检:当无创检查无法确诊时进行,组织活检是ATTR诊断的有创金标准之一,可选择唾液腺、周围神经、骨骼肌、心脏、腹部皮下脂肪等多个部位,多次或联合活检可提高阳性率。活检组织的核心诊断标准为:刚果红染色阳性,且在偏振光下呈苹果绿双折射;通过免疫组织化学、免疫荧光、免疫电镜或激光显微切割联合质谱分析,确定淀粉样纤维的前体蛋白为TTR。
基因检测:用于明确ATTRv分型,是遗传咨询和家系筛查的基础。
诊断标准
共识明确了两种主要临床表型的诊断标准:
ATTR-CM诊断标准:
1. 无创路径(首选):放射性核素骨显像(如PYP)心肌摄取达2或3级,且单克隆球蛋白筛查阴性,且超声心动图或心脏磁共振存在任一典型心脏淀粉样变性特征,即可确诊。
2. 有创路径:若骨显像无法诊断,则需组织活检证实TTR蛋白沉积。
ATTRv-PN诊断标准:
1. 存在TTR基因致病突变,且合并无法用其他原因解释的进行性多发性神经病/自主神经病。
2. 或通过组织活检(如神经、脂肪)证实为TTR蛋白沉积。
03
ATTR的多学科协作筛查策略
ATTR的早期识别难度较大,心血管内科医师在临床工作中,需通过详细询问患者病史、家族史,首先识别存在高危临床情景的人群,再开展针对性的警示征评估,从而筛选出疑似患者,启动后续诊断流程。
1.高危临床情景识别
接诊患者时,若存在以下任一情景,应警惕ATTR可能:
有ATTR家族史,或家族中有不明原因的心力衰竭、猝死、快速进展的神经病患者。
无症状的TTR基因致病突变携带者。
不明原因的心力衰竭(尤其是HFpEF)。
不明原因的左心室肥厚。
年龄≥65岁,合并低流速、低压力阶差的主动脉瓣狭窄,或严重主动脉瓣狭窄。
不明原因的慢性进行性神经病。
快速进展的多发性神经病且对常规治疗(如丙种球蛋白)无应答。
2.警示征评估
识别高危情景后,需进行针对性评估以筛选出疑似患者:
以心脏表现为主者:若存在不明原因左心室壁厚度≥12mm,并合并以下至少1条警示征,应怀疑ATTR-CM:
o 年龄≥60岁(男性风险更高)。
o 存在HFpEF。
o 心电图出现低电压、假性梗死征等。
o 超声心动图显示“心尖保留”征、舒张功能障碍等。
o 心脏磁共振显示典型LGE或ECV升高。
o 生物标志物NT-proBNP或hs-cTnT升高。
o 合并心外表现:如双侧腕管综合征、腰椎管狭窄、不明原因周围神经病变等。
以神经表现为主者:若存在排除了糖尿病等常见病因的慢性进行性神经病,并合并心脏受累(如超声显示室壁增厚、利钠肽升高等)或其他系统受累警示征,应怀疑ATTRv-PN。
04
多学科协作,打破学科壁垒
ATTR作为全身多系统疾病,单一科室无法完成全程诊疗,共识强调需建立完善的多学科协作(MDT)管理体系,心血管内科作为核心科室,在团队中承担着心脏病变评估、诊断、治疗及长期随访的关键角色。
组建ATTR多学科协作团队:应以心血管内科、神经内科为核心,联合超声诊断科、影像科、核医学科、病理科、遗传咨询等专家。其核心职能:
1. 协同诊疗:共同制定筛查、诊断和个体化治疗方案。
2. 全周期管理:对确诊患者及无症状基因携带者进行定期随访评估。
3. 遗传咨询与宣教:为患者及其家属提供专业的遗传咨询和疾病知识教育。
体系建设:鼓励有条件的医院建设ATTR专病中心或专病门诊,并建立分级诊疗转诊机制,让基层医院能识别并转诊疑似患者,由上级专病中心完成确诊和复杂管理。
05
严道心得
在临床工作中,遇到射血分数保留的心力衰竭(HFpEF)或不明原因左心室肥厚的患者,特别是老年男性,ATTR-CM必须纳入鉴别诊断清单。不能再满足于高血压性心脏病或老年性改变等模糊解释。共识中提到的“HFpEF伴室壁增厚患者中ATTRwt患病率达13.4%”这一数据,足以让我们警醒。
过去,心脏淀粉样变性的确诊高度依赖有创的心内膜心肌活检,门槛高、推广难。如今,超声心动图(“草莓征”)、心脏磁共振(特征性延迟强化)和放射性核素显像构成了强大的无创诊断体系。心内科医师需要熟悉这些影像学特征,并能正确解读和排序这些检查。
询问病史时,应有意识地探查双侧腕管综合征、腰椎管狭窄、自主神经功能异常(如体位性低血压)、胃肠道症状等线索。这些不起眼的合并症,往往是提示ATTR这一全身性疾病的蛛丝马迹。
ATTR的诊断和管理涉及多个专业。心内科医师应主动成为多学科团队的发起者和协调者,与神经科、影像科、核医学科、病理科同事建立常态化协作机制。这不仅有助于复杂病例的确诊,也为患者后续的全面评估和治疗奠定了基础。