
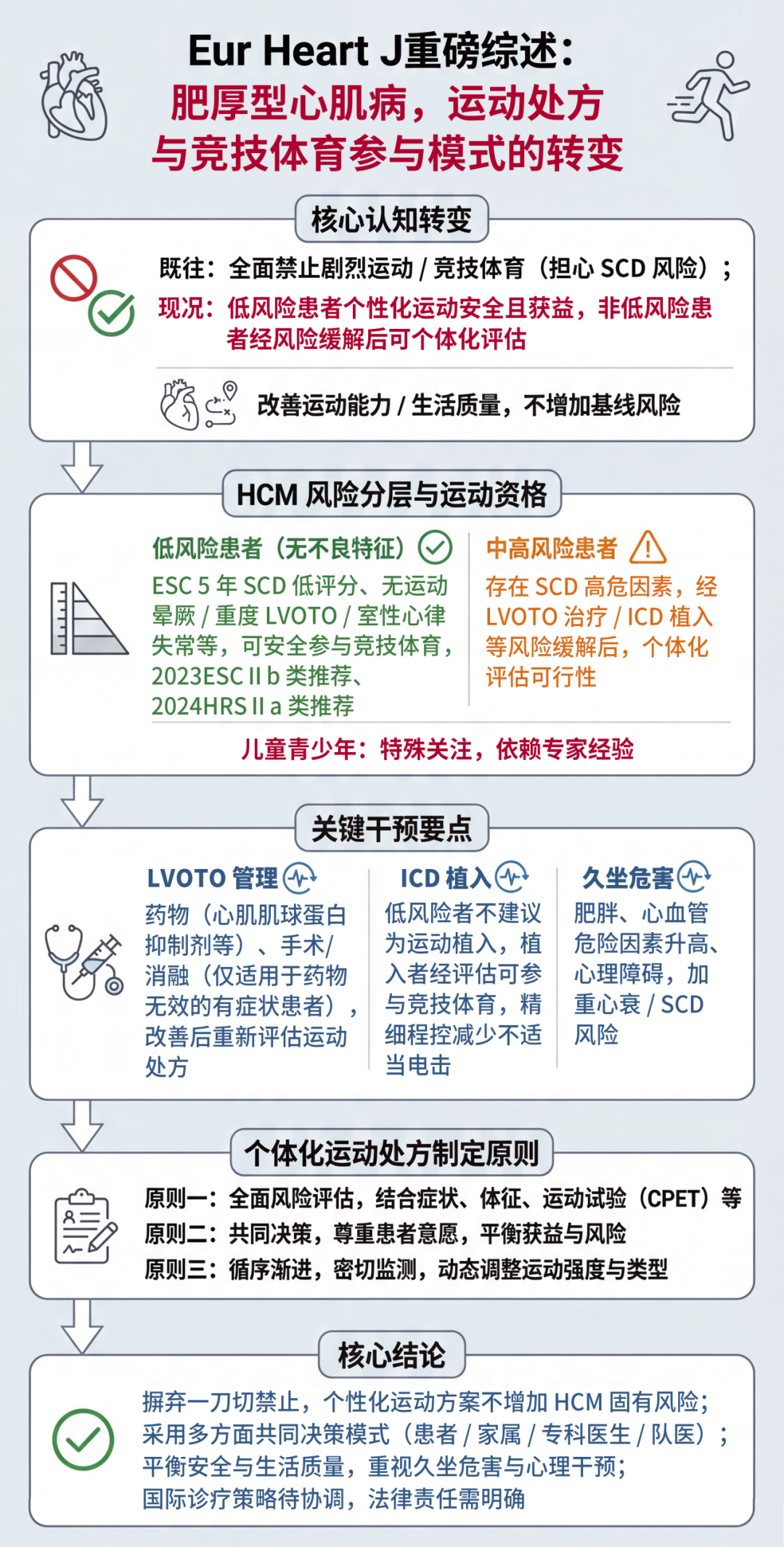
既往,因担心心源性猝死(sudden cardiac death,SCD)风险升高,肥厚型心肌病(hypertrophic cardiomyopathy,HCM)患者被全面禁止进行剧烈运动和参与竞技体育。但新的证据对这一模式提出了挑战。观察性研究和随机试验表明,为HCM患者制定个性化运动方案(包括低风险患者参与竞技体育),能改善其运动能力、生活质量,以及整体心血管和心理健康,且未出现安全风险倾向。低风险患者的定义是不具备明确的不良特征,例如较高的欧洲心脏病学会HCM SCD高风险评分、运动诱发性晕厥、严重的左心室流出道梗阻(left ventricular outflow tract obstruction,LVOTO)、室性心律失常等。尽管各国在相关法规和临床诊疗策略上存在差异,但低风险HCM患者可安全参与竞技体育这一观点,已在国际上得到广泛认可。对于未达到低风险标准的患者,相关证据仍较为有限,但在采取适当的风险缓解策略(包括必要时对流出道梗阻进行治疗、植入式心脏复律除颤器[implantable cardioverter defibrillator,ICD])后,仍可根据个体情况评估其参与竞技体育的可行性。

当代HCM的诊疗策略,应基于个体化、目标导向的运动处方,辅以多学科咨询和共同决策模式,同时兼顾医疗建议与患者的安全、价值观、健康目标及生活质量的一致性。《European Heart Journal》发表了最新重磅综述,通过审慎评价HCM患者进行剧烈运动和参与竞技体育的最新证据,探讨相关新数据如何重塑临床实践和国际诊疗指南,推动该领域诊疗模式的变革。
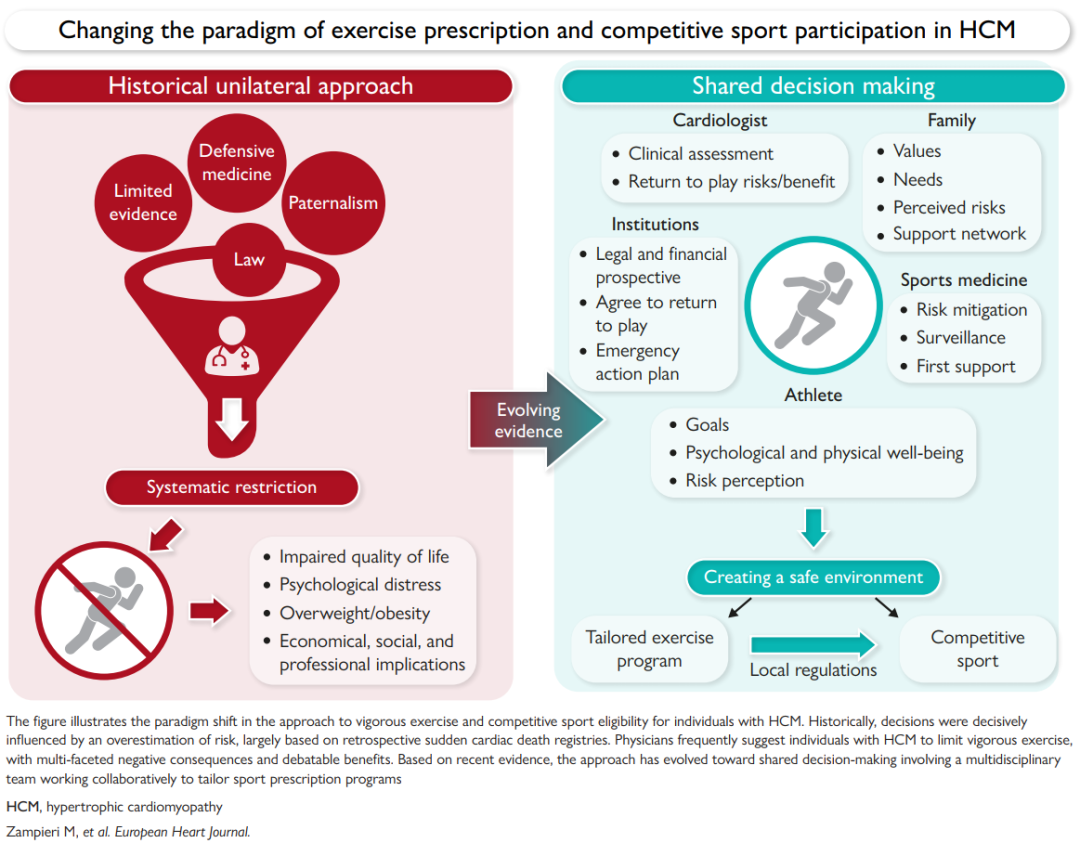
图解摘要
HCM是最常见的遗传性心肌病,以原发性心肌肥厚、室性心律失常易感性增加为特征,患者静息或运动状态下可能发生罕见的致命性心律失常事件。多数HCM患者无症状或症状轻微,且保持积极的生活方式,确诊后往往不愿放弃运动。然而,HCM患者能否安全进行剧烈运动、参与竞技体育,是近年来心血管领域最具争议且不断发展的焦点问题之一。
在缺乏可靠研究数据的时期,临床决策多依赖专家经验和主观判断,导致临床医生对HCM运动员持消极态度,并普遍禁止其参与体育活动。但越来越多的证据表明,结合患者个体特征制定运动方案,参与体育运动并不会增加HCM疾病本身的基线风险;相反,强制患者久坐不动则必然会对其健康造成损害。
本综述审慎评价HCM患者进行剧烈运动和参与竞技体育的最新证据,探讨相关新数据如何重塑临床实践和国际诊疗指南,推动该领域诊疗模式的变革。
01
历史视角
HCM确诊对运动员生活的影响,长期以来一直是临床医生关注的问题。
早在1980年,BJ Maron在首项针对年轻运动员SCD的尸检研究中,就指出HCM是首要相关病因。在29例于运动场地发生SCD的竞技运动员中,14例(48%)由HCM导致。这项里程碑式的研究及后续相关研究,将HCM与竞技体育相关的SCD高风险紧密关联。
在1980-2006年开展的一项纳入1866例竞技运动员猝死病例的大型研究中,1049例为SCD,且82%发生在训练或比赛期间,其中HCM仍是最常见病因,占比36%。
此后,多项基于尸检的回顾性登记研究进一步强化了人们对年轻运动员中HCM与心源性猝死存在关联的认知(表1),且学者们提出了多种可能的发病机制。
表1 HCM患者SCD与体力活动相关研究综述:来自SCD登记研究、回顾性队列研究、前瞻性研究和临床试验的证据
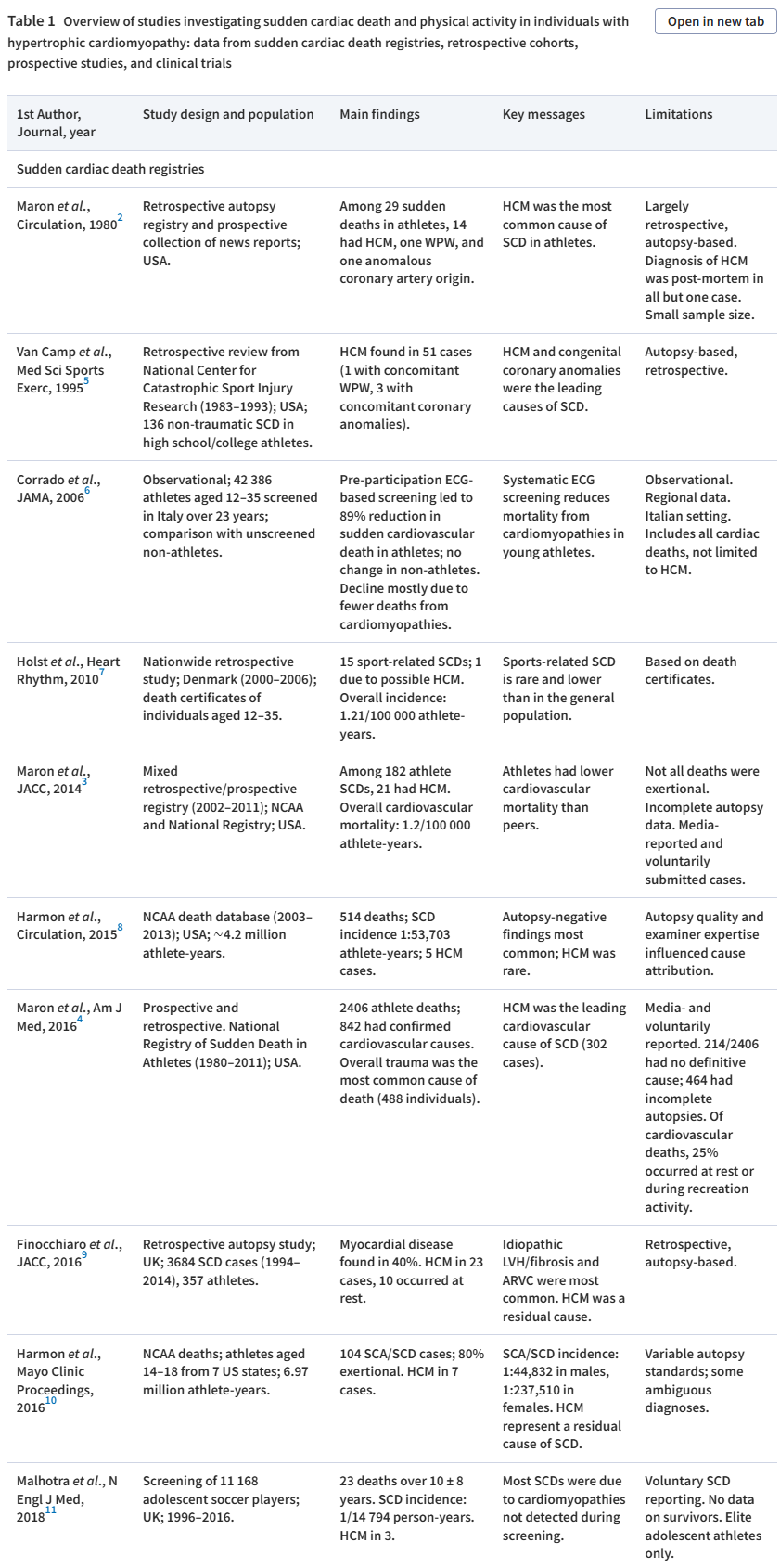
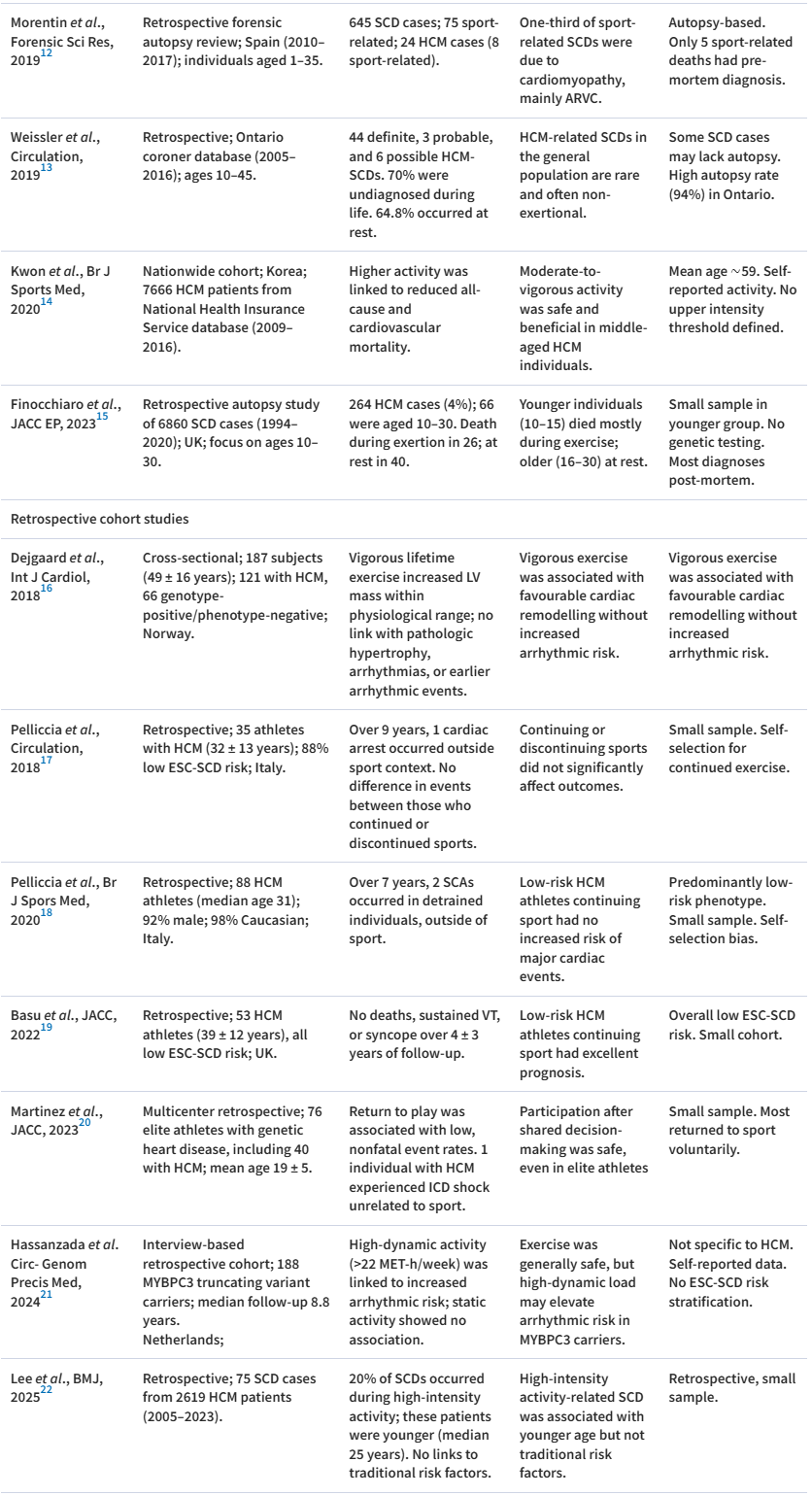

但与采用预设方案的系统性登记研究相比,尸检研究存在明显的选择偏倚;其回顾性设计也不可避免地使研究结果偏向疾病的最严重表型。此外,与年轻人SCD的其他病因相比,HCM在普通人群中的患病率相对较高,这必然会导致其相关猝死事件的绝对数高于其他疾病,进而高估了其在运动员和非运动员群体中的相对风险。
近期基于更大规模尸检登记研究(纳入青少年和儿童)的结果显示,HCM相关死亡的占比显著降低,该疾病已被归为SCD的少见病因。
尽管如此,这些早期研究的影响仍持续存在。“HCM患者进行剧烈运动、参与竞技体育存在高风险”的临床认知迅速传播并根深蒂固,加之知名运动员在重大赛事中突发SCD的个案被广泛报道,进一步强化了这一观点。
此后,多个体育联合会开始对职业运动员实施筛查项目,而运动员赛前筛查问题也在二十多年里一直是科研文献的研究热点。
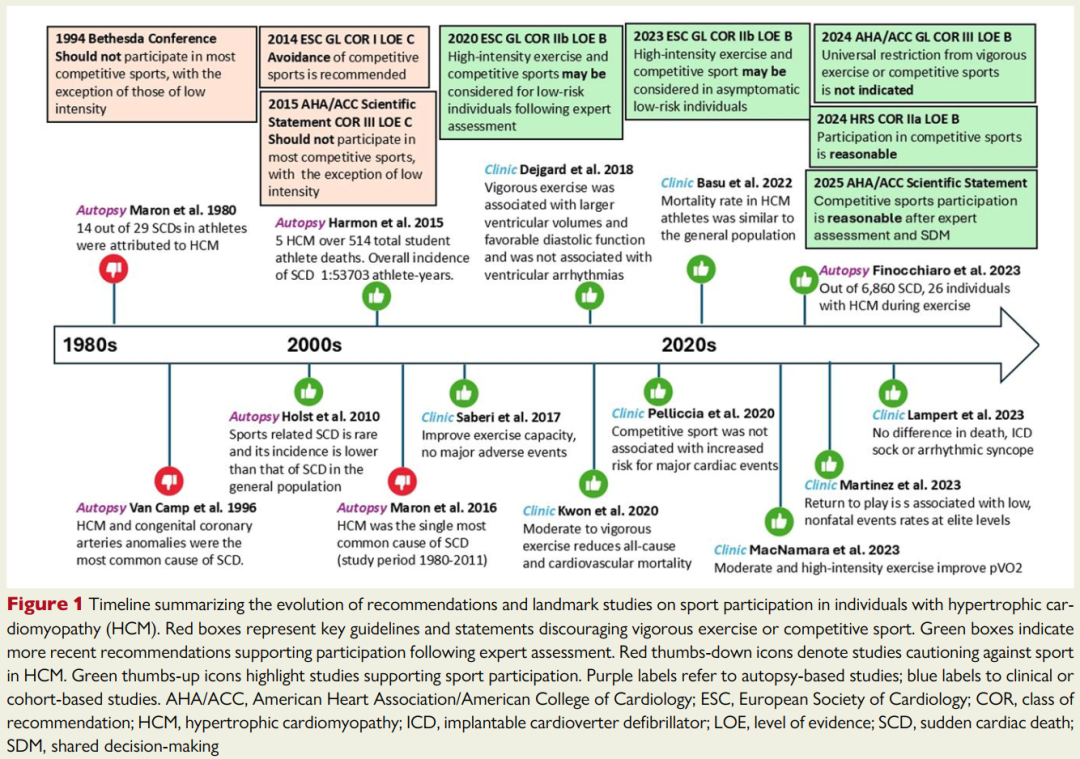
从1985年第16届Bethesda会议发布的运动员参赛资格建议开始,各科学协会就认可了所有肥厚型心肌病患者应避免剧烈运动和参与竞技体育这一原则(图1)。
该建议后来在1994年第26届和2005年第36届Bethesda会议中更新,明确指出“确诊HCM的运动员不应参与大多数竞技体育项目”;2005年欧洲心脏病学会的相关指南也呼应了这一建议。
直至2011年,美国心脏病学会基金会/美国心脏协会(ACCF/AHA)发布的HCM诊疗指南,以及2014年欧洲心脏病学会发布的HCM诊疗指南,仍反对患者参与竞技体育,并不鼓励其进行高强度体力活动(图1)。
彼时,由于缺乏可靠的风险分层标准,无法界定真正的“低风险”患者,进一步加剧了临床医生对HCM患者参与运动的消极态度。
02
证据更新与模式转变
20世纪90年代,超声心动图得到广泛应用,对门诊非选择性HCM人群的研究开始发现,该病存在轻症表型;研究显示,无主要危险因素的HCM患者,年SCD发生率仅为0.6%。
随着对HCM临床病程的认识不断深入,基于证据的有效SCD风险分层模型逐步建立。同时,医学界认识到体力活动对心理和生理健康的重要作用,推动了相关临床研究的设计和开展,以完善现有证据。尽管这些研究仍非定论,但一致表明,HCM患者参与个性化运动方案(包括剧烈运动)后,预后良好(表1)。
长期以来,临床个案显示HCM并非与体育运动完全矛盾。
1994年,BJ Maron报道了一组14例HCM患者(30-66岁),该组患者均在参与马拉松、游泳、铁人三项等耐力运动后被偶然确诊HCM;其中12例为全国级或职业级运动员,所有患者均无症状,且随访期间无疾病进展或SCD发生。
一项回顾性研究纳入了1997-2017年确诊的88例非职业HCM运动员,所有患者均规律运动「中位7小时/周(四分位距:6-14),每年运动>10个月」,其中部分患者还参与竞技体育,这与当时的主流诊疗建议相悖。中位7年随访期间,继续进行剧烈运动(≥3次/周,≥2小时/次,含高强度运动时段)的患者与停止训练的患者(<6小时/周),在症状、SCD、心搏骤停的复合终点上无差异。值得注意的是,2例心搏骤停(年发生率0.3%)均发生在停止训练的患者中,且均在非运动场景。该研究队列总体为低风险人群「中位ESC 5-year SCD风险评分2.2%(四分位距:1.7-3.0)」,仅11例患者(12.5%)为中高风险。
一项横断面研究纳入121例HCM患者,其中44例(36%)参与剧烈运动;生存分析显示,HCM运动员与非运动员的室性心律失常发生率无差异(对数秩检验P=0.36)。多变量分析校正整体纵向应变和左心室壁最大厚度后,运动员身份与室性心律失常无关联。
同样,一项回顾性研究纳入53例低风险HCM运动员(平均ESC 5-year SCD风险评分1.9%±0.9%),所有患者均继续参与竞技体育;4.5年随访期间,所有患者均无症状,且无晕厥、持续性室性心动过速或死亡病例。值得注意的是,该队列中17%为黑人运动员(通常被认为患病风险更高),且半数为职业运动员。
另一项研究纳入76例患有遗传性心脏病的大学生运动员和职业运动员,其中40例(53%)为HCM;91%的患者在接受指南指导的优化治疗(32%ICD)后,选择重返赛场。7年随访期间,仅1例运动员(1.3%)发生运动诱发的心脏不良事件,无死亡病例。
近年来,临床试验和大型前瞻性登记研究越来越多地证实,HCM患者进行中高强度运动是安全的,且可能获益(表1)。首项系统性研究为一项小样本、非随机研究,纳入有症状的HCM患者并参与心脏康复项目,结果显示患者运动能力改善、症状负担减轻,且无不良事件发生。
两项随机对照试验(包括RESET-HCM研究)表明,与常规活动相比,结构化的中等强度运动能显著改善训练组患者的峰值摄氧量(peak oxygen consumption,pVO2)、自我感知的身体活动受限程度和生活质量;尽管两项研究均未以安全性为主要终点,但均未报道严重不良事件或室性心律失常。
HIT-HCM研究进一步证实,中等强度和高强度运动训练改善pVO2的效果相当。所有受试者均先进行2个月的中等强度运动,随后被随机分为继续中等强度运动组和每周增加1-2次有监督的高强度间歇训练(HIT)组。尽管该研究受限于样本量较小,但证实了运动相关的严重心律失常或心脏不良事件风险未升高。
SAFE-HCM研究将16-60岁的HCM患者随机分为高强度运动组和常规管理组,结果显示高强度运动组患者的心肺适能、动脉粥样硬化心血管风险指标和心理评分均得到改善;尽管运动组出现心律失常,但发生率与对照组无显著差异。
多中心前瞻性LIVE-HCM登记研究纳入1660例HCM患者,对比剧烈运动组(≥6代谢当量,≥60小时/年;42%)与非剧烈运动组的预后。3年随访后,两组在死亡、SCD、适当的ICD电击、心律失常性晕厥的复合终点上无差异(4.7% vs 4.6%;HR 1.01;90% CI 0.68-1.48;P=0.98)。该研究中年轻亚组(14-22岁)样本量过小,无法进行有意义的分析,但高中和大学校队运动员的不良事件发生率,低于同龄的中等强度运动/久坐人群「5.7/1000人年(95% CI 0.8-40.8)vs 20.7/1000人年(95% CI 9-46.2)」。
ICD运动安全登记研究的结果进一步印证了运动的安全性,该研究纳入372例植入ICD的运动员(65例为HCM;13例(22%)参与高水平竞技体育)。中位31个月随访期间,无患者在运动中或运动后发生死亡或经复苏的心律失常;仅1例运动员在训练中接受了适当的ICD电击。
综合以上数据可知,结合患者个体临床特征制定运动方案,进行剧烈运动(包括竞技体育)并不会增加HCM本身的基线心律失常风险,且运动相关不良事件的绝对风险较低(图解摘要)。
03
久坐的潜在危害
HCM患者易养成久坐的生活习惯,原因包括心脏症状、自我感知的运动能力受损、对SCD的恐惧,也包括临床医生不鼓励运动,且未给出明确的推荐运动方式,或未提供任何运动建议。
美国一项全国性调查显示,HCM患者的工作或休闲活动时间显著少于普通人群,多数患者表示确诊后会刻意减少活动量。一项纳入198例在HCM专科中心接受治疗的成人患者的研究显示,通过问卷评估发现,55%的患者未达到每周150分钟中等强度运动的最低推荐量;而通过加速度计进行客观评估时,这一比例升至87%。
一项针对儿童和青少年HCM患者的多中心横断面研究显示,不足10%的患者达到每日60分钟中高强度体力活动的推荐量,75%的患者被心脏科医生限制运动。
与普通人群一样,HCM患者也易出现心血管危险因素。研究显示,超70%的HCM患者体重指数(body mass index,BMI)升高,其中半数(35%)达到肥胖诊断标准(BMI>30kg/m2)。重要的是,与非肥胖患者相比,肥胖的HCM患者发生严重功能受限的(NYHA Ⅲ/Ⅳ级)心力衰竭的风险升高2-4倍,且该风险独立于心力衰竭的其他已知决定因素。
肥胖还与左心室质量增加相关,且增加程度与肥胖程度成正比;与BMI正常的患者相比,肥胖的HCM患者左心室质量显著增加(>120g/m2)的风险升高3倍。此外,肥胖还与可诱发的LVOTO和高血压的患病率升高相关,而这两种情况又会进一步导致左心室质量增加。
久坐的生活方式会促进动脉粥样硬化危险因素的形成,而动脉粥样硬化与HCM患者的死亡率升高相关(与普通人群相比)。一项纳入425例HCM患者的研究显示,32%的白人患者和58%的黑人患者合并高血压;合并高血压的患者,心血管死亡、心搏骤停或适当的ICD治疗的复合终点风险升高2倍。当HCM患者合并冠状动脉疾病时,两种疾病的协同作用会显著升高患病风险。
最后,HCM确诊还会对患者的心理健康产生负面影响,进而影响预后,并造成显著的社会医疗成本。而禁止患者参与剧烈运动和竞技体育,会进一步加重这种负面心理影响,对于将体育运动作为生活核心甚至谋生手段的运动员而言,尤为明显。
一项针对以休闲运动为主的中老年HCM运动人群的调查显示,54%的患者难以适应运动限制,且多数患者表示运动建议模糊且相互矛盾。运动限制不仅会导致体重增加等身体变化,还会使患者产生不确定感和残疾感;既往运动水平越高的患者,心理障碍越严重。
一项研究纳入25例近期确诊心血管疾病的年轻竞技运动员(5例为HCM),结果显示,既往参与高水平竞技体育的患者,以及需要频繁关注基础疾病的患者(如每日服药、运动时监测心率),发生心理障碍的风险更高。
不足为奇的是,运动积极性高、有训练基础的HCM患者,往往会突破运动限制继续运动,以维持运动带来的益处。一项探讨该行为动机的研究显示,多数患者表示,运动能改善身心健康,且有助于维持社交关系,这是他们继续运动的主要原因。
重要的是,运动限制对患者心理健康的负面影响,可能直接影响其疾病预后。一项纳入793例HCM患者的研究显示,焦虑水平升高的患者,心力衰竭风险升高3倍,SCD风险升高1.4倍;同时合并焦虑和抑郁的患者,心力衰竭事件风险升高4倍,SCD风险升高3.5倍(与无焦虑、抑郁的患者相比)。
即使HCM患者确诊后被鼓励重返赛场或继续运动,其仍常存在心理压力,且这类压力往往未被充分认识,包括重返赛场的焦虑、运动时发生ICD电击的恐惧,或因对疾病的不确定感、运动表现的压力而形成的不良训练行为。这些因素可能影响患者对医疗建议的依从性,并导致情绪困扰。
总体而言,尽管各项研究存在方法学局限性,但上述结果强调了以下两点的重要性:一是需系统性筛查HCM患者的焦虑、抑郁症状,减少不必要的生活方式限制;二是应将积极的心理评估和及时的干预措施(如心理咨询或其他支持性措施),纳入HCM的综合诊疗中。
04
个体化风险评估与运动资格判定
对心律失常风险进行详细、多维度的评估,是HCM临床管理的基石,也是确定患者适宜运动强度的关键。事实上,对非选择性HCM人群的研究显示,剧烈运动时不良事件发生率升高,因此对于存在重度LVOTO等明确高风险特征的HCM患者,进行运动时需谨慎。
尽管风险分层工具不断完善,但在复杂、动态的生物系统中,预测罕见不良事件仍不可避免地存在不确定性。尽管欧洲心脏病学会(ESC)和美国心脏病学会基金会/美国心脏协会(AHA/ACC)的指南在风险分层模型上存在差异,但SCD的核心危险因素基本一致,包括:
①既往发生心搏骤停或持续性室性心律失常;
②年龄较小;
③有HCM相关的SCD或持续性室性心律失常家族史;
④重度左心室肥厚;
⑤显著左心房扩大;
⑥检出室性心律失常;
⑦近期有致心律失常性晕厥史;
⑧存在LVOTO;
⑨心脏磁共振成像显示广泛心肌纤维化;
⑩左心室射血分数≤50%;
⑪存在左心室心尖部室壁瘤。
无上述所有特征的患者,为低风险或极低风险HCM患者。对于存在1项及以上上述特征的患者,学者们提出了多种模型,结合感知风险为其制定运动处方、评估运动参与资格,但临床实践中,仍需结合常识和临床经验,弥补现有认知的诸多不足。表2列出了HCM患者运动时的实用风险降低建议。
表2 HCM患者的实用运动建议
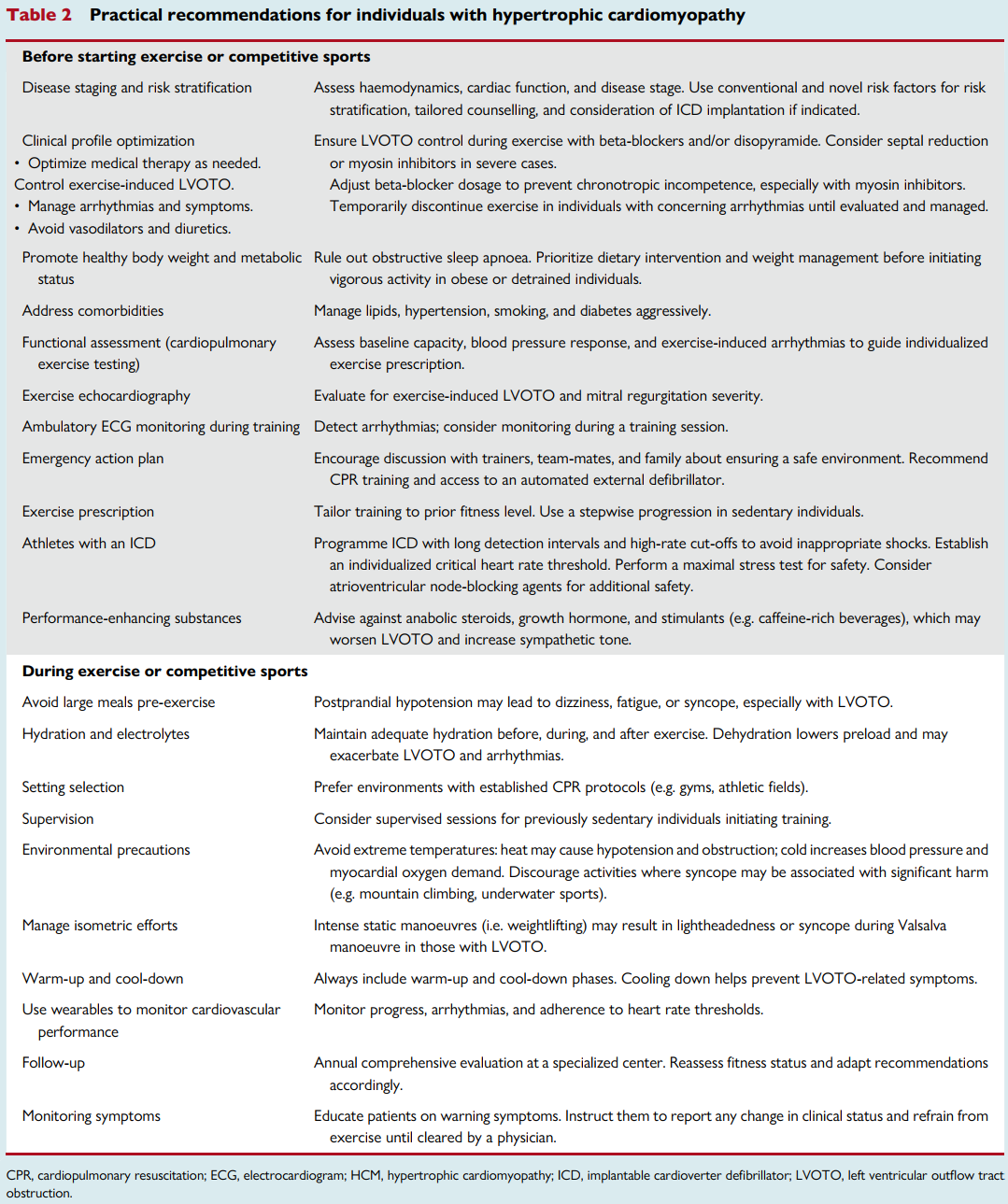
2023年ESC指南建议,无症状、低风险且心脏形态学轻度异常的HCM患者,可考虑进行剧烈运动和参与竞技体育。该建议已被多个欧洲国家采纳,并纳入各国竞技体育参赛资格的国家规程中。
与之相比,AHA/ACC指南未根据心脏形态学标准或SCD风险制定具体的运动建议;且AHA/ACC和心律学会(HRS)的科学声明均认为,HCM患者经全面的专家评估和知情共同决策后,参与竞技体育是合理的。
2024年HRS共识将HCM运动员重返赛场列为Ⅱa类推荐(“合理”),而2023年ESC指南的推荐级别则更为谨慎,为Ⅱb类(“可考虑”)。这一差异反映出,HRS认为运动带来的获益不断增加,且与有限的风险证据相平衡。
值得注意的是,AHA/ACC和ESC提出的传统SCD风险分层模型,尚未在进行剧烈运动或参与竞技体育的人群中验证,因此其对运动员的适用性受到质疑。这些风险评分模型的推导和验证队列中,患者的运动员身份尚不明确,且高强度运动人群的代表性可能不足——部分原因是既往禁止HCM患者参与体育活动。
基于此,HCM患者的剧烈运动参与决策,应在心肌病专科中心制定;这些中心需具备开展全面多学科评估、进行充分讨论和提供密切随访的专业能力。
最后,儿童和青少年患者需得到特殊关注。一方面,该年龄段人群需要规律的体力活动,以支持健康的身体发育、心理健康和社会融入;另一方面,幼年起病的HCM,往往与心律失常事件高风险相关。尽管目前已有儿科风险评分,但未纳入体力活动的强度和类型,且相关文献中的特异性证据仍有限,临床决策仍高度依赖专家经验。
05
左心室流出道梗阻(LVOTO)
临床中需重点关注的一个亚组为:无症状的梗阻性HCM运动员。
该亚组的诊疗存在独特挑战,因为目前指南推荐的治疗方案,通常仅适用于有症状的患者。但在实际临床中,许多被归为无症状的患者,其日常生活动能受限或运动诱发的症状,可能被低估。
在此背景下,全面的功能评估(包括心肺运动试验)对客观评价患者病情至关重要。此外,对于真正无症状的患者,建议其运动时遵循HCM的标准预防原则(总结见表2)。
对于无症状或无血流动力学不稳定的患者,若存在运动诱发性LVOTO,仍可考虑使用药物治疗以缓解症状。而室间隔心肌切除术或酒精室间隔消融术,仅适用于经β受体阻滞剂或丙吡胺初始药物治疗后,仍存在明确症状、客观动能受限或血流动力学不稳定(如运动诱发性晕厥、运动后低血压)的患者。
在高诊疗量医疗中心开展上述手术时,手术安全性高,且能显著、持久地缓解患者症状,表现为运动能力和pVO2的明显改善。但多数有症状的梗阻性HCM患者仅为NYHA心功能Ⅱ级,因此通常不符合有创治疗的指征,尽管其症状负担可能影响积极的生活方式。
近年来,随着药物治疗的进展,越来越多的梗阻性HCM患者能够进行剧烈运动。新上市的心肌肌球蛋白抑制剂(mavacamten、aficamten),通过抑制肌动蛋白-肌球蛋白横桥的过度形成、改善心肌过度收缩发挥作用,可降低心肌能量需求,改善舒张功能。
研究显示,心肌肌球蛋白抑制剂能显著降低左心室流出道压差,改善有症状的梗阻性HCM患者的运动指标,包括pVO2、通气效率(VE/VCO2)和运动时长。值得注意的是,对于不能耐受β受体阻滞剂或存在变时功能不全的患者,心肌肌球蛋白抑制剂可单药使用。
FOREST-HCM研究的证据表明,对心肌肌球蛋白抑制剂应答良好的患者,可考虑停用基础治疗,且不会影响治疗的安全性和有效性,这可能改善患者的运动能力,并减少多重用药。aficamten的MAPLE-HCM试验正在开展,将为该问题提供确凿证据。
但β受体阻滞剂的负面影响,并不能推广至运动员人群;事实上,低剂量β受体阻滞剂在某些情况下对运动员有益。因此,在针对运动员人群的相关数据公布前,尝试停用基础治疗(尤其是运动员患者)时应谨慎。
作为一般原则,当HCM患者在成功接受治疗(无论是手术、介入还是药物治疗)后,LVOTO得到显著改善时,可根据更新后的血流动力学和临床特征,重新评估并制定运动处方。
06
植入式心脏复律除颤器(ICD)对运动参与的影响
ICD是预防高风险患者SCD的唯一有效手段,但2024年AHA/ACC HCM指南明确建议,对于低风险的HCM患者,不应仅为了参与体育运动而植入ICD,因为这种做法可能使患者面临不必要的器械相关并发症。
尽管缺乏具体数据,但既往因认为植入ICD的患者存在潜在高风险病变,对其运动参与的建议较为严格。但ICD运动登记研究的结果显示,在竞技运动期间未出现ICD失效的情况。
因此,2024年HRS和2025年AHA/ACC的科学声明认为,因一级或二级预防植入ICD的运动员,参与竞技体育是合理的;但需通过共同决策,综合考虑患者的基础疾病、心律稳定性的全面确认结果,以及设备适当和不适当治疗的可能性。
由于从定义上讲,ICD植入者不符合低风险HCM的标准,因此这种宽松的诊疗策略尚未达成普遍共识,相关领域仍需更多研究。
07
运动处方的个体化制定、开具与监测
临床医生通过为患者制定个性化的训练方案,并进行持续监测,既能让HCM患者保持积极、有质量的生活,又能将风险降至最低(图解摘要)。在对患者进行全面的临床评估后(包括运动史、持续训练情况、运动超声心动图和心肺运动试验),制定结构合理的训练方案时,应遵循以下原则:
个体化:运动方案需根据患者的运动能力、症状负担和风险特征制定。有训练基础的患者起点更高,通常可继续进行剧烈运动;而久坐、超重和/或合并代谢性疾病的患者,应从中等强度运动开始,而非高强度运动,且这一初始方案并不排除患者后续参与更高强度运动的可能性。高风险患者应接受更保守的运动建议,必要时可能需要暂停训练以优化治疗。需对ICD进行精细程控,包括设置更高的频率检测区间,以减少窦性心动过速引发的不适当电击(表2)。尽管为防止器械损伤,建议患者避免接触性运动,但经适当调整(如使用防护装备)后,部分患者仍可参与。
运动强度:可通过Borg量表、最大心率百分比、心率储备、pVO2确定运动强度,并通过心肺运动试验计算有氧和无氧阈值。利用这些参数制定个体化运动处方时,需考虑治疗(尤其是β受体阻滞剂)的影响。对接受心肺运动试验的患者,可将其个体通气阈值对应的心率,作为有氧运动强度的客观指标(通气阈值1为乳酸开始堆积的节点,通气阈值2为运动诱发性代谢性酸中毒开始的节点)。值得注意的是,对于以减重、改善代谢状态和养成健康生活方式为目标的多数患者,中等强度运动比高强度运动的获益更大。
运动场所:HCM患者应在舒适的环境中运动,且无论运动强度如何,均需了解特定环境的风险,在偏远地区进行的单人耐力活动、登山、水下运动(实用建议见表2)。
运动强度渐进性:对于无训练基础的患者,中等强度的有氧运动能有效改善心肺适能、降低心血管风险;同时也应鼓励患者进行抗阻训练,初始抗阻强度为最大重复次数的40%-70%,从1-3组、每组8-10个抗阻动作开始,动作速度为慢至中等,随后根据身体适应情况每周逐步增加。训练的频率、时长和强度,应根据患者的年龄、个体反应、既往训练情况、药物治疗调整和临床特征逐步增加。
长期监测:进行剧烈运动或参与竞技体育的HCM患者,建议每年重新评估一次,或在临床需要时可增加评估频率;评估内容包括症状复查、静息和/或负荷超声心动图、运动试验(优选心肺运动试验),以及在典型训练时段进行动态心律失常监测。若患者新发高风险特征(如运动诱发性室性心律失常、显著LVOTO),应进行详细的重新评估,并通过共同决策重新判定其运动参与资格。这种结构化、定期的评估方式,有助于及时调整诊疗方案,保障运动员的安全。
可穿戴技术:能在运动时监测心率和心律的可穿戴设备,可提供实时反馈,提升运动的安全性和有效性。让患者使用可穿戴设备,能使其在安全运动的同时,深入了解自身的心血管健康状况。但需认识到可穿戴设备的潜在局限性,且患者需接受专业咨询。
多学科协作:为HCM患者制定运动处方,通常需要多学科专家团队的参与。但即使在大型HCM中心,运动心脏病学方面的专业知识也并非总能获取,可能需要运动医学医师、运动生理学家等专业人员的外部支持。多学科团队应包含心理支持人员,因为运动相关的焦虑或恐惧在HCM患者中较为常见,且已被证实是该人群不敢运动的重要原因。

07
结论
在临床实践中,已不再能一概而论地禁止HCM患者参与体育运动。尽管无论何种临床评估,都无法保证零风险,但最新证据表明,制定个性化的运动方案(包括参与竞技体育),并不会增加HCM本身的固有风险(通常较低)。
既往临床医生单方面决定运动员是否能参与运动的家长式诊疗模式,正逐步被更精细化的共同决策模式取代;即在充分告知病情后,由运动员、家属、医疗机构、心肌病专家和队医等所有相关方共同参与决策。
这种模式能结合患者的个人偏好、感到的知风险及后果、身心发育、职业发展意愿,以及经济或法律因素,做出最终决策。共同决策已被纳入临床指南,被认为是一种平衡、全面的诊疗方式,能减少决策冲突,尽管该模式仍存在潜在挑战和局限性。
尽管安全性和SCD预防仍是首要目标,但在决策过程中,也应仔细权衡并考虑禁止患者参与体育运动的潜在危害。最新证据表明,在心肌病专科中心实施共同决策,结合适当的风险分层和随访,能降低心脏不良事件的发生率。此外,共同决策已成为ICD、LVOTO的手术与药物治疗,以及晚期心力衰竭治疗方案管理流程的重要组成部分。
尽管取得了显著进展,但该领域仍面临重大挑战。具体而言,运动员被批准参与运动后发生不良事件,相关的法律责任认定在不同国家存在差异。部分国家不认可共同决策模式,且运动员的参赛资格由相关管理机构制定的法律和政策框架决定。
共同决策与监管框架之间的这种相互作用,使参赛资格判定变得尤为复杂,并导致在国际上HCM患者重返赛场的诊疗策略缺乏公平性。因此,协调各国不同的诊疗策略,是该领域未来的重要目标。