

复旦大学附属中山医院心内科黄浙勇教授
思辨介入困境
解析手术技巧
梳理中山经验
助您从新手变“心”手
每月15日、30日,严道医声独家发布
孤立性分支开口病变(Medina 0,0,1)的处理目标:既要充分覆盖分支开口病变,又要最大限度避免主支损伤。微突法支架保证了分支开口完全覆盖,却毫无悬念的带来另外二个跷跷板问题:支架突出至主支(支架冗余)和斑块/脊移位。理论上,DK-Crush似乎可以完美化解这二个问题:“Crush”可以挤压冗余支架,使其分布于分支开口四周;“DK” (二次对吻)可以矫正脊移位和斑块移位。基于此逻辑,2023 年 Acar 等提出 OSDOKINA 术式(One-Stent Double-Kissing Nano Crush Technique),即“单支架 DK 微挤压技术”,试图在不植入主支支架的前提下,实现类似 DK-Crush 的几何优势[1]。
本文并不推荐 OSDOKINA 术式作为常规策略。通过对其操作流程进行批判性剖析,旨在帮助术者重新审视:在分支病变处理中,技术复杂化是否真的带来临床获益,抑或只是对理想几何结构的过度追求。
一
OSDOKINA术式的操作流程
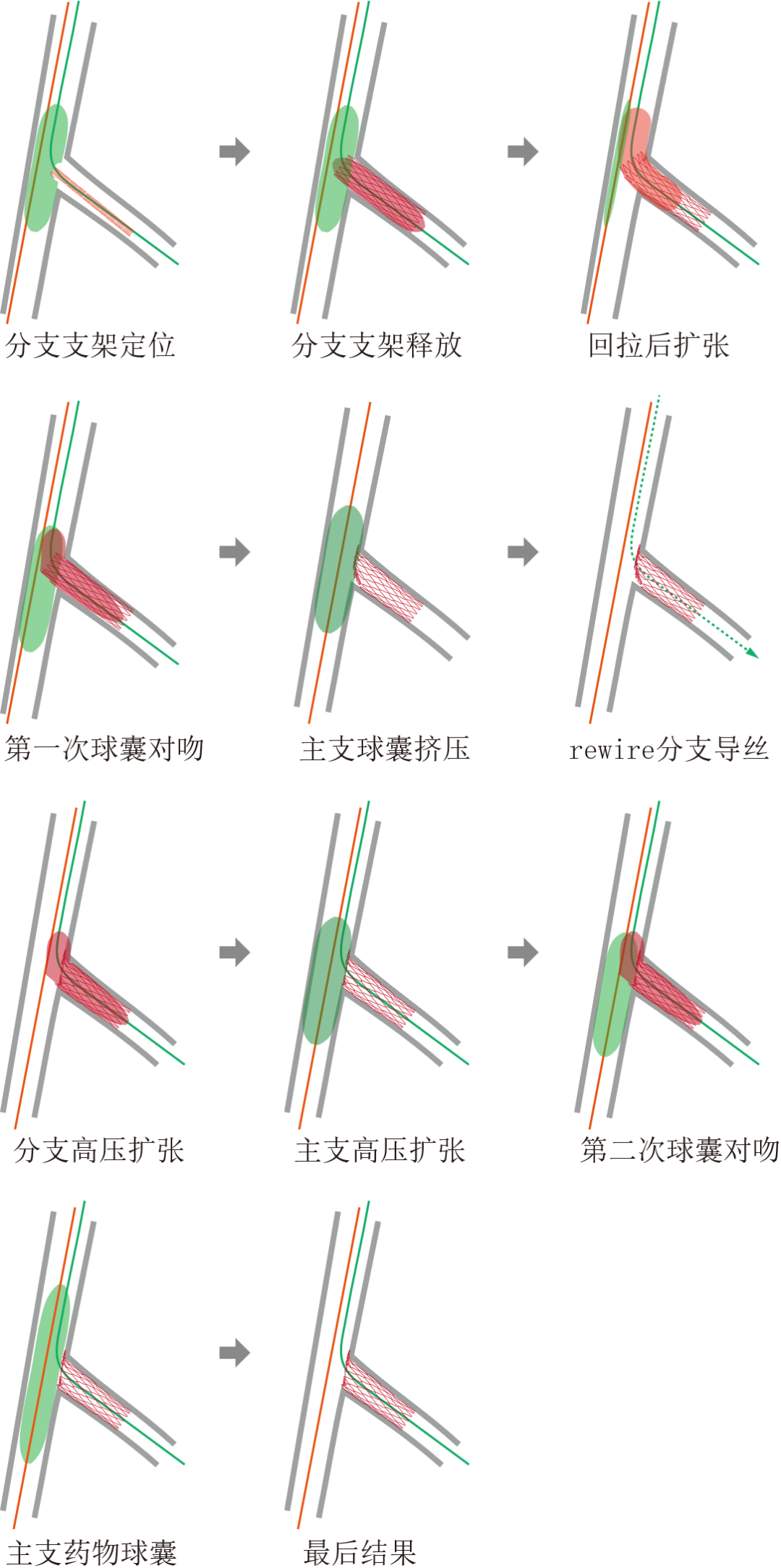
图1 OSDOKINA术式操作步骤
OSDOKINA术式操作步骤高度模拟 mini-crush 双支架技术,区别仅在于未植入主支支架。
1、预处理。主支和分支送入导丝,分支开口病变球囊预处理。
2、支架置入。分支支架(直径比1:1)和主支球囊(直径比也是1:1)就位,主支球囊于分叉口以命名压充盈,同时回撤分支支架齐平分支开口,齐平的标准是主支充盈球囊出现凹痕,此时释放分支支架。支架球囊部分回撤(一半支架内一半支架外),然后高压扩张(命名压+4atm),完成近端支架优化(图2)。
解析:主支球囊辅助是一种粗糙的开口定位技术,不同的回拉力度可产生精确定位、微突、微凹等不同结局,重复性与可控性有限。
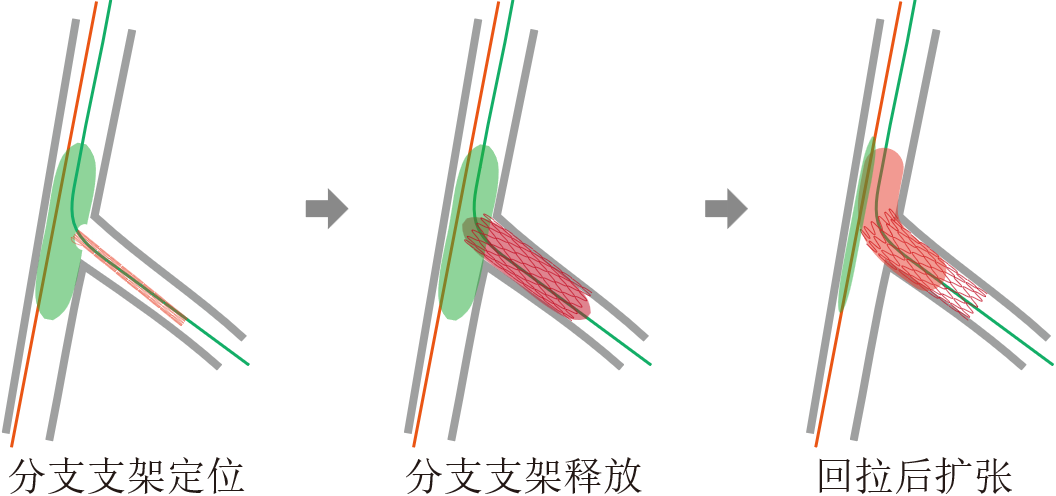
图2 主支球囊辅助下,分支支架植入
3、第一次对吻。分支支架球囊和主支球囊以命名压完成第一次球囊对吻。撤离分支支架球囊,主支球囊高压扩张(命名压+4atm),完成对分支支架开口的挤压(nano-crush)。随后重置分支导丝(图3)。
解析:(1)第一次对吻的目的是优化分支口支架梁分布,确保血管脊有支架梁分布紧贴,从而利于导丝重置。如省略对吻步骤直接进行主支球囊crush,血管脊部位可能缺乏支架梁覆盖。(2)如何保证重置?命名nano-crush也好,mini-crush也罢,微突支架突出并不多,Crush后导丝重置很难保证通过网孔。突出越少,越容易再次进入支架真腔,因此有可能无意间做成T术式,无妨。
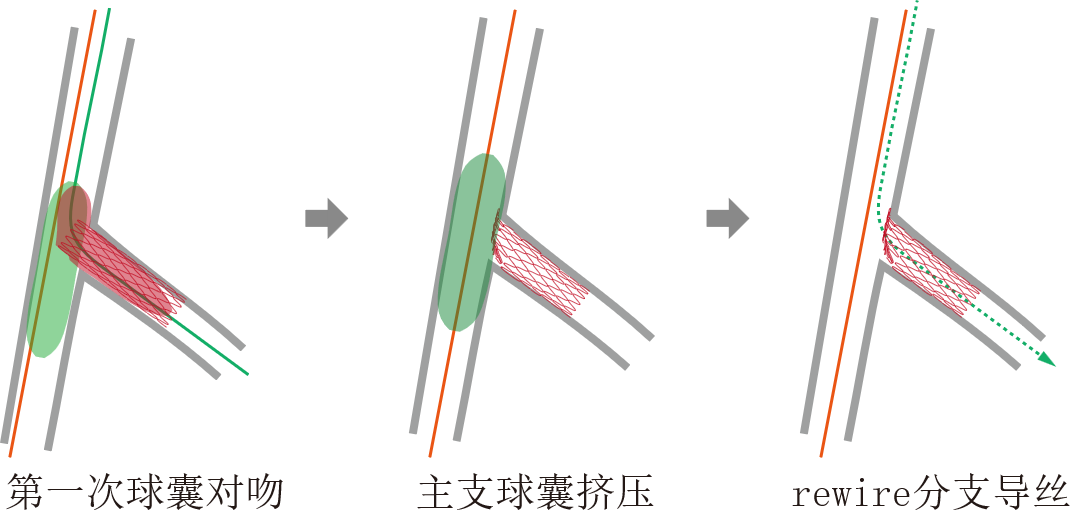 图3 第一次KBI,挤压边支支架
图3 第一次KBI,挤压边支支架
4、第二次对吻。采用非顺应性NC球囊(直径比为1:1),以命名压 +4 atm 分别高压扩张分支与主支,随后以命名压完成第二次对吻(图 4)。
解析:等直径球囊高压扩张(命名压+4atm)支架没问题,但对不准备支架的主支血管进行高压扩张,其合理性值得商榷。试想,在 DCB 治疗策略中,通常并不推荐等直径高压预处理。
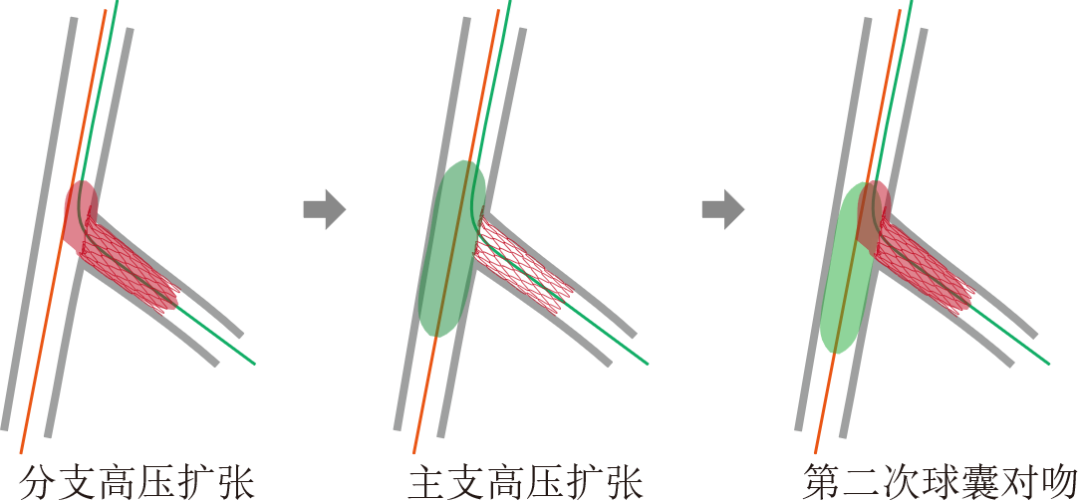
图4 第二次KBI
5、主支药物球囊。撤离两球囊,主支行药物球囊扩张(直径比为1:1,14 atm×90 s)(图5)。
解析:主支血管直径越大,对缺血越不耐受,90 秒的持续阻断在现实临床中并不总是可行。
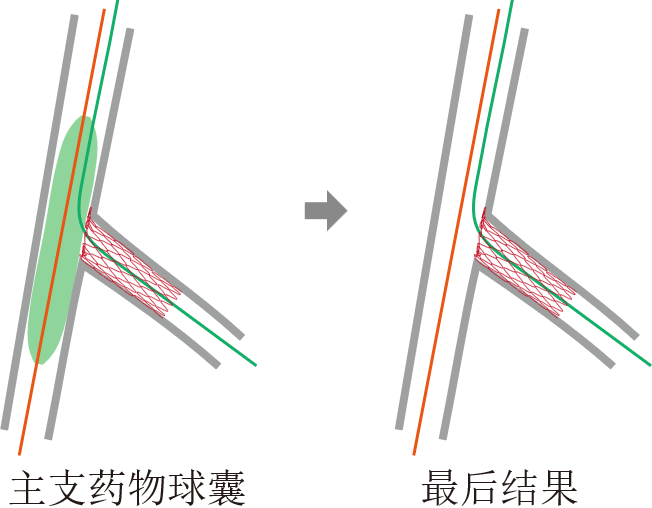
图5 主支药物球囊
二
OSDOKINA术式的应用案例(图6)
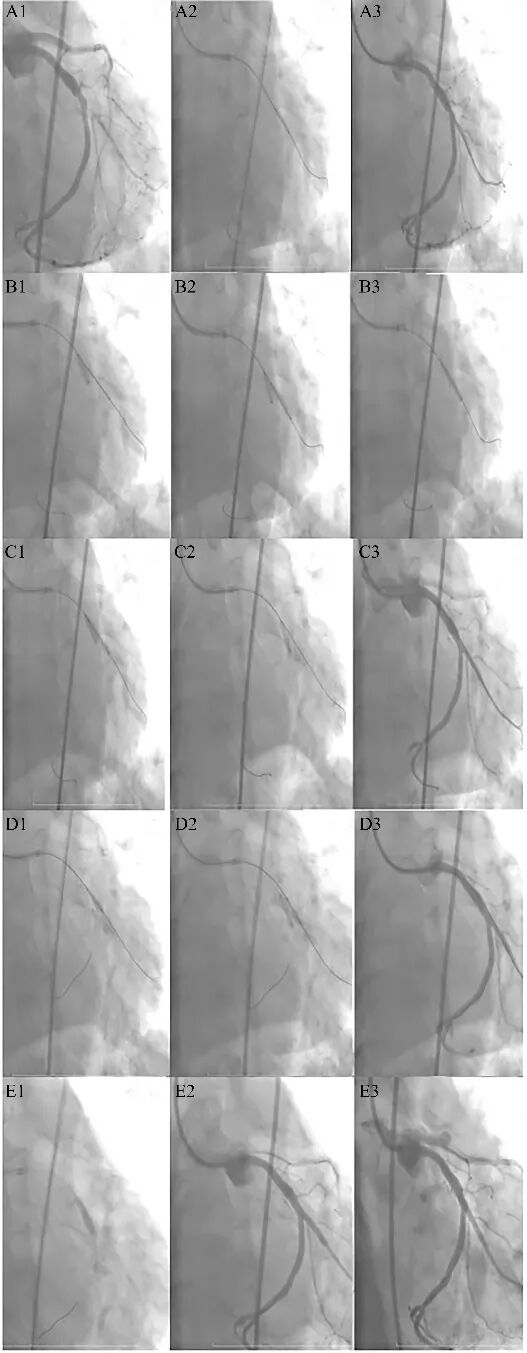 图6 OSDOKINA CRUSH技术处理钝缘支开口病变[1]。
图6 OSDOKINA CRUSH技术处理钝缘支开口病变[1]。
1、预处理(A):第二钝缘支(OM2)开口狭窄 98%(A1),2.5 × 12 mm 球囊预扩张(A2),预处理充分(A3)。
2、释放支架(B):回旋支3.5 × 12 mm非顺应性球囊12 atm扩张(B1),然后OM2内支架回撤至开口对回旋支球囊产生压痕,支架以12 atm释放(B2),稍回撤支架球囊以16 atm对近半段支架进行塑形(B3)。
3、第一次对吻(C):分支支架球囊和主支球囊以12 atm完成第一次球囊对吻(C1)。撤离分支支架球囊,主支球囊14 atm对OM2支架开口进行挤压(nano-crush)(C2)。
4、第二次对吻(D): OM2支架进行重置导丝,然后分阶段对吻:OM2采用2.75 × 15 mm非顺应性球囊 18 atm后扩张(D1),然后主支采用3.5 × 12 mm 非顺应性球囊12 atm扩张,最后12atm完场第二次对吻(D2),造影未见明显夹层(D3)。
5、主支药球(E):主支采用4.0 × 16 mm药物球囊14 atm *90秒扩张,防止再狭窄(E1)。造影检查主支无夹层和血栓形成(E2-E3)。
三
OSDOKINA术式的优缺点
OSDOKINA术式并无惊艳之处,只是一种试图通过复杂化操作来追求几何完美化的尝试[2]。理论上存在如下优点:
(1)完全覆盖。支架微突技术可避免分支开口覆盖不足,OSDOKINA 属于该范畴。
(2)轻微突出。支架在保证完全覆盖分支开口病变的基础上,只有少量支架梁突入主支(nano-protruding)。
(3)球囊对吻,避免脊移位和斑块移位。
(4)主支药物球囊处理,期望缓解主支4次球囊扩张可能导致的内膜损伤。
但事实上,OSDOKINA术式可能是一种繁复的、“因小失大”的术式:
(1)不安全。分支开口病变处理的核心风险是主支损伤。OSDOKINA挤压技术中,主支球囊扩张多达4次,包括支架定位、第一次对吻、挤压、第二次对吻,因此存在主支损伤的高度危险。补救措施仅仅是DCB(不植入主支支架),其安全性和可靠性存疑。
(2)太复杂。OSDOKINA术式基本模拟了DK-Crush双支架的技术步骤,可分解为13个步骤,复杂度明显高于 Szabo 技术或单支架跨越策略。同时,需使用预扩张球囊、高压球囊、药物球囊等诸多耗材,是一种费时、费钱、费力的术式。
因此,对于孤立性分支开口病变,我们仍然强调“简单化”处理原则,不得已时才“由简入繁”!OSDOKINA 术式提供了一种有趣的思路,但其复杂性与潜在风险并未被明确的临床获益所抵消,不宜作为常规推荐策略。
参考文献:
1. Acar, E., Y. Gunes, I.A. Izgi, et al., One-Stent Double-Kissing Nano Crush- Osdokina Crush-Technique Could be a Game- Changer in the Treatment of Medina 0.0.1 Lesion. Anatol J Cardiol, 2023. 27(7): p. 432–435.
2. Acar, E., Y. Gunes, I.A. Izgi, et al., Reply to Letter to the Editor: 'Pros and Cons of a Novel Coronary Stenting Technique for Medina 0.0.1 Lesions: Osdokina Crush'. Anatol J Cardiol, 2023. 27(9): p. 554–555.
“中山PCI解码”下期预告
心肌壁内血肿的发生和后果
心肌壁内血肿(Intramyocardial Hematoma,IMH)指血液进入心肌内形成夹层和局灶样血肿。属于急性心肌梗死或冠脉介入的一种罕并发症,可以理解为心脏破裂前状态的一种机械并发症:撕而不破!


