
重要性
免疫检查点抑制剂(ICI)治疗的应用改善了癌症患者的预后,但也带来了免疫系统相关不良反应。其中,心血管(CV)毒性反应,尤其是心肌炎,备受关注,也是本次国际心脏肿瘤学会联合肿瘤学、血液学和心脏病学领域专家发布本立场声明的核心议题。
研究发现
ICI治疗相关的心血管毒性反应包括心肌炎、心包炎、血管炎等炎症相关性疾病,也会加重动脉粥样硬化等慢性疾病并引发急性缺血性并发症(心肌梗死、脑卒中)。接受ICI治疗的患者还可能出现心肌无炎症细胞浸润的心脏功能障碍、应激性心肌病(章鱼壶型心肌病/心尖球囊综合征)和心力衰竭。
全身性炎症、心肌炎或缺血状态下,患者可能出现房性和室性心律失常。在所有潜在的心血管不良反应中,心肌炎仍是最受关注的类型,尽管其死亡率随疾病表现谱的拓宽呈下降趋势,临床表现从意义未明的肌钙蛋白升高,到隐匿性、非重症型,再到重症或暴发性心肌炎不等。
结论与意义
心肌炎仍是接受ICI治疗患者心血管毒性反应中最主要的问题,其治疗方案需根据病情严重程度制定。多学科协作是处理急性毒性反应、制定后续癌症治疗方案(包括ICI再次使用)的关键。缺血性心脏病是此类患者的主要鉴别诊断疾病,同时可能合并心包炎,房性和室性心律失常也会使临床情况复杂化。目前该领域仍存在诸多认知空白,亟待进一步研究。

过去十年,癌症诊疗领域发展迅速,免疫检查点抑制剂(ICI)的广泛应用做出了变革性贡献。ICI带来获益的同时,也存在免疫相关不良反应(irAE)的风险,这类反应可累及全身任一器官系统,甚至危及生命。
总体而言,irAE的死亡率从2016年前的14%降至2021-2022年的7.3%。
这一下降趋势也体现在ICI相关心肌炎中,同期其死亡率从45.5%降至23%,但心肌炎仍是致死率最高的irAE,也是临床最需重视的类型之一。
单药ICI治疗相关心肌炎的发生率约为0.75%,联合ICI治疗的发生率为1%~2%。
其他心血管并发症的发生率更高,其中心包炎患病率为0.55%(95% CI:0.21~1.41)、心血管死亡患病率为0.67%(95% CI:0.21~2.09)、传导障碍患病率为0.85%(95% CI:0.14~5.05)、急性冠脉综合征(ACS)患病率为1.73%(95% CI:0.81~3.70)、脑卒中患病率为2.17%(95% CI:1.35~3.47)、快速性心律失常患病率为3.15%(95% CI:1.60~6.22)、心力衰竭(HF)患病率为3.40%(95% CI:1.52~7.61)、心包积液患病率为3.98%(95% CI:0.54~29.60)。有研究报道ICI治疗患者可出现血管炎和血栓栓塞,但相关风险评估尚无明确数据。
本跨学科国际立场声明由国际心脏肿瘤学会(IC-OS)牵头制定,总结了目前对ICI治疗相关心血管毒性反应的认知(图1),包括推荐的诊断、治疗和潜在再次用药策略,并梳理了该领域的相关认知空白。
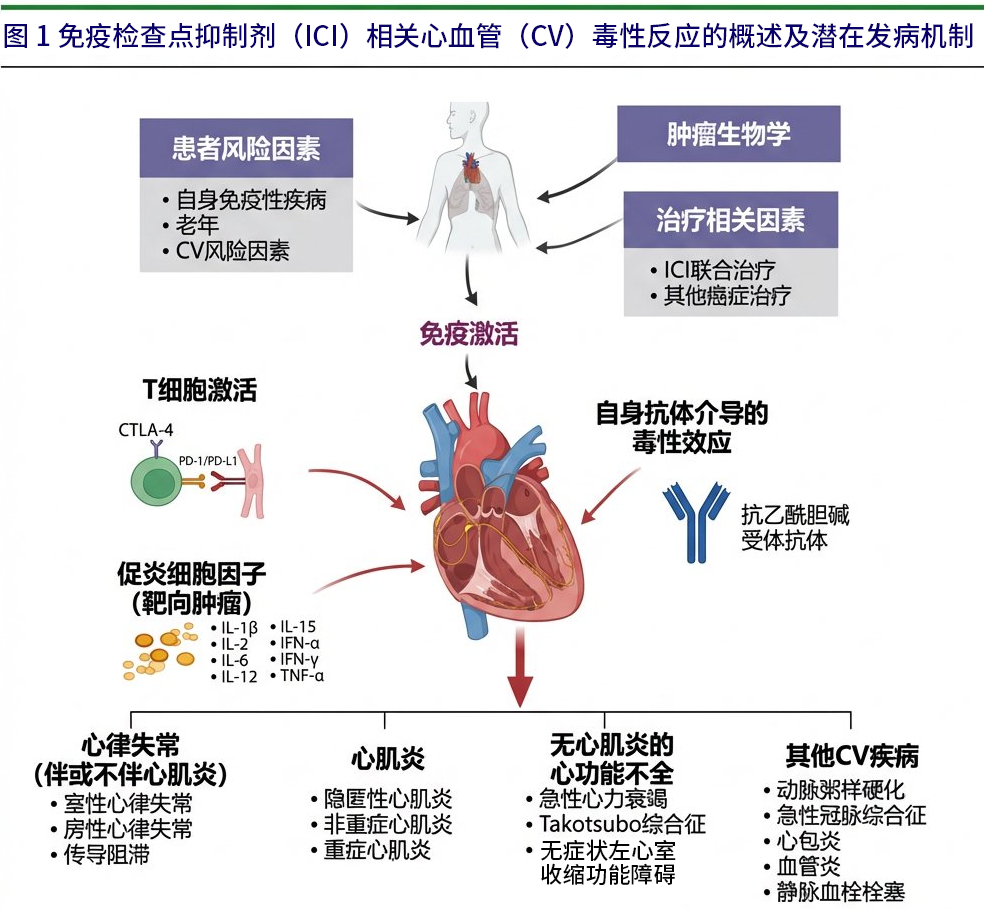
图1免疫检查点抑制剂(ICI)相关心血管(CV)毒性反应的概述及潜在发病机制
01
危险因素与病理生理学
双联ICI治疗是ICI相关心肌炎风险升高的明确危险因素,部分数据显示,ICI与酪氨酸激酶抑制剂联用时,心肌炎风险也会增加。
与其他癌症类型相比,黑色素瘤患者发生ICI相关心肌炎的风险更高;胸腺上皮肿瘤患者,尤其是放射病理学分型高级别的患者,风险最高(较其他癌症高10~30倍),且预后更差。
抗乙酰胆碱受体自身抗体阳性会使ICI相关心肌炎风险升高5倍以上,还会使重症心脏和呼吸肌衰竭的风险翻倍,这也凸显了胸腺相关自身免疫反应的作用。其他危险因素包括重症肌无力病史、自身免疫病史和高龄(75岁及以上)。既往存在心血管疾病及心血管危险因素(包括冠脉和主动脉钙化证据)的患者,接受ICI治疗后发生心肌炎等心血管事件的风险更高。
02
临床特征
临床表现
心肌炎的严重程度从隐匿性到暴发性不等。多数患者表现为胸痛、乏力、呼吸困难、心悸等轻微症状,尽管心内膜心肌活检(EMB)或心脏磁共振成像(CMR)可检出明显的心肌炎症,但LVEF多保持正常。
此类情况下,心肌生物标志物和心电图(ECG)的敏感性更高,且比超声心动图更具预后价值。
识别肝炎、肌炎、类重症肌无力综合征等合并综合征至关重要;反之,对于出现肌肉无力、肌痛、上睑下垂、复视或视力模糊的患者,若检出异常,需立即行心电图检查、评估心肌生物标志物,并及时开展心肌炎的进一步诊断性检查。
无论是否合并心肌炎,患者均可能出现新发传导异常(房室传导阻滞、束支传导阻滞)或心律失常(心房颤动/扑动、室性异位搏动、非持续性和持续性室性心动过速,甚至心室颤动)。对于出现严重传导障碍或心律失常的患者,需考虑心肌炎的可能。
非炎症性心力衰竭通常出现在治疗后期,在既往存在心血管疾病的患者中更常见,其诊断和治疗策略与经典心力衰竭相似,但需排除心肌炎和章鱼壶型心肌病。
ICI诱导的全身性和血管炎症会加速动脉粥样硬化,进而引发急性冠脉综合征、脑卒中等血管相关并发症。接受ICI治疗的患者,免疫介导性心包炎的发生风险也会升高,可合并或不合并心肌炎;心包炎多为晚期心血管事件,极少引发心脏压塞。
事件定义
心血管事件的定义遵循目前公认的急性冠脉综合征、心力衰竭、血栓栓塞相关指南和临床实践模式。
根据国际心脏肿瘤学会的共识标准(已纳入欧洲心脏病学会心脏肿瘤学指南),ICI相关心肌炎的诊断可通过病理检查确诊,或结合临床表现确诊:心肌肌钙蛋白(cTn)较基线新发明显升高,且满足以下任一条件——(1)心脏磁共振成像检查结果符合心肌炎诊断;(2)至少满足2项临床、心电图或影像学次要标准。
ICI相关心肌炎可进一步分为隐匿性、非重症型和重症(暴发性)型。需着重强调的是,急性冠脉综合征作为主要鉴别诊断,需快速明确诊断,且需知晓心肌炎与急性冠脉综合征可同时发生。由于心肌炎可危及生命,国际心脏肿瘤学会的共识定义在兼顾敏感性和特异性的同时,将乏力、肌肉无力等特异性较低的临床症状纳入次要标准。
研究显示,将发病时间限定为启动ICI治疗后3个月内、次要标准数量从2项增至3项,可使诊断特异性从70%提升至83%,同时维持93%的敏感性。鉴于诊断对临床的影响及对癌症治疗方案的决定作用,在具备相应专业能力的中心,应尽可能通过心脏磁共振成像或活检确诊ICI相关心肌炎。
除已确立的心血管事件诊断标准外,部分患者会出现意义未明的肌钙蛋白升高(约10%~15%的ICI治疗患者)(图2)。此类情况的难点在于明确肌钙蛋白升高的发病时间、病因和临床意义。尽管有时无法明确具体病因,但需全面排查其他致肌钙蛋白升高的原因,包括急性冠脉综合征、章鱼壶型心肌病、心力衰竭、肺栓塞、肾功能不全、胃肠道出血、呼吸系统疾病、甲状腺疾病、脓毒症、神经系统事件,甚至无心肌炎的ICI相关肌炎和心肌转移瘤。
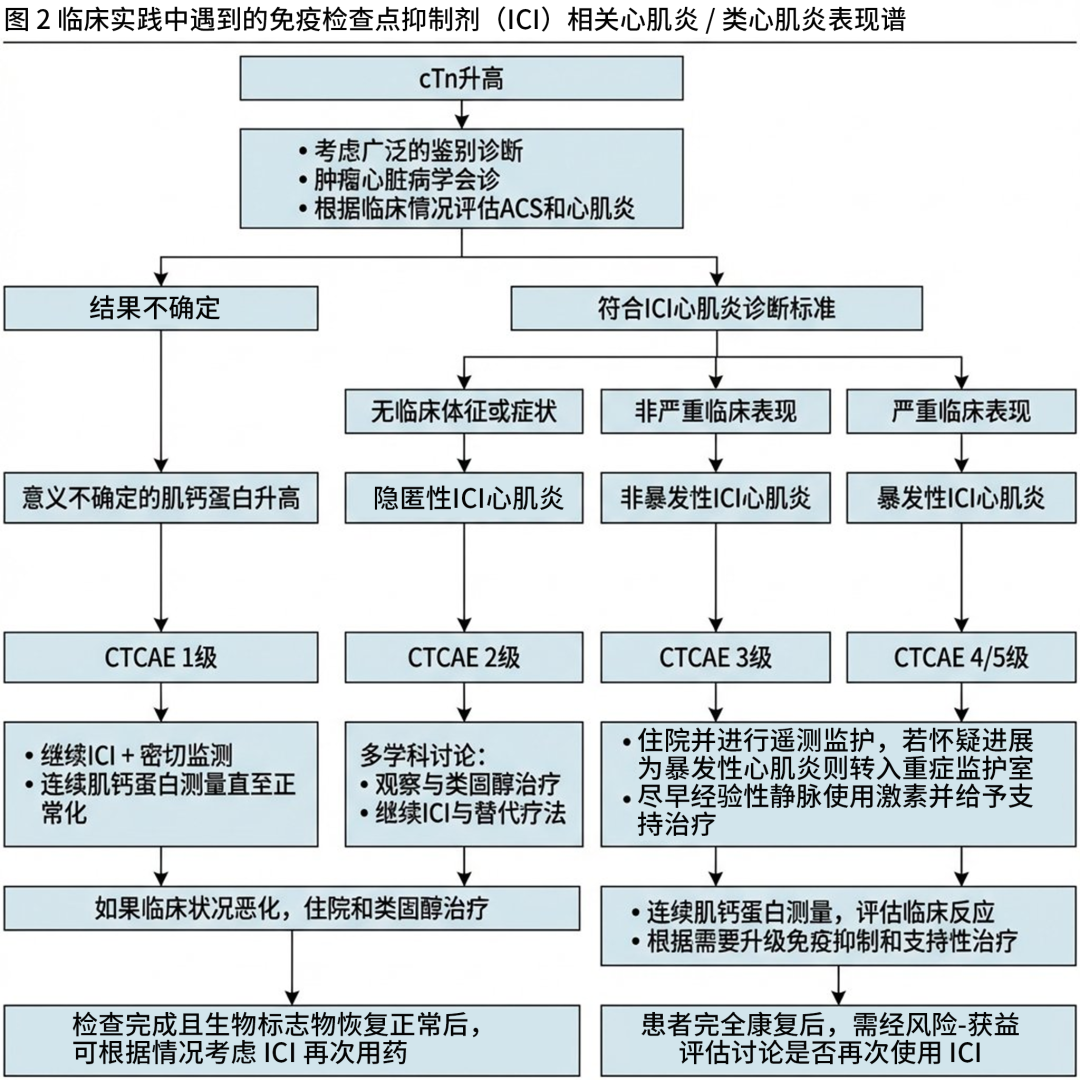
图2临床实践中遇到的免疫检查点抑制剂(ICI)相关心肌炎/类心肌炎表现谱
诊断评估
识别ICI治疗相关的心血管疾病,需结合临床怀疑并进行细致的评估,通常需采用多模态检查(表)。解读肌钙蛋白升高结果时,除结合临床表现外,还需关注其较基线的动态变化(图2)。与超声心动图类似,心脏磁共振成像的应变异常并非心肌炎的特异性表现,但与晚期钆增强相关,可能早于LVEF的变化,且具有预后价值。
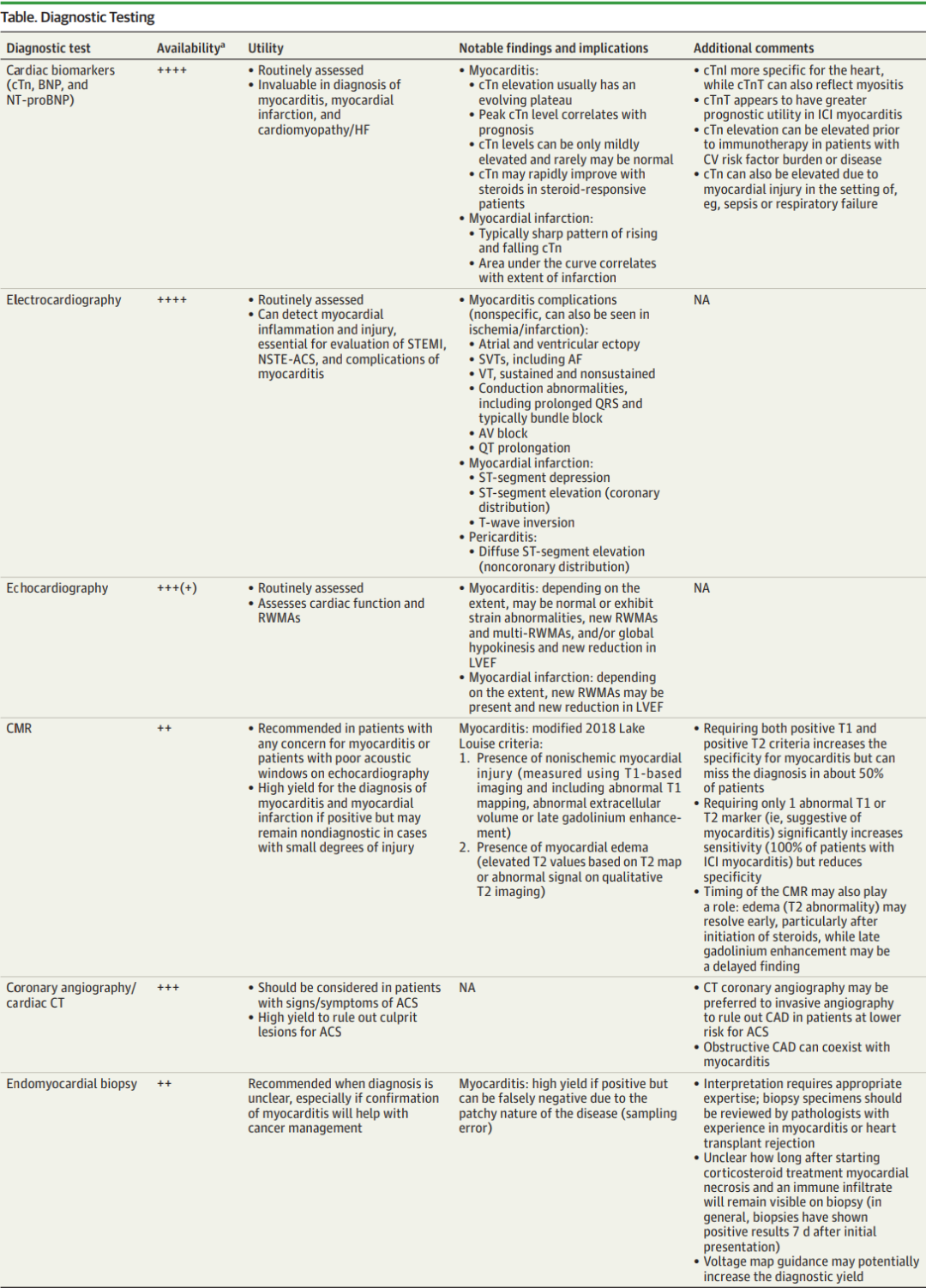

心脏磁共振成像的检查时机对心肌炎诊断的敏感性和特异性有影响,例如入院4天内检查的晚期钆增强阳性率为22%,4天后检查的阳性率为72%。
需明确的是,无任何单一的临床或影像学表现为ICI相关心肌炎所特有,这些异常也可见于其他多种心血管疾病,诊断需结合相应的临床背景。若需快速明确临床诊断,或无创评估后诊断仍不明,心内膜心肌活检可有帮助;若需组织学确诊或对心肌炎进行病理严重程度分级,以制定后续癌症治疗方案,该检查也具有价值,尤其是心脏磁共振成像结果不具特异性时。
筛查与监测
2022年欧洲心脏病学会心脏肿瘤学指南给出I类(必须执行)推荐(证据级别B):所有接受ICI治疗的患者均需在基线时(即ICI治疗前)行心电图检查、检测肌钙蛋白和利钠肽;高危患者(接受双联ICI治疗或ICI与心脏毒性抗癌药联合治疗的患者、发生ICI相关非心血管不良反应的患者、有心血管疾病史的患者)均需行基线超声心动图检查。尽管早期检出心肌炎症的前景良好,但ICI治疗期间常规心脏监测的成本效益尚未明确。
此外,常规肌钙蛋白筛查存在解读错误和治疗不当的实际风险:在普通人群中,肌钙蛋白升高提示心肌梗死的概率是心肌炎的7倍;接受ICI治疗的患者中,传统的主要不良心血管事件也比心肌炎更常见。
此外,肌钙蛋白升高可能是恶性肿瘤细胞克隆表达肌钙蛋白,或恶性肿瘤浸润心肌导致肌钙蛋白释放所致。
03
治疗与预后
意义未明的肌钙蛋白升高
仅肌钙蛋白升高不足以停止ICI治疗或启动免疫抑制治疗,是否继续ICI治疗需经多学科团队共同决策。
由于此类情况可能是ICI相关心肌炎的早期亚临床表现,无论是否继续ICI治疗,均需对心肌生物标志物、心电图和心血管疾病的体征症状进行系列监测。
隐匿性心肌炎
符合ICI相关心肌炎诊断标准,但无症状且检查仅见轻微异常的患者,归为隐匿性或亚临床心肌炎。
这类特殊患者应先暂停ICI治疗,若ICI仍是最佳癌症治疗方案,经多学科评估后可重启治疗。
目前尚无足够数据明确继续ICI治疗后,疾病进展为临床症状明显或重症型的概率,因此需对患者进行密切监测。
尽管尚无严格标准,但对于LVEF下降、出现新发传导异常或室性心律失常、肌钙蛋白显著升高的无症状患者,通常应按临床心肌炎而非隐匿性/亚临床心肌炎管理。
肌钙蛋白升高的程度可作为另一项风险评估指标,也是国际ICI心肌炎注册研究中,预测严重或危及生命的心脏毒性事件评分的核心指标。在该风险评分的前瞻性验证队列中,7名评分为0分的患者均未发生严重事件,即使未接受免疫抑制治疗(仅停用ICI)。同样,在28名因疑似ICI相关心肌炎接受心内膜心肌活检的连续患者中,5名活检未见心肌细胞溶解、仅见低度炎症浸润的患者(其中4名肌钙蛋白水平与活检阴性患者相近)未接受糖皮质激素或其他免疫调节剂治疗,其中4名继续接受ICI治疗,所有患者均保持无症状且无心血管并发症。
非重症心肌炎
符合ICI相关心肌炎诊断标准、有症状但无血流动力学或电活动不稳定的患者,应停用ICI,入院行遥测监护并接受多学科评估。
确诊后应尽快启动静脉甲泼尼龙治疗,剂量为500~1000mg/天;待肌钙蛋白水平呈下降趋势后,改为口服泼尼松1~2mg/(kg・天)(多数中心一般不超过100mg/天)。随后可根据肌钙蛋白水平和临床状态,每周将泼尼松减量约10mg,当剂量降至10mg/天后,减慢减量速度;
对于轻症患者,可采用更快的减量方案。
监测肌钙蛋白时需注意,肌钙蛋白I和肌钙蛋白T的峰值出现时间不同(中位时间分别为发病第3天和第7天),且肌钙蛋白I恢复正常的速度更快(中位时间分别为发病第17天和第133天)。这一动态变化为判断治疗反应和激素抵抗带来了挑战。
对于激素抵抗型病例(本文定义为:大剂量甲泼尼龙治疗后,临床症状加重和/或肌钙蛋白持续升高),需考虑加用二线免疫抑制剂。阿巴西普是一种细胞毒性T淋巴细胞抗原4免疫球蛋白融合蛋白,可通过结合抗原呈递细胞表面的CD80/CD86分子下调T细胞激活,基于小样本量和非随机研究数据,该药已成为逆转ICI激活通路的首选药物。鲁索利替尼是Janus激酶1(JAK1)/Janus激酶2(JAK2)抑制剂,可快速抑制T细胞激活,因阿巴西普的起效(达峰)时间较慢,鲁索利替尼可用于增强疗效、弥补药物代谢动力学的时间差。目前有关阿巴西普治疗轻中度ICI相关心肌炎(临床试验编号:NCT05335928)和重症ICI相关心肌炎(临床试验编号:NCT05195645)的研究正在进行中。
英夫利昔单抗与心血管死亡风险升高相关,应避免使用,尤其是心力衰竭患者。对于长期使用激素出现明显不良反应、无法完成激素减量方案,或因合并其他免疫抑制状态(如血液系统恶性肿瘤)而存在机会性感染高风险的患者,吗替麦考酚酯可作为激素节省剂。
长期使用激素(泼尼松≥20mg/天,持续4周及以上)的患者,常规需使用预防性抗生素(如甲氧苄啶-磺胺甲恶唑)、抗真菌药(如制霉菌素)和质子泵抑制剂。接受免疫抑制治疗的患者,需及时筛查和处理感染,同时也需关注高血糖等严重的代谢相关问题。
最后,大剂量免疫抑制治疗可能拮抗ICI的原发治疗效果,尤其是在ICI治疗早期(前2个月)启动时,但这一点仍存在争议。
重症心肌炎
ICI相关心肌炎患者若出现电活动或血流动力学不稳定的进展性体征,应在肿瘤科和心脏科协作下转入重症监护室。立即停用ICI,同时启动大剂量激素治疗(静脉甲泼尼龙500~1000mg/天),并同步开展进一步诊断和临床稳定治疗。重度房室传导阻滞患者可能需要临时起搏,心律失常不稳定患者可能需要电复律/除颤。心源性休克患者必要时需使用血管加压药和正性肌力药,部分病例需采用临时机械循环支持,作为治疗过渡或康复过渡。
对于出现重症/暴发性心肌炎或三重M综合征(肌炎、心肌炎、类重症肌无力综合征)的患者,推荐首选大剂量激素联合另一种免疫抑制剂(如阿巴西普)的初始方案,阿巴西普可单独使用,也可与JAK抑制剂、抗胸腺细胞球蛋白和/或静脉注射免疫球蛋白、血浆置换联用。静脉注射免疫球蛋白和/或血浆置换尤其适用于类重症肌无力综合征表现的患者。重症ICI相关心肌炎或三重M综合征患者的治疗通常需要多学科协作,若医疗机构无法处理潜在并发症,应考虑将患者转院。
ICI相关心包炎及其他并发症
ICI相关心包炎患者需监测心包积液和心脏压塞情况。对于合并心肌受累的重症心包炎或中至重度心包积液患者,应停用ICI,并启动糖皮质激素治疗(可联用秋水仙碱),疗程3~5天;临床症状改善后,根据症状和C反应蛋白水平缓慢减量。与其他类型心包炎不同,此类患者初始即使用激素的原因是,ICI相关心包炎的发病机制推测为活化T淋巴细胞介导。
对于激素抵抗型病例,可考虑使用白细胞介素-1拮抗剂(如阿那白滞素、利洛纳塞)。对于无并发症的ICI相关心包炎,可继续ICI治疗,同时给予大剂量非甾体抗炎药(阿司匹林750~1000mg,每8小时1次;或布洛芬600mg,每8小时1次,疗程1~2周)和秋水仙碱(0.6mg,每日2次,疗程3个月);无并发症的患者,可在秋水仙碱维持治疗的基础上考虑ICI再次用药。
急性冠脉综合征、心肌病等其他心脏并发症,应遵循心脏病学常规指南治疗,同时结合多学科意见。章鱼壶型心肌病患者在心肌病缓解后,可恢复ICI治疗,这一结论也在接受其他癌症治疗的同类患者中得到验证。
04
结局与预后
一项单中心当代研究纳入160例疑似ICI相关心肌炎患者,结果显示其1年心血管死亡率随病情严重程度呈梯度变化:重症患者(n=28)为27.6%,非重症患者(n=96)为5%,非心肌炎患者(n=36)为8%;而非重症患者发病1年内的心血管相关再入院率在数值上高于重症和非心肌炎患者,但差异无统计学意义(分别为16%、4%、6%)。有趣的是,三组患者的总死亡率无显著差异(分别为64%、57%、53%)。
使用1种以上免疫抑制剂的患者死亡率更高(50% vs 21%),合并肌炎、心肌炎和类重症肌无力综合征的患者亦是如此。呼吸肌受累是关键的预后因素,呼吸困难和需要氧疗与主要不良事件风险升高相关。其他具有预后意义的指标包括:肌钙蛋白峰值及变化趋势、完全性房室传导阻滞、QRS波群增宽(>100ms)或QTc间期延长(>450ms)、超声心动图或心脏磁共振成像检测的心肌应变异常、心脏磁共振成像的心肌固有T1值升高。
基于国际ICI心肌炎注册研究的所有可用指标,Power等人确定了5项可预测严重、危及生命的心肺事件的指标,这些指标可在患者疑似ICI相关心肌炎就诊时评估临床病程,也可为分诊决策提供依据。
ICI再次用药的决策需平衡初始发病的严重程度、复发风险和重启ICI治疗的潜在获益。若条件允许,首选单药ICI治疗,更换ICI种类,避免使用细胞毒性T淋巴细胞抗原4(CTLA-4)抑制剂。再次用药期间,建议通过心肌生物标志物系列检测(每个ICI治疗周期1次,出现症状时提前检测)和定期影像学检查进行监测,以早期检出心脏毒性反应并及时干预,如停用ICI、启动免疫抑制治疗。
05
再次用药
肿瘤临床指南推荐,发生任何4级irAE(不良事件通用术语标准)和2级及以上心肌炎的患者,应永久停用ICI。目前关于ICI再次用药后心肌炎等irAE复发风险的数据十分有限。在Vigibase数据库的452例患者队列中,25%~33%发生过irAE的患者,再次用药后出现相同不良反应复发。在1082例非致死性心肌炎患者中,16例接受了ICI再次用药,其中6例(38%)出现心肌炎复发。
仅在以下情况下可考虑ICI再次用药:ICI相关心肌炎临床症状完全缓解,免疫抑制治疗剂量降至最低(理想状态为口服泼尼松等效剂量<10mg/天),且有明确的临床指征需要继续ICI治疗。此类情况下,需在医生与患者共同决策的基础上进行,详细告知患者风险与获益,包括新发或复发性毒性反应对生活质量的潜在影响。考虑再次用药时,需采取多种风险缓解策略(图3)。目前,预防性使用免疫抑制剂(如小剂量泼尼松)以减少新发和复发性irAE的研究正在进行中。
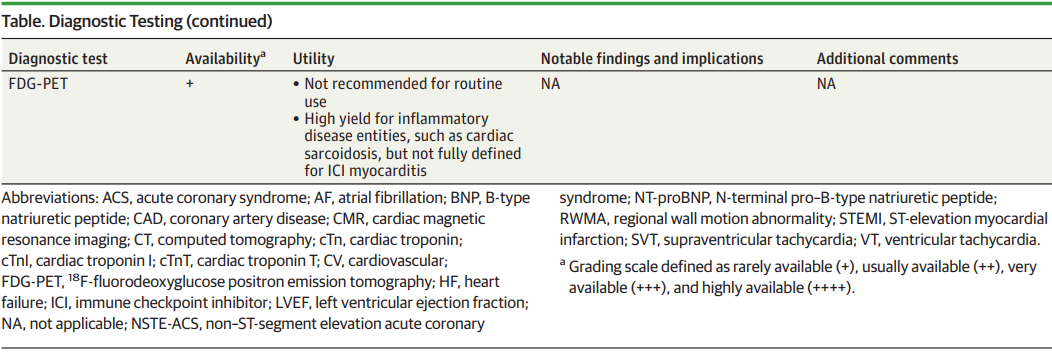
图3ICI再次用药的策略示意图
06
结论
随着可使用ICI的癌症患者群体不断扩大,不仅是患者数量增加,患者的疾病多样性和合并症也更为复杂,各医学领域的医护人员面临着为这类患者优化心血管不良反应管理的挑战。对患者采取多学科、个体化的管理策略,兼顾病情严重程度,并平衡毒性反应与继续使用挽救性癌症治疗方案的必要性,才能使患者最大程度获益。