

复旦大学附属中山医院心内科黄浙勇教授
思辨介入困境
解析手术技巧
梳理中山经验
助您从新手变“心”手
每月15日、30日,严道医声独家发布
心肌壁内血肿(intramyocardial hematoma,IMH)是指血液进入心肌组织并沿肌纤维间隙形成夹层或局灶性血肿的病理状态。属于急性心肌梗死或PCI的一种罕见的机械并发症,可以理解为心脏破裂之前的过渡状态:撕而不破!
有时候,心肌壁内血肿和心外膜下血肿(心肌和心外膜之间)、包裹性心包积血(心外膜和壁层心包之间)难以精确区分,血流动力学影响也类似,在此一并讨论。
一
心肌结构和心肌壁内血肿
心肌纤维在解剖上呈多层螺旋状排列,可分为三层(图1),因此可能发生层间撕裂。然而,与血管壁不同,心肌层间缺乏明显的弹力层结构,心肌与心内膜、心外膜之间亦无弹力层,因此一旦出血形成夹层,血肿往往难以局限,容易进一步扩展并最终发生破裂:向心腔破裂,形成冠状动脉-心腔瘘;向心包腔破裂,导致心包积血甚至心脏破裂。因此,血肿局限于心肌壁内并不常见,仅见于PCI间隔支穿孔和急性心肌梗死时。
(1)穿隔支穿孔。心室壁供血通常从心外膜向心内膜逐级分支,室间隔的特殊之处在于两侧均为心内膜面,供血血管从中穿越,即穿隔支!穿隔支穿孔时,出血部位位于室间隔中央部位,从而形成肌间血肿。室间隔侧枝是广受青睐的CTO逆向通路,理由是即使发生穿孔,出血往往局限于心肌而较少导致心包填塞。然而,室间隔血肿一旦扩大,也可诱发明显的血流动力学障碍。因此,对室间隔侧枝穿孔仍需及时处理。
(2)心肌梗死机械并发症。在急性或亚急性阶段,梗死区微循环结构受损,再灌注后容易发生梗死后出血。若出血沿肌束间隙扩展,可形成心肌壁内血肿,甚至进一步发展为心脏破裂(图2)[1]。从病理演变角度可将其概括为以下连续过程:“心肌内出血→心肌壁内血肿→心脏破裂或室间隔穿孔”。再灌注治疗(溶栓或PCI)可能成为壁内血肿的触发因素。此外,梗死区心肌失去原有收缩力度,也为血液在肌束间隙扩展提供了条件。
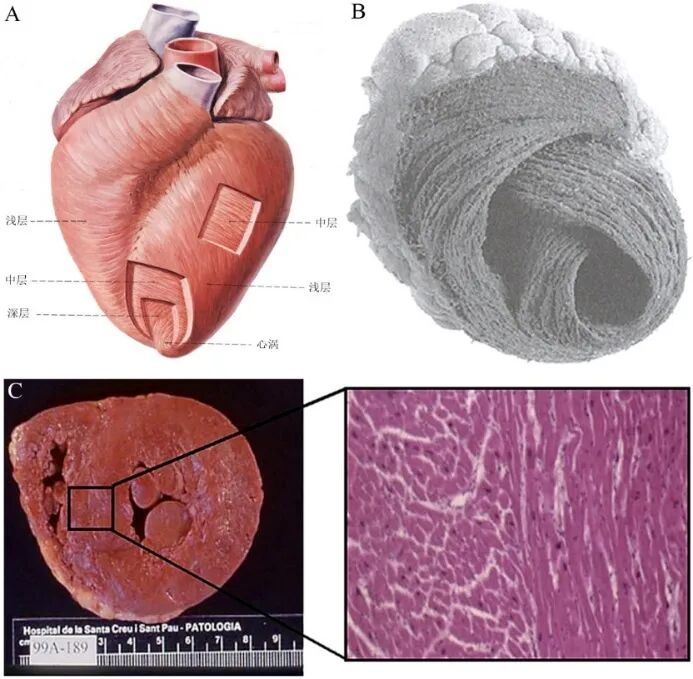
图1 心肌纤维的分层现象。
A.示意图。B.Torrent-Guasp认为,心肌条带像筋道宽面或皮带一样,以螺旋的形态包裹成心脏。C.心脏横断面显示心脏由多层不同排列方向的多层纤维组成。
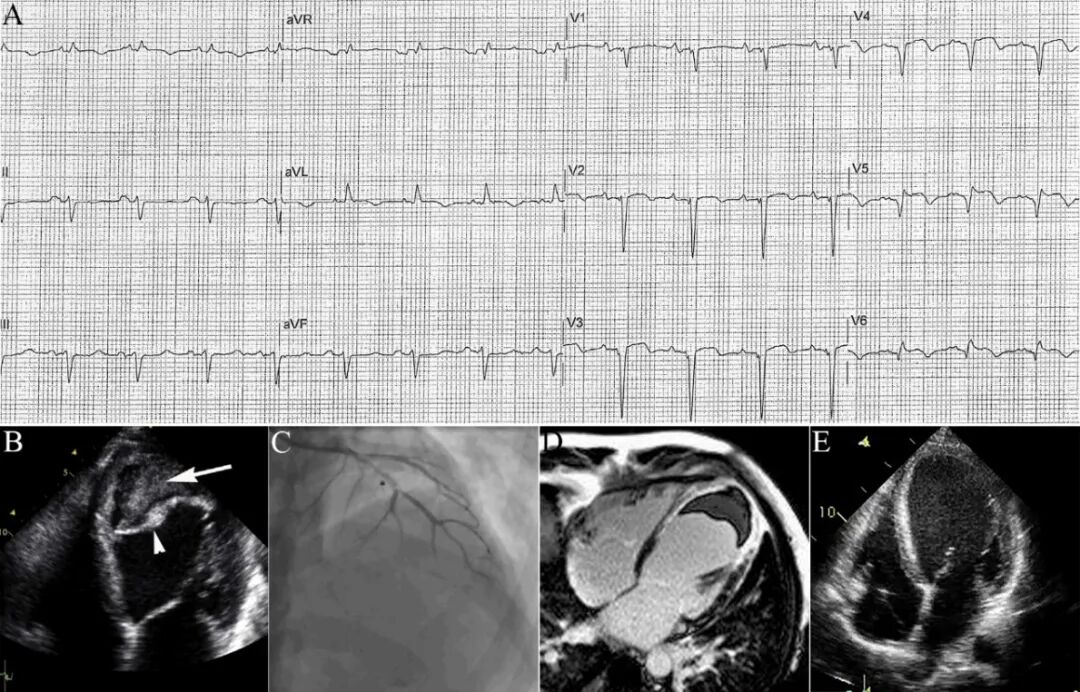
图2 AMI并发自发性心肌壁内血肿[2]。
42岁男性,劳力性呼吸困难2周,无胸痛病史和心血管危险因素。心电图示胸前导联广泛Q波形成(A)。心超示左室心尖部、前壁活动消失,LVEF<20%;最大发现是左室心尖部巨大混合性团块,声学造影和多普勒检查均未发现团块与心腔相通,也无心包积液,考虑心梗后心肌内血肿(B)。冠脉造影显示前降支中段次全闭塞(C)。增强CMR显示心肌梗死合并左室壁内血肿形成伴心尖部少量附壁血栓(D)。多学科会诊后决定保守治疗。住院期间反复出现持续性单形性室速,电复律后植入ICD。出院后6个月复查心超显示心肌壁内血肿和附壁血栓消失(E)。
二
心外膜结构和心外膜下血肿
心外膜结构极为纤薄,仅由一层间皮细胞构成,籍脂肪结缔组织与外层心肌连接。心外膜其实也是浆膜性心包的脏层(图3)。
理论上,PCI相关的心外膜下血肿见于以下几种情形:①导丝“谨小慎微”的行走在心外膜下间隙,而不捅破菲薄的心外膜;②心外膜下冠脉穿孔,但破裂面发生在血管的心肌面,而不累及心外膜;③肌间微小血管穿孔,逐渐渗漏到心外膜下间隙。
事实上,一旦出血达到至心外膜下,往往容易突破纤薄心外膜进入心包腔,导致游离性心包积液。因此,心外膜下血肿的发生前提是心外膜明显增厚或存在粘连!
(1)房间沟和室间沟。心外膜下脂肪层分布极不均匀,房间沟和室间沟脂肪较厚,包含冠状动脉和静脉、神经等组织(图3A)。若该区域冠脉穿孔,血液可在脂肪层内局部堆积,外渗的造影剂难以消散,俗称“脂肪染色”。
(2)心脏外科术后。CABG等心脏外科手术后,心外膜增厚,心包黏连。此时,心肌或心外膜下出血不易突破心外膜,因此容易形成心肌壁内血肿或心外膜下血肿;即使突破心外膜,也容易被黏连的心包所包裹,形成包裹性心包积血。诚如前述,偏心的心肌内血肿、心外膜下血肿和包裹性心包积血在临床上难以鉴别,对血流动力学影响也雷同,通常无需鉴别(图4-5)。既往研究报道[3],在部分所谓“心肌壁内血肿”的病例中,相当比例存在CABG病史。传统观点认为这种情况在一定程度上具有“保护作用”,可降低急性心包填塞的发生风险。然而需要注意的是,一旦局部血肿形成并压迫心腔,可导致所谓的干性心包填塞,其处理往往比典型心包填塞更加困难。

图3 心外膜下脂肪的分布和结构,部分素材来自[4]
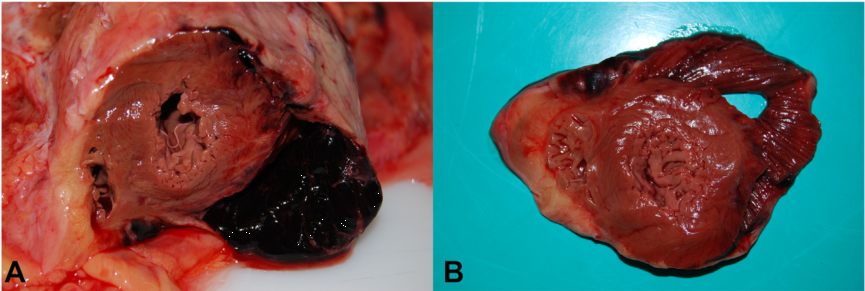
图4 心肌壁内血肿的大体观[5]。
桥血管PCI后出现壁内血肿,进行性增大,临床疑诊包裹性心包积血。但最后尸检证实为左室侧壁心肌内囊袋样血肿(A),清理血块后发现心肌夹层撕裂范围极大,几乎包绕左室游离壁(B)。
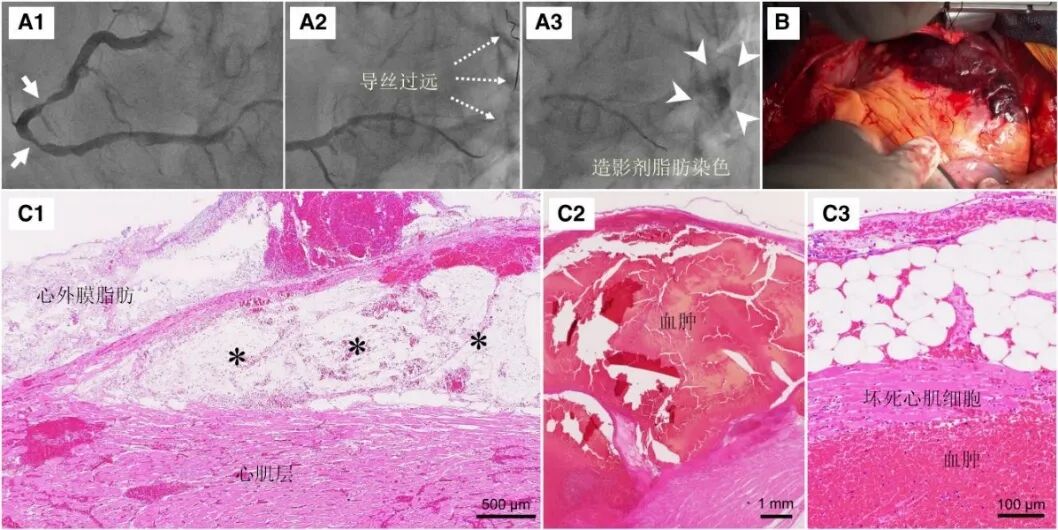
图5 心肌壁内血肿的组织学表现[6]。
75岁男性,右冠中段严重狭窄(A1),介入过程中导丝送入左室后支的小分支过远(A2),导致冠脉穿孔和脂肪染色(A3)。心超提示合并游离性心包积液。立即弹簧圈封堵,心包穿刺,但渗出持续,血流动力学不稳定。心外科紧急手术修补,术中发现下侧壁到心尖部的巨大血肿(B)。5天后患者死于多器官衰竭。尸检发现左心室表层巨大肌间夹层(C1-C2),血肿毗邻处可见心肌坏死(C3)。由此确诊该患者存在冠脉穿孔导致的心肌壁内血肿。
三
临床后果
心肌壁内血肿的临床后果可概括为“三个压迫”和“三个破裂”。压迫心腔导致低血压,压迫冠脉导致心绞痛,压迫心肌导致心律失常;破入心腔导致心腔瘘,破入心包导致心包积液,贯通破裂就是心脏破裂(图6-7)!

图6心肌壁内血肿的临床后果
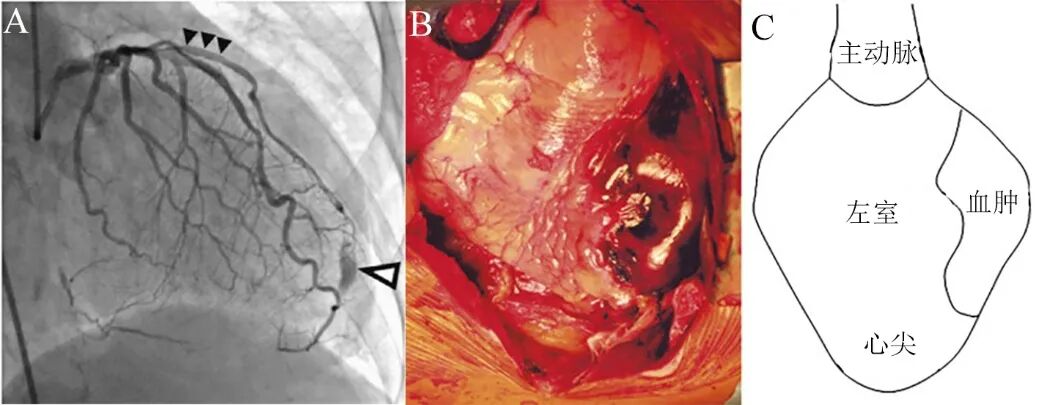
图7 心肌壁内血肿导致心脏破裂[9]。
70岁男性,静息性心绞痛2个月(A)。造影显示第一对角支近段99%狭窄,支架置入(A,黑色箭头),远端发生导丝穿孔(A,白色箭头)。病人出现胸痛,I、avL、V4-V6 导联ST段抬高,随后低血压、心动过速,心超证实心包填塞。心包抽取500 ml血液后外科手术,发现心包腔大量积血,前侧壁巨大心外膜下血肿伴局部破裂孔(B-C)。行外科修补加CABG手术,术后因消化道出血而死亡。
1、低血压。血肿压迫心腔是最主要的临床危害,可表现为类似心包填塞的血流动力学改变(低血压),但由于心包腔内积液不明显,因此常被称为假性心包填塞(pseudotamponade)或干性心包填塞(dry tamponade)。不同部位的血肿,其压迫效应存在明显差异(图8)。
①房室沟和右室游离壁:房室沟处血肿可压迫心室流入道,不仅直接阻碍房室口血流,还可能影响房室瓣功能,类似于“粘液瘤样效应”。因此即使是较小血肿也可引起显著的血流动力学恶化[7]。右室游离壁壁薄,也容易受到压迫出现低血压。
②室间隔:基底部室间隔血肿可压迫左室或右室流出道,类似“肥厚型梗阻性心肌病”,容易引起梗阻性低血压,迄今已有致死报道[8]。若血肿位于中部间隔,可压迫右心室,导致低血压(图9)。若血肿位于心尖部间隔,病理生理机制类似“心尖肥厚性心肌病”,临床意义较小。
③左室游离壁:由于左室游离壁较厚,对外压的耐受性相对较高,因此该部位血肿(尤其是心外膜下血肿)对血流动力学的影响通常较小。
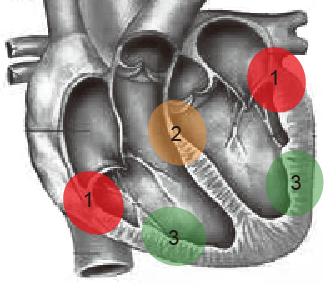
图8 心肌壁内血肿部位。
1为房室沟,2为室间隔,3为游离壁
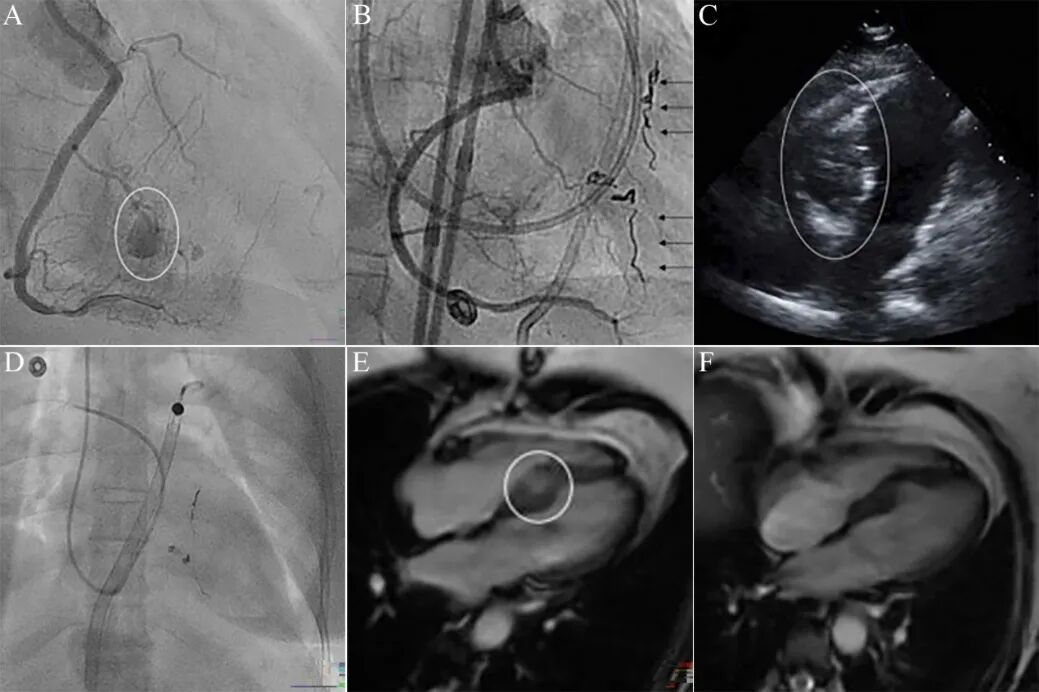
图9 室间隔血肿导致顽固性低血压[9]。
右冠CTO,经室间隔侧枝逆向开通后,造影发现穿隔支穿孔和室间隔血肿形成(A)。回病房后反复胸痛,血压稳定在100/78 mmHg左右,送回导管室复查造间隔血肿扩大,间隔侧枝弹簧圈封堵(B)。患者血压进行降低至70/48 mmHg,2小时内液体复苏3 L ,多巴胺和去甲肾上腺素静脉升压,效果不佳。超声显示室间隔血肿4.2cm,右室几乎被完全压闭(C),左室功能正常,心包积液微量。鉴于严重右心衰,经右股动脉植入右室辅助装置(Impella RP)(D),血流动力学立即恢复正常,血肿逐日缩小。出院前MRI(E)相比, 3个月后血肿基本吸收(F)。
2、胸痛。血肿可伴有不同程度的渗出或轻度破裂,可产生心包刺激,从而出现典型的浆膜性胸痛。偶尔的,血肿压迫心外膜下脂肪层内的冠脉分支,也可诱发心绞痛。
3、心律失常。心肌内出血与缺血坏死区域可共同形成电不稳定基质,从而增加室速/室颤的发生风险。
参考文献:
⇅ 向上滑动阅览
“中山PCI解码”下期预告
心肌壁内血肿2:从影像识别到治疗决策
心肌壁内血肿处理方法没有共识。传统观点要求外科手术,近年来有不少保守成功的案例。基于“血肿进展→血肿破裂或血流动力学崩溃”的病情三要素判断,可采取三种不同的治疗策略:血肿稳定型 → 保守;血肿进展型 → 介入;破裂/崩溃型 → 外科。


