
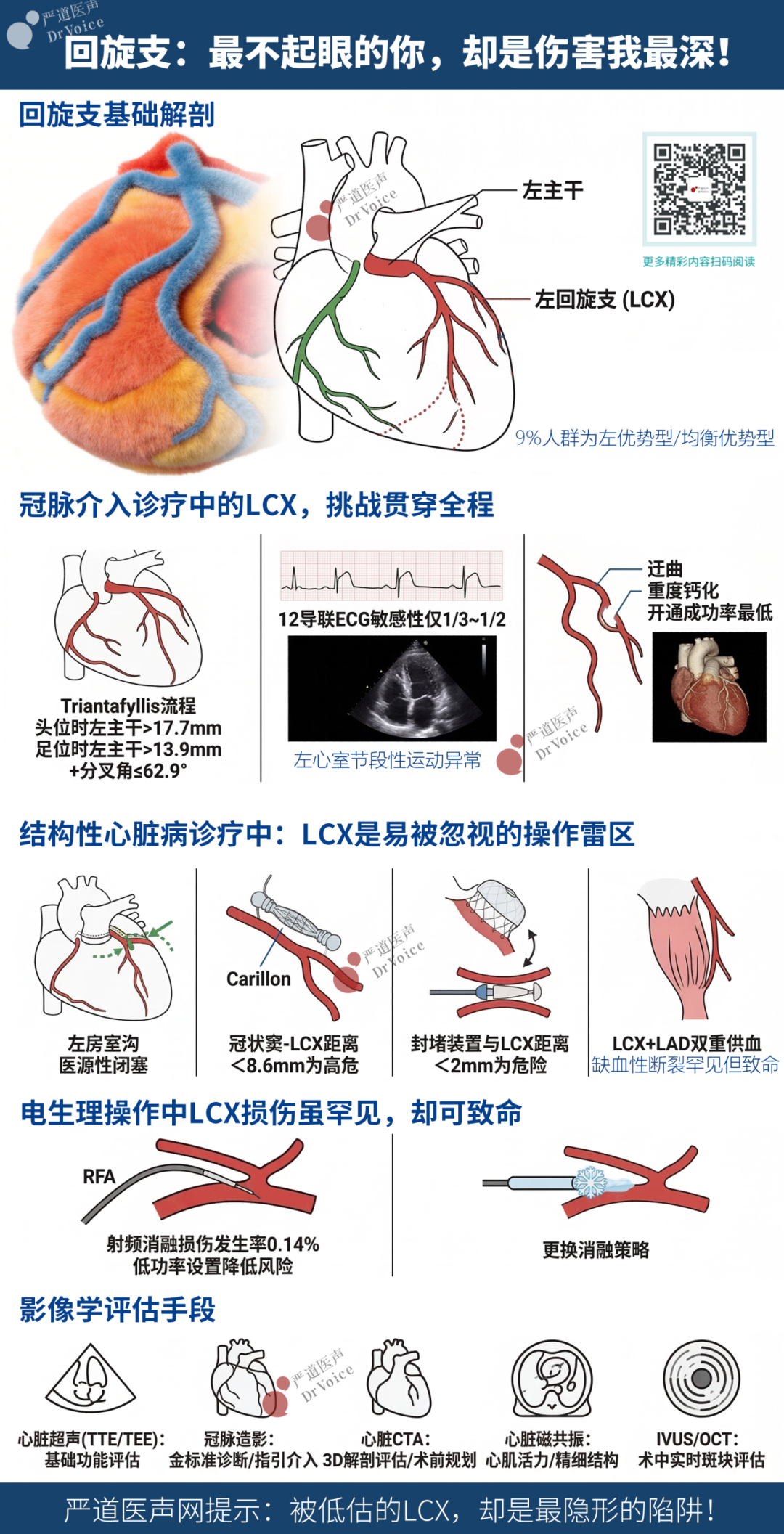
在冠状动脉家族中,左前降支(LAD)、右冠状动脉(RCA)始终是临床关注的焦点,而回旋支(left Circumflex Artery, LCX)始终因存在感较低而被忽视。但最新发表于《Rev Cardiovasc Med》2026年2期的综述却直指这一被低估的血管:相较于其他冠脉,LCX在射频消融、左心耳封堵、二尖瓣修复等多种心内操作中更易受损,慢性完全闭塞病变(CTO)开通成功率更低,且其与心大静脉的解剖关系高度多变,约30%的病例中会因LCX介入操作引发心大静脉损伤。这一系列临床特点让LCX成为最不起眼却最易造成致命伤害的隐患血管。

作为心血管内科医师,我们日常诊疗中对LCX的认知偏差,往往会导致诊疗延误、并发症增加甚至不良预后。本文将基于该综述的核心内容,系统梳理LCX的临床意义、介入挑战与复杂解剖特点,结合影像学应用与诊疗策略,为临床实践提供循证参考。
01
LCX的坎坷,从其解剖起点就已注定
在绝大多数人群中,左主干分为LAD和LCX,这是LCX的基础解剖特征。
LCX走行于左心室与左心房之间的左房室沟心外膜下,可发出多达3支钝缘支;若冠脉循环为左优势型或均衡优势型,LCX还会发出左后外侧支(PLB),并为后降支供血,其供血区域为左心室侧壁和后外侧壁。
正是这一看似固定的解剖走行,成为其与周围心脏结构紧密关联的基础,也为后续操作损伤埋下了伏笔。
冠脉循环的优势型由后降支(PDA)和PLB的供血来源决定,与LCX密切相关:临床中最常见的是右优势型(RCA为后降支供血),约9%的正常人群为左优势型(LCX为PDA供血)或均衡优势型(PDA /PLB由RCA和LCX共同供血)。
解剖特点直接影响LCX的临床重要性——左优势型人群中,LCX的损伤或闭塞将直接导致左心室后下壁严重缺血,预后更差。
更值得关注的是,LCX的解剖变异与畸形发生率并不低,且多数变异会增加临床诊疗难度,包括LCX缺如、单独开口、走行迂曲、分叉角度异常等,而其与心大静脉的解剖关系更是最大变数:约30%的病例中,二者的位置关系高度多变且无法预测,这也是LCX介入操作中心大静脉损伤的解剖学原因。
表:LCX的临床意义、介入挑战和管理策略

02
冠脉介入诊疗中的LCX,挑战贯穿全程
LCX相关的冠状动脉疾病是临床最常见的诊疗场景,从解剖变异到急性闭塞,从钙化病变旋磨到CTO开通,每一个环节都存在独特的介入挑战,且其诊疗难度远高于LAD和RCA。
(一)LCX解剖变异
LCX的解剖变异并非罕见,且部分变异会直接导致动脉粥样硬化更早、更严重,甚至引发心肌梗死或心源性猝死,临床中若未能及时识别,将造成严重诊疗失误。
右冠窦起源的LCX:这是第二常见的冠脉解剖变异(最常见为左主干缺如,LAD与LCX分别开口于左冠窦),并非真性畸形,但因血管开口呈裂隙状、主动脉后段反复受压,易诱发早发且进展迅速的动脉粥样硬化。冠脉造影若未能预判并识别该变异,可能导致非阻塞性冠脉心肌梗死的误诊,延误介入治疗,增加梗死面积,同时还会增加造影剂用量和辐射暴露;在经导管主动脉瓣置换术(TAVR)中,该变异还会增加冠脉阻塞风险,需术前充分识别以做好冠脉保护。Triantafyllis等人分析了异常LCX的血管造影预测因素,并对136例异常LCX患者和135例对照者进行了比较。他认为,左主干较长和分叉角度锐利可能提示存在异常LCX。此外,还提出了“Triantafyllis流程”,用于从右前斜位快速识别异常LCX:头位视角下左主干长度>17.7mm时,患者存在该变异的概率增加5.3倍;若头位视角<17.7mm,需进一步行足位视角测量,若左主干长度>13.9mm且分叉角度≤62.9°,则高度怀疑该变异,无上述表现则概率极低。
双LCX畸形:属于罕见的解剖变异,临床挑战主要为易漏诊或低估畸形LCX相关的心肌缺血,其解剖特点多为一支LCX起源于左主干,另一支起源于RCA,极罕见情况下两支均起源于左冠窦。
冠状动脉异常起源于主动脉窦(AAOCA):该畸形中LCX起源于右冠窦,冠脉造影若发现LCX收缩期“挤奶样”改变,提示其为主动脉后异常走行,属于危及生命的情况,易诱发恶性心律失常和心肌梗死,需要重视。
肺动脉起源的左冠脉(ALCAPA):其中LCX起源于右肺动脉的亚型极为罕见,首发表现可为心源性骤停,需多模态影像学确诊并紧急外科矫正。
LCX瘘:瘘口可引流至冠状窦、右心房、肺动脉或左心耳,其临床症状由多种机制引发,包括冠脉扩张处附壁血栓、动脉瘤壁破裂、感染性心内膜炎、左向右分流、冠脉窃血导致的心肌缺血、主动脉瓣关闭不全等。心脏CTA、右心导管、冠脉造影和血管内超声(IVUS)是评估的关键手段,可明确血管大小、附壁血栓、内膜完整性和局限性动脉瘤;核素负荷试验对可逆性缺血的检测通常为阴性。当肺体循环流量比(Qp:Qs)>1.5:1时,需行瘘口封堵;若动脉瘤样变性引发血栓、破裂或冠脉窃血,也需积极介入干预。
(二)LCX闭塞在急性冠脉综合征(ACS)中最易漏诊
急性LCX闭塞是ACS中最易漏诊的类型,若未能及时识别,将导致再灌注治疗延误,显著增加不良预后风险,其漏诊的核心原因与临床表现和检查特点密切相关。
标准12导联心电图对急性LCX闭塞的敏感性极低,仅能在1/3~1/2的ACS患者中检测到异常,约1/3的LCX闭塞ACS患者无明显ST段改变,直接导致门-球时间延迟;且与其他冠脉闭塞相比,LCX闭塞更易表现为非ST段抬高型ACS(NSTE-ACS),进一步增加了诊断难度。
为克服这一诊断挑战,有人提出采用床旁经胸超声心动图(TTE)识别左心室节段性运动异常,联合V7-V9后壁导联的额外记录,同时结合心肌标志物和超声心动图的室壁运动异常,可显著提高诊断准确性。
(三)下壁心肌梗死时LCX与RCA,谁是真凶?
下壁心肌梗死中,LCX和RCA均为潜在的罪犯血管,仅依靠冠脉造影往往无法明确判定,而罪犯血管的精准识别直接影响介入治疗策略和预后。
临床中虽有心电图流程用于识别下壁心肌梗死的罪犯血管,但其鉴别效能尚未得到证实。结合无创影像学及超声心动图室壁运动异常的PCI指导策略,可使靶病变失败的主要复合终点降低31%。定量影像学的核心优势在于可实现更客观的诊断,精准识别稳定/不稳定斑块、溃疡、夹层和血栓,同时评估治疗效果,但临床应用中需结合具体场景、患者特点和技术可及性,要求医师具备丰富的操作经验。
(四)钙化病变旋磨的高风险,LCX开口病变
LCX开口的重度钙化病变伴明显弯曲时,旋磨术的操作难度极高,并发症风险显著高于其他冠脉,对术者经验提出了严格要求。
心脏CTA和血管内影像学可帮助明确解剖结构、理解病理特点,选择合适的减容策略和旋磨头尺寸,是降低操作风险的关键。
造影中需采用多投照视角评估旋磨导丝与钙化灶的实际接触点,若LCX开口侧壁存在重度偏心钙化斑块,旋磨头跳动可能导致开口嵴侧穿孔,因此需尝试消蚀开口侧壁以避免该并发症,但过度消蚀又可能因深度切割导致侧壁穿孔。
此外,LCX开口穿孔后的经皮补救性介入难度极大——血管弯曲角度会干扰支架输送,而覆膜支架的植入又可能阻塞LAD,这也是旋磨术需严格把控操作规范的重要原因。
(五)LCX近段/开口病变PCI预后更差
LCX开口或极近段的新发病变行PCI治疗后,预后显著差于LAD和RCA的同部位病变:一项纳入4759例患者的1年随访研究显示,LCX病变的靶病变血运重建率和主要不良心脏事件(MACE)发生率更高。原因包括急性LCX闭塞的诊疗挑战(漏诊导致再灌注延误)、血管解剖特点(开口弹性纤维含量高、钙化负荷重、分叉和角度异常)等。定量影像学的应用可实现更客观的诊断,有效改善诊疗结局,是提高该类病变PCI疗效的重要手段。
(六)CTO开通成功率最低的靶血管
在多中心CTO-PCI注册研究中,LCX是最不常见的靶血管,且其CTO开通的手术成功率更低,并发症发生率呈非显著性升高趋势。
原因是LCX CTO病变具有更显著的解剖复杂性:血管走行更迂曲、解剖走行变异多、钙化负荷重、分叉和角度异常更常见。
心脏CTA的3D容积重建图像是LCX CTO-PCI术前规划和管理的关键手段,可对斑块形态和成分进行详细的解剖和形态学表征;评分系统的应用可帮助选择减容策略,预测介入操作的成功率,为临床决策提供循证依据。
(七)心大静脉损伤是LCX介入的独特并发症
心大静脉是冠状窦最长的属支,58%起源于前室间沟下1/3,与心中静脉在心底汇合形成冠状窦,其与LAD、LCX交叉形成Brocq三角,二者的解剖关系是LCX介入操作中独有的风险点。
约60%~70%的人群中的心大静脉走行于冠脉浅面,而30%的人群中的心大静脉走行于两支冠脉深面,这一高度多变且不可预测的解剖关系,使得LCX介入操作中的心大静脉损伤成为独特且易发生的并发症。
重度钙化的LCX斑块在介入操作中向血管壁外突出,加之LCX与心大静脉共同走行于狭窄的室间沟内,无足够的活动空间,过度的球囊扩张会直接导致相邻的心大静脉受损。

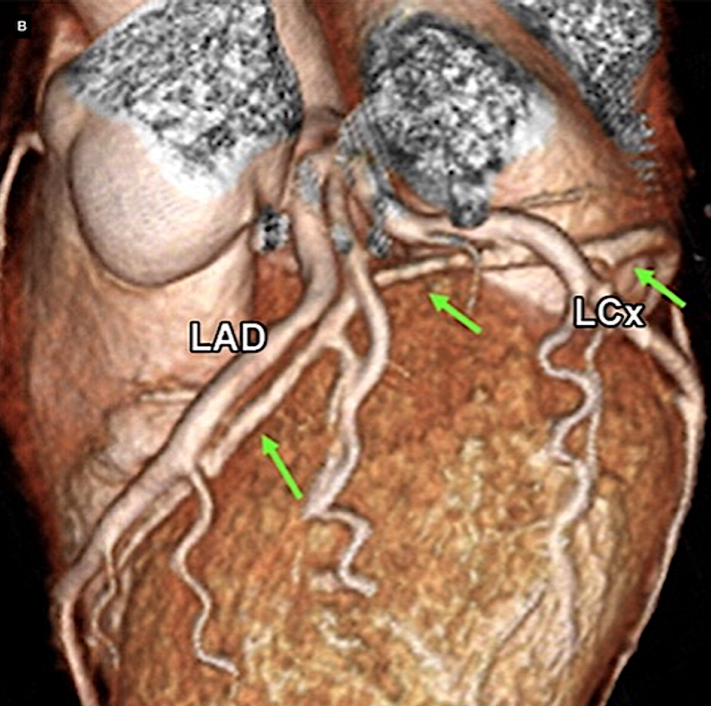
冠状动脉CTA成像
心大静脉(GCV)(绿色箭头)穿过左前降支(LAD)和左回旋支(LCX)动脉,形成一个三角形。在60%–70%的人群中,前室间静脉走行于动脉表面(A),而在30%的人群中,该静脉从两条动脉下方穿过(B)
心大静脉损伤的诊断为排除性诊断:若介入后出现静脉性心包积液,且无心脏右侧或周围结构损伤,胸部CT显示LCX-PCI区域存在血肿,即可确诊;部分病例可出现无积液的血流动力学恶化(干性心包压塞),需高度警惕。
心大静脉损伤的治疗策略为个体化决策:首先考虑保守治疗,若患者持续出血或血流动力学不稳定,需行心包穿刺引流;复杂病例中需紧急开胸探查,清除血肿并缝合受损静脉,高风险患者可采用导管相关的补救性介入技术。
心脏静脉系统的影像学信息可帮助理解空间解剖关系,优化钙减容策略,最大限度减少并发症,改善预后。
03
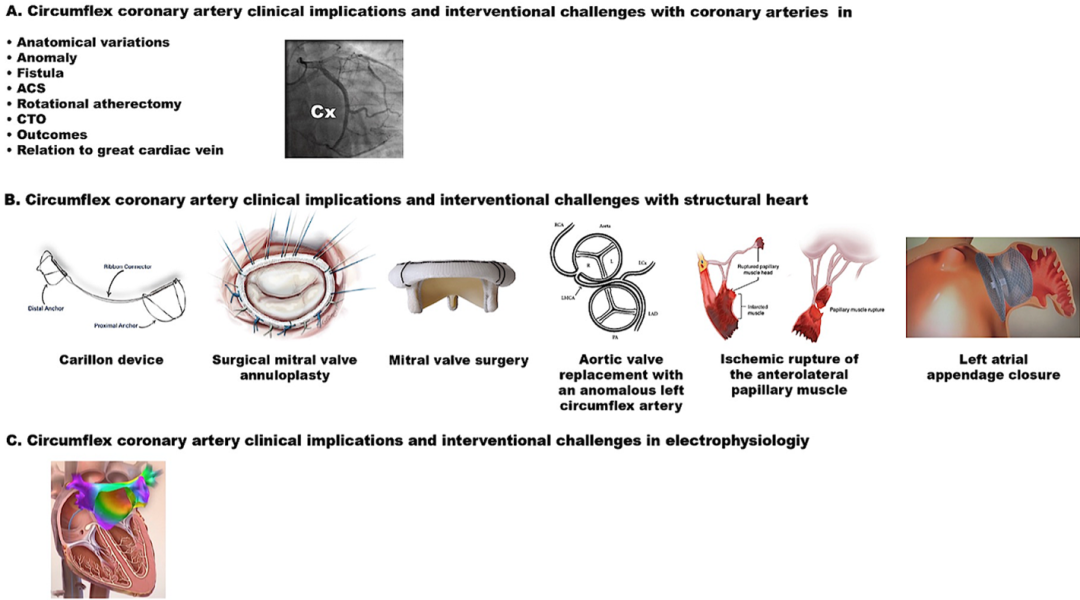
结构性心脏病诊疗中:LCX是易被忽视的操作雷区
二尖瓣修复、主动脉瓣置换、左心耳封堵等结构性心脏病介入/外科治疗中,LCX因走行于左房室沟,成为操作中最易发生医源性损伤的冠脉,且该类损伤多为致命性,需术前充分评估、术中密切监测、术后及时干预。
(一)二尖瓣瓣环成形术的高风险操作
二尖瓣瓣环成形术可导致LCX的医源性损伤,尤其在冠脉主动脉异常起源的人群中风险更高——因LCX行于左房室沟内,瓣环成形操作易导致其机械性闭塞,该并发症虽可预判,但目前文献中对其描述不足,发生率尚未明确。
术前心脏CTA成像可帮助制定诊疗策略,是降低损伤风险的关键:对于该类解剖变异患者,二尖瓣修复难度极高,可考虑使用部分瓣环成形环/带;若修复的耐久性不受影响,可选择非切除技术;避免瓣环操作的微创策略(如经心尖人工腱索植入)是合理的替代方案。
(二)二尖瓣外科手术的损伤高发
左优势型冠脉循环人群中,二尖瓣修复术后的LCX医源性损伤更常见,损伤机制主要为盲目的瓣环成形缝合结扎或LCX扭结,临床可表现为早期ST段改变、恶性室性心律失常和节段性室壁运动异常,属于危及生命的并发症。
心电图变化和术中冠脉造影是诊断的核心手段,治疗方案包括补救性PCI和紧急冠脉旁路移植术;特定情况下,重新定位器械或移除瓣环成形环是必要的干预措施。
(三)Carillon装置经导管间接二尖瓣瓣环成形术的距离
利用Carillon装置行冠状窦为基础的间接二尖瓣瓣环成形术时,LCX受压或闭塞是已明确的并发症,操作中需格外谨慎以避免该损伤。一项纳入25例患者的回顾性心脏CTA分析研究明确了LCX受损的预测指标:装置远端着陆区的冠状窦-LCX距离<8.6mm时,LCX受损的风险显著升高,该指标为术前评估提供了量化依据。
临床心绞痛症状、心电图变化和术中冠脉造影可帮助诊断LCX受损,治疗策略需个体化:重新定位Carillon装置;更换治疗策略(如经导管缘对缘修复Mitral Clip);LCX支架植入;无症状患者可选择保守治疗。
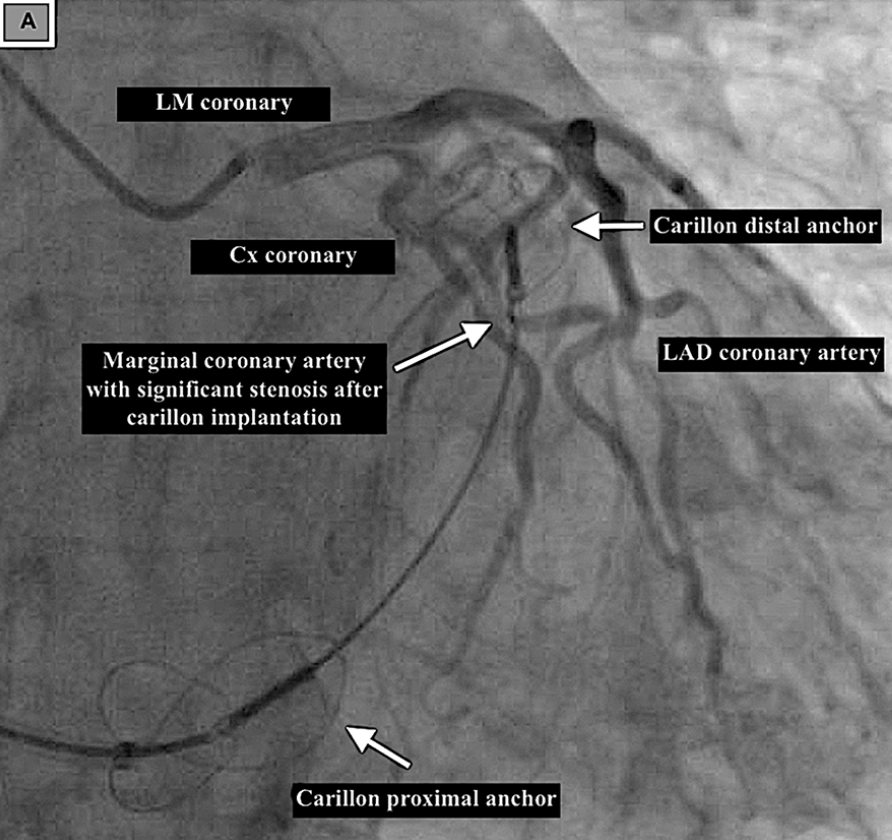
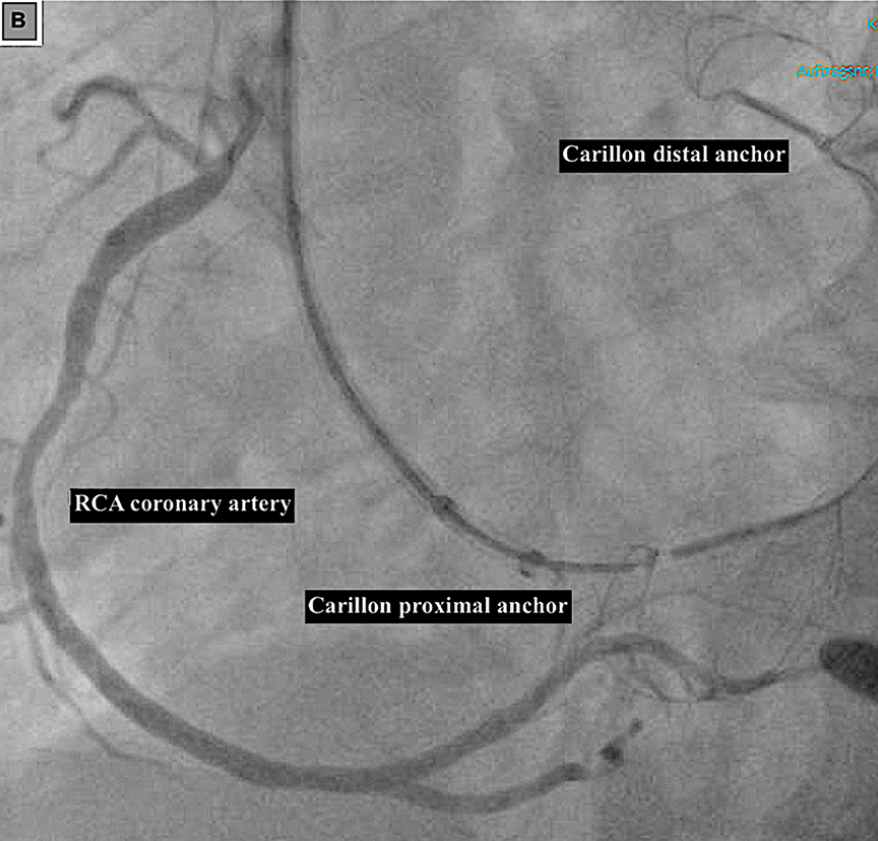
冠状动脉与Carillon装置植入的关系
(A)冠状动脉造影显示Carillon装置植入后回旋支冠状动脉边缘支存在明显狭窄。(B)冠状动脉造影显示右冠状动脉从Carillon装置旁走行。
(四)前外侧乳头肌缺血性断裂是LCX闭塞的罕见致命并发症
乳头肌断裂是心肌梗死后潜在的致命性机械并发症,死亡率极高,可导致重度二尖瓣反流、心源性休克和急性肺水肿。其血供特点决定了断裂的发生率:后内侧乳头肌由后降支单支供血,断裂发生率是前外侧乳头肌的6~12倍;而前外侧乳头肌由LAD和LCX双重供血,其断裂多与前外侧心肌梗死相关,LCX闭塞是重要的致病原因。
TTE诊断乳头肌破裂的敏感性为65%~85%,部分病例需经食管超声心动图(TEE)确诊,cMRI可帮助明确潜在病理机制。该并发症需紧急行外科或导管介入治疗,外科治疗包括二尖瓣修复或保留腱索的二尖瓣置换,且二尖瓣修复在改善左心室功能方面优于二尖瓣置换,是首选方案。
(五)LCX异常起源患者的外科主动脉瓣置换术(SAVR)
LCX起源于RCA或主动脉后走行的变异属于罕见的冠脉畸形,该类患者行SAVR时,需采用更小的器械,以避免压迫异常的LCX,防止致命性并发症的发生。术前心脏CTA成像是必须的检查手段,可清晰显示LCX的起源、走行及与周围结构的空间关系,为器械选择和操作规划提供依据,改善诊疗结局。
(六)左心耳封堵(LAA)需规避LCX损伤
经导管和外科左心耳封堵操作均可能损伤LCX,术前精准评估与术中操作把控是降低风险的关键。一项纳入116例患者心脏CTA扫描的研究定义了封堵装置的着陆区平面(与左心耳开口平行,与LCX起始段垂直),并明确:着陆区距左心耳开口越远,LCX损伤风险越低,装置与LCX距离<2mm时为高危情况(占所有病例的30.2%)。
术前心脏CTA成像可明确LCX与周围结构的空间关系,为装置选择和着陆区规划提供依据;术中心电图变化和冠脉造影可帮助诊断LCX损伤,治疗策略包括重新定位装置或更换封堵机制。
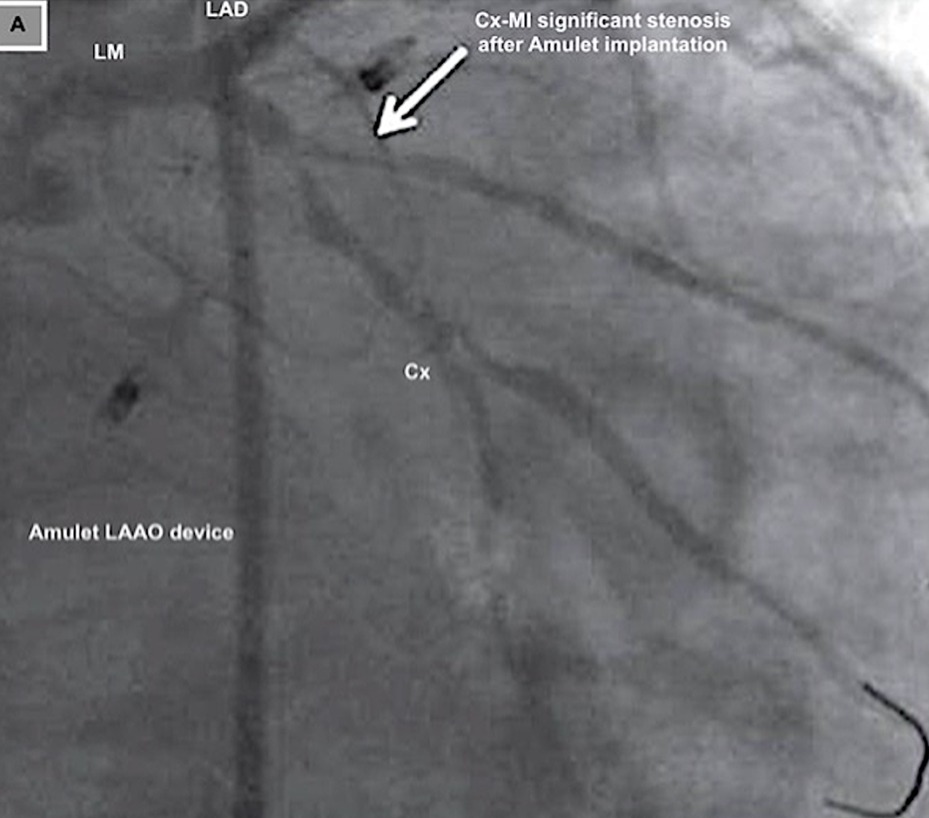
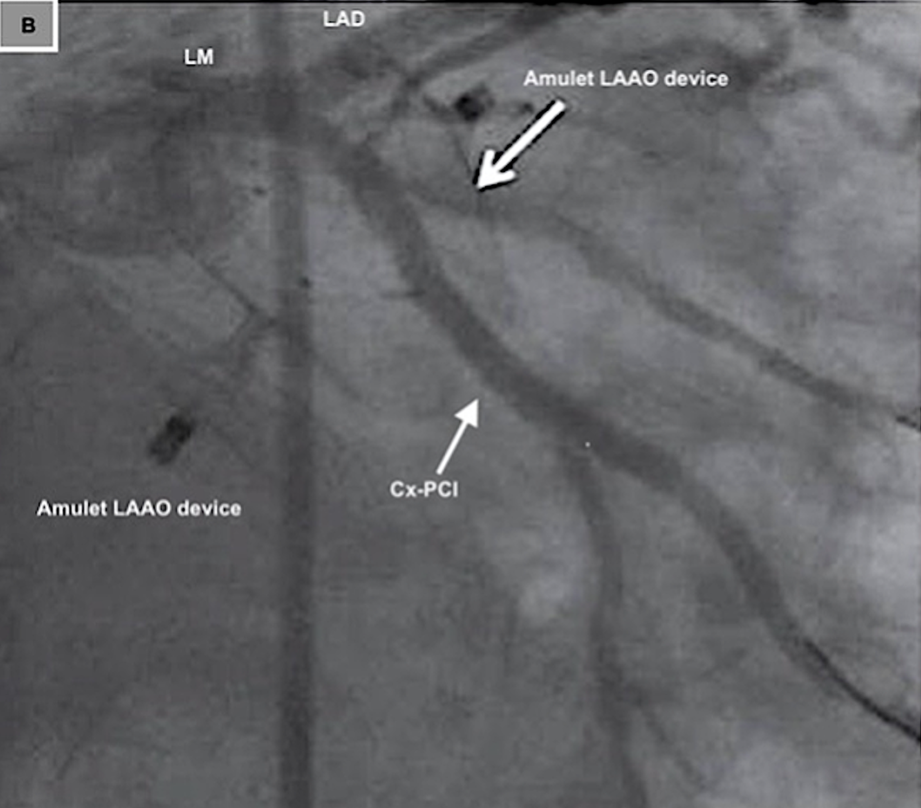
Amplatze左心耳封堵术与左冠状动脉的关系
(A)使用Amplatzer装置的左心耳封堵术已完全展开。冠状动脉造影证实,在植入后,回旋支-M1冠状动脉存在明显狭窄。(B)回旋支-经皮冠状动脉介入治疗
临床病例报告也证实了该损伤的可干预性:一例59岁患者行Amulet装置左心耳封堵时,因装置压迫导致LCX近端重度狭窄,出现下壁ST段抬高,重新将装置深入左心耳开口并联合LCX-PCI后,狭窄完全解除;另一例患者行二尖瓣、三尖瓣手术联合AtriClip装置左心耳封堵后24小时,因装置压迫导致LCX闭塞引发心肌梗死,经LCX-PCI后狭窄显著改善。
因此,外科操作中需将AtriClip装置放置于远离左心耳基底部的位置,避免LCX闭塞。
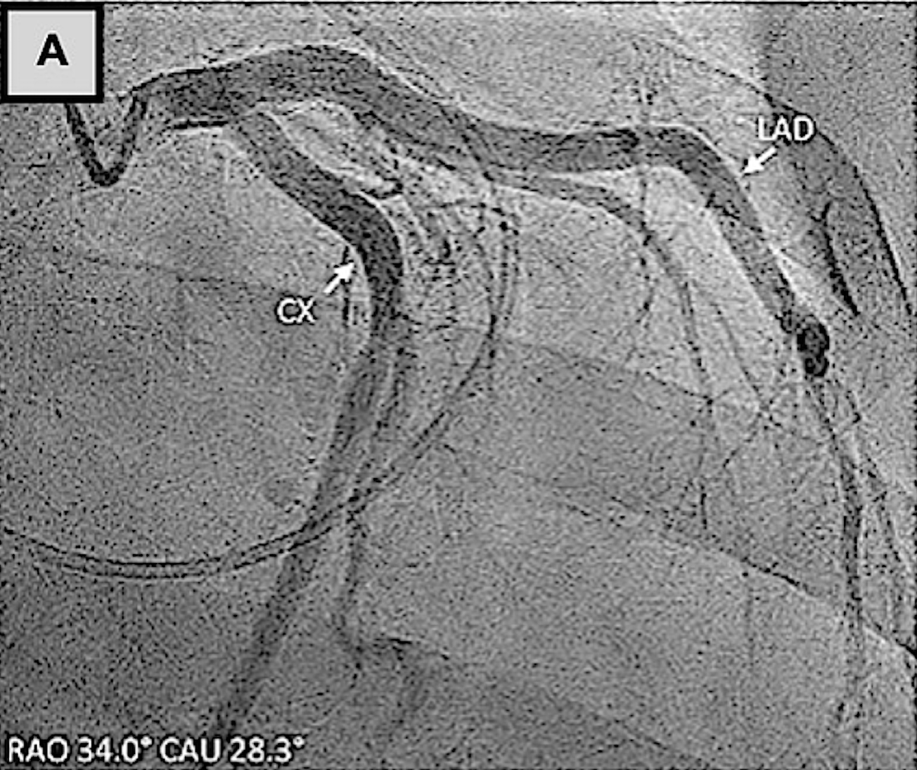
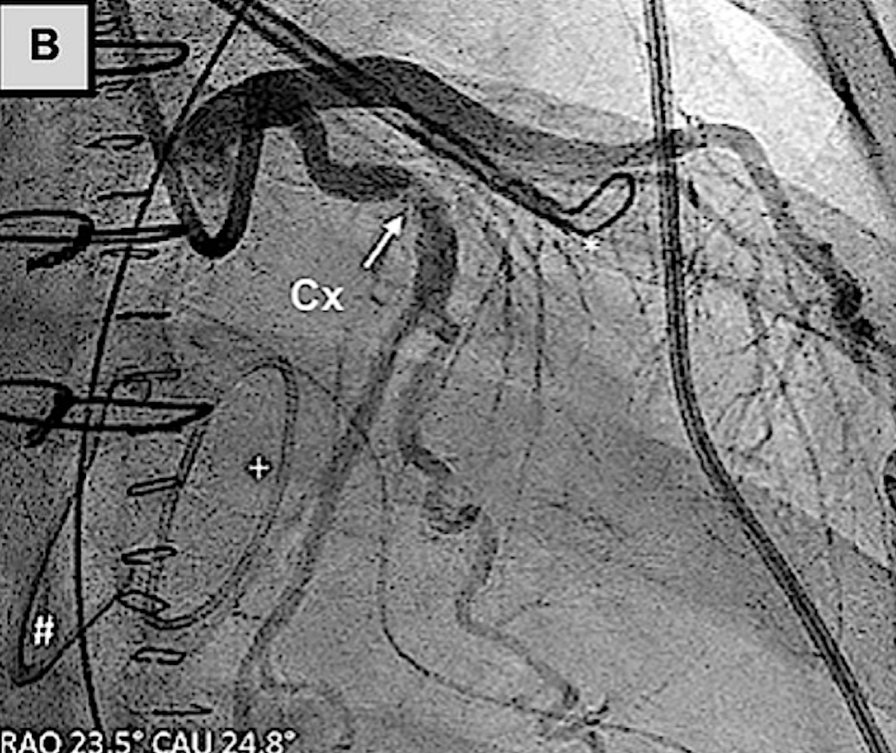
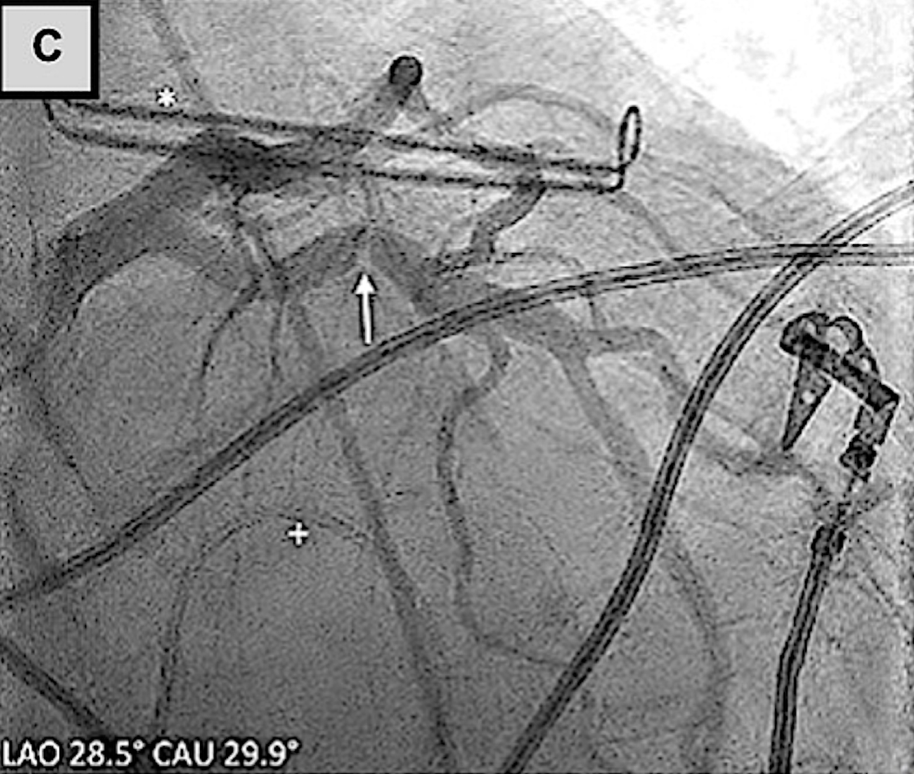
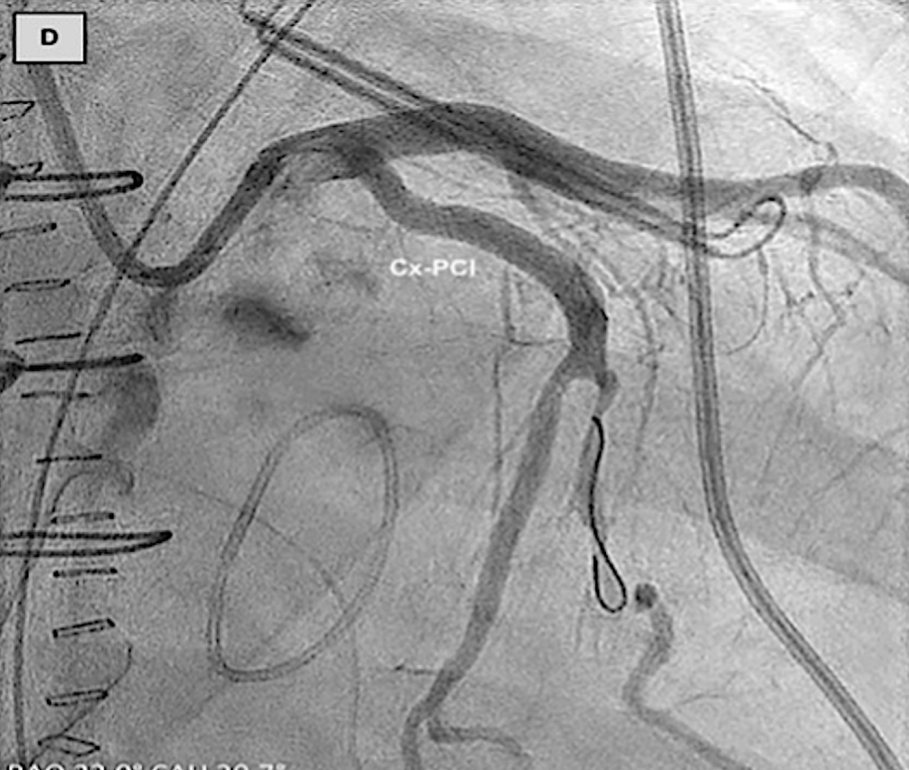
AtriClip左心耳封堵术与左冠状动脉的关系
(A)术前冠状动脉造影显示回旋支狭窄不显著。(B、C)使用AtriClip装置进行左心耳封堵术后,冠状动脉造影证实回旋支存在显著狭窄。(D)回旋支经皮冠状动脉介入治疗后,冠状动脉造影显示血管造影结果良好
04
电生理操作中LCX损伤虽罕见,却可致命
射频消融是心律失常的核心治疗手段,虽LCX损伤的发生率极低,但一旦发生,可导致危及生命的严重并发症,临床中需高度警惕。
一项纳入5709例房颤射频消融患者的研究显示,LCX损伤的发生率仅为0.14%(8例),病理标本分析显示,损伤部位与冠状窦远端和左心房前壁的LCX走行密切相关。该并发症虽罕见,但可诱发恶性室性心律失常和急性窦房结功能障碍,甚至需要永久起搏,因此操作中保持警惕并采用低功率设置,是降低冠脉损伤风险的关键。
临床病例也为电生理操作中LCX的保护提供了参考:一例16岁预激综合征合并室上速患者,行左外侧区域射频消融时,因消融导管与LCX距离过近,引发LCX痉挛导致可逆性ST段抬高,更换冷冻消融技术后,旁路传导成功消除,未发生严重并发症。
cMRI可帮助制定消融策略,术中心电图变化和冠脉造影是诊断LCX损伤的核心手段,治疗策略包括术中使用解痉药物、更换消融策略、LCX支架植入,及时干预可有效避免不良预后。
05
影像学是LCX诊疗的眼睛
LCX的解剖复杂性、损伤隐匿性和诊疗高风险性,决定了影像学在其全程诊疗中的地位——从初始快速评估到精准诊断,从术前规划到术中监测,从并发症识别到术后随访,各类影像学技术各有优势与局限性,临床中需合理选择、联合应用,实现对LCX的全面评估。
(一)TTE与TEE
TTE是初始快速评估的首选手段,可清晰显示左心室节段性运动异常、缺血性二尖瓣反流、LCX区域血肿,以及LCX-PCI后心大静脉损伤引发的心包积液,为快速诊断提供依据。
TEE的准确性和分辨率高于TTE,适用于TTE诊断不明确的病例(如乳头肌破裂的确诊)。
二者均为无创、便捷的影像学手段,可在床旁快速实施,是临床一线的评估工具。
(二)冠脉造影
冠脉造影是评估冠脉解剖的金标准,可清晰显示LCX的起源、走行、狭窄程度和瘘口引流部位,但其局限性在于需结合3D重建信息,尤其对于LCX与周围结构的空间关系,单纯造影难以全面评估,需联合其他影像学技术。
(三)心脏CTA
心脏CTA是LCX诊疗中最具价值的无创影像学技术之一,具有高分辨率、多平面成像/重建能力和广阔的视野,可清晰显示LCX的解剖结构、与周围心脏结构的空间关系、斑块成分和钙化程度,为术前规划(如CTO-PCI、结构性心脏病操作)提供详细的解剖和形态学信息。
心电门控心脏CTA可快速实施,有效避免运动伪影;其局限性为存在电离辐射和造影剂暴露,但可通过多种技术将辐射剂量降至最低。
多平面重建和3D重建技术可精细展示心脏结构,尤其在二尖瓣环钙化(MAC)患者中,心脏CTA可分析其与LCX的解剖关系、钙化范围、MAC严重程度,以及冠脉受压和心肌浸润的风险,为二尖瓣介入治疗的术前规划和风险分层提供依据。
(四)心脏磁共振(cMRI)
cMRI是另一项核心的无创影像学技术,无需电离辐射,可通过多种序列实现多维度评估:无需造影剂的导航门控3D全心稳态自由进动(SSFP)序列可获取解剖信息;亮血(电影SSFP)或黑血(双反转恢复)序列可进一步明确解剖结构;相位对比速度编码序列可量化血流;负荷灌注成像可检测心肌缺血;延迟增强MRI序列可识别心肌梗死灶。
cMRI的局限性为检查时间长、部分患者需镇静、易出现伪影,且部分检查需使用钆基造影剂,但可通过相关技术在不降低诊断质量的前提下减少造影剂用量。
(五)腔内影像学(IVUS/OCT)
IVUS和OCT是冠脉介入中的核心影像学技术,可在术中清晰显示LCX的血管壁结构、斑块成分、钙负荷程度、夹层和血栓,为减容策略选择、支架植入和并发症识别提供实时依据,显著提高介入操作的安全性和有效性。
临床中需根据具体诊疗场景,合理选择影像学技术并联合应用,实现对LCX的全面、精准评估,这是降低诊疗风险、改善预后的关键。
06
被低估的LCX,却是伤害我最深
在临床工作中,我们因对LAD、RCA的高度关注,而忽视了LCX,其解剖的复杂性、操作的高风险性、损伤的隐匿性,都要求我们彻底重塑对LCX的诊疗思维。
LCX的损伤并非不可避免,而是可预判、可识别、可干预。临床中多数LCX相关的不良事件,源于医师对其解剖特点和操作风险的认知不足,如左优势型人群二尖瓣手术中对LCX的保护不足、旋磨术中对开口钙化病变的操作不当、左心耳封堵中对着陆区的规划不合理等。只要我们在术前充分评估、术中密切监测、术后及时干预,就能最大限度减少LCX损伤的发生,改善患者预后。
对待LCX,我们需怀有更多的敬畏之心。通过充分的影像评估和精细的操作规划,让这位低调的被低估的LCX,不再成为伤害我最深的隐形陷阱,方能真正改善患者预后。