

GLP-1受体激动剂已被证实可降低2型糖尿病患者的主要不良心血管事件(MACE)及肾脏风险。替尔泊肽作为同时激动GLP-1与GIP受体的双靶点药物,在降糖和减重方面优于传统GLP-1类药物,并可改善多项代谢危险因素。SURPASS-CVOT研究是首个采用活性药物对照的肠促胰素类大型临床试验,结果显示,在心血管死亡、心肌梗死或卒中构成的三项复合终点上,替尔泊肽相较于GLP-1受体激动剂度拉糖肽具有非劣效性(P<0.001)。然而,糖尿病患者的疾病负担远不止于MACE事件,心力衰竭、冠脉血运重建及肾功能恶化同样显著影响患者预后。而在SURPASS-CVOT研究中,更广泛范围的心血管-肾脏不良结局尚未被系统报告。
2026年3月28日,《JAMA Cardiology》在线发表了一项基于SURPASS-CVOT随机临床试验的事后分析,系统评估了替尔泊肽与度拉糖肽在更广泛心血管-肾脏结局中的差异。本次分析在既有终点基础上进一步扩展至包含6组成分心血管-肾脏复合终点,以更全面反映患者的整体风险负担。3月29日,Steven E. Nissen教授代表SURPASS-CVOT研究者在2026年美国心脏病学会年会(ACC.26)上同步公布了该研究结果,为肠促胰素类药物在心-肾-代谢(CKM)一体化管理中的应用提供了新的证据。
研究设计——全球多中心RCT的事后分析
本研究为SURPASS-CVOT研究的事后分析。SURPASS-CVOT研究是一项国际多中心、随机、双盲、活性对照临床试验,于全球640个中心开展,共纳入13,165例2型糖尿病合并已确诊ASCVD的患者。受试者平均年龄为64岁,男性占71.0%,平均HbA1c为8.4%,中位随访时间为46.9个月。参与者按1:1比例随机分配至两组:替尔泊肽组(6,586例):皮下注射,起始剂量2.5 mg/周,每4周递增,最大剂量15 mg/周;度拉糖肽组(6,579例):皮下注射,固定剂量1.5 mg/周。
本研究的主要终点为6项心血管-肾脏复合终点,包括全因死亡、心肌梗死、卒中、冠脉血运重建、因心力衰竭住院及肾脏复合终点。上述终点在原试验中均已预先收集,其中除肾脏终点外,其余事件均由独立盲态终点委员会进行中心化裁定。敏感性分析通过不同终点组合形式评估结果稳健性。
研究结果
(1)基线特征——事件人群呈典型高风险特征
在两组人群中,发生终点事件的患者表现出一致的高风险特征,包括年龄较大、男性比例更高、基线肾功能较差以及既往心血管事件负担更重,同时白蛋白尿及吸烟比例亦更高。两组在体重指数及HbA1c方面未见明显差异。上述结果与既往心血管结局试验及流行病学研究观察一致。
(2)主要终点——6项心血管-肾脏复合终点差异显现
在中位随访4年后,替尔泊肽组共有1,559例患者(23.7%)发生主要终点事件,而度拉糖肽组为1,803例(27.4%)。替尔泊肽组事件风险显著降低16%(HR 0.84;95% CI 0.79–0.90;P < 0.001),绝对风险降低3.7%,对应的需治疗人数为27,即每治疗27名患者可避免1例不良事件发生。
Kaplan-Meier曲线显示,两组事件发生率在随访过程中逐渐分离,并随时间推移持续扩大,显示出替尔泊肽在长期心肾保护方面的优势。
(3)各单项终点分析——死亡与肾脏结局贡献主要差异
对复合终点各组成部分的分析显示,替尔泊肽在多数终点上均呈现方向一致的风险降低趋势。其中,全因死亡风险降低16%(HR 0.84;95% CI 0.75–0.94),肾脏复合终点风险降低21%(HR 0.79;95% CI 0.68–0.91),二者对整体复合终点的获益贡献最大。而卒中及心力衰竭住院的风险比虽在数值上倾向于替尔泊肽,但其95%置信区间跨越1.0,未达到统计学显著性水平。
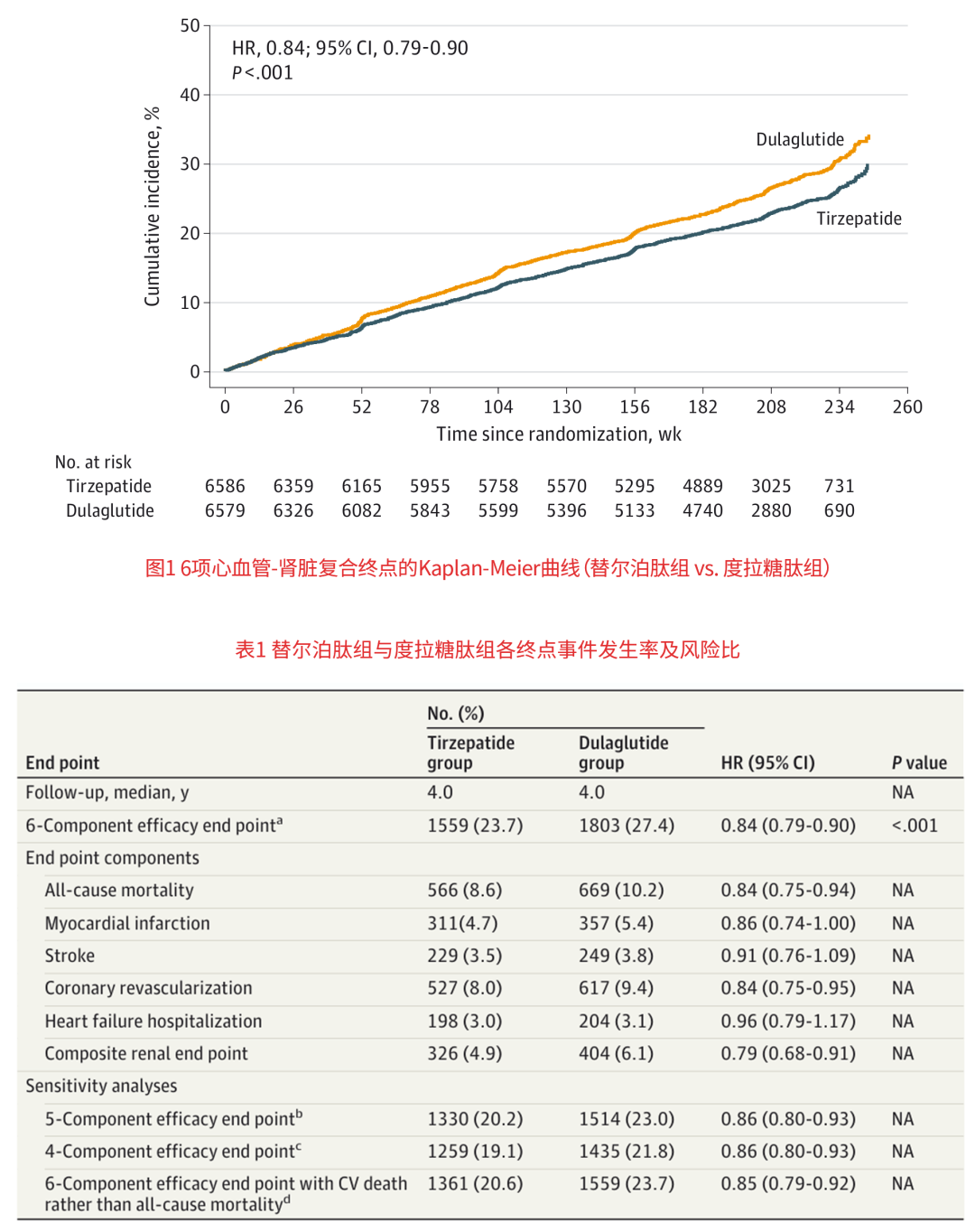
(4)敏感性分析——不同终点定义下结果一致
为验证结果的稳健性,研究者进行了多项敏感性分析:
5项复合终点(排除肾脏终点):替尔泊肽组1,330例(20.2%) vs. 度拉糖肽组1,514例(23.0%),HR = 0.86(95% CI:0.80–0.93);
4项复合终点(排除肾脏及心力衰竭终点):替尔泊肽组1,259例(19.1%) vs. 度拉糖肽组1,435例(21.8%),HR = 0.86(95% CI:0.80–0.93);
6项复合终点(以心血管死亡替代全因死亡):替尔泊肽组1,361例(20.6%) vs. 度拉糖肽组1,559例(23.7%),HR = 0.85(95% CI:0.79–0.92)。
在不同终点定义下的敏感性分析结果与主要分析保持一致。无论采用5项或4项复合终点,替尔泊肽均显示出相似方向及幅度的风险降低,支持主要结果的稳健性。
(5)亚组分析——整体一致,未见明确交互作用
在预设的亚组分析中,替尔泊肽的获益在各亚组中总体一致,包括性别、年龄、种族、基线HbA1c水平等。仅在体重指数(BMI)亚组中观察到边际显著的交互作用,但该交互作用未达到统计学显著性水平,应谨慎解读。
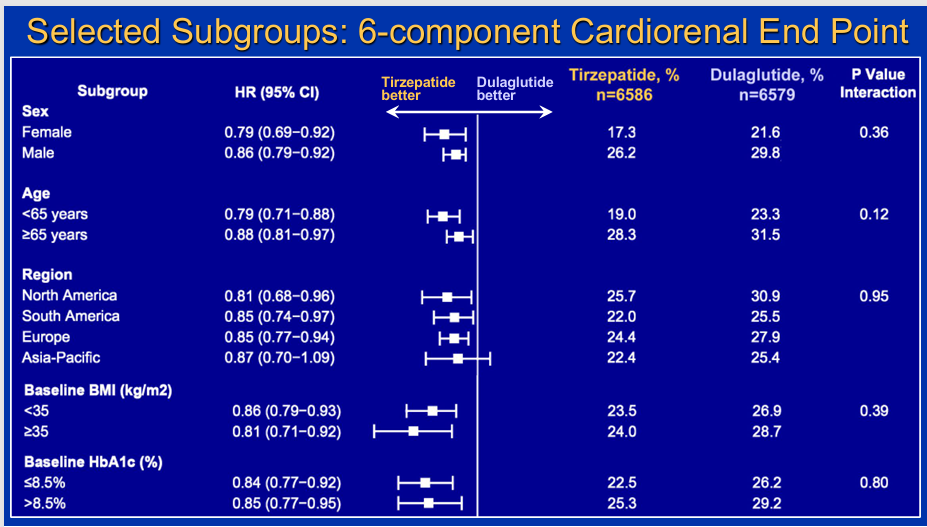
图2 6项心血管-肾脏复合终点的亚组分析森林图(替尔泊肽组 vs. 度拉糖肽组)
(6)安全性分析——胃肠道反应增加,总体安全性可控
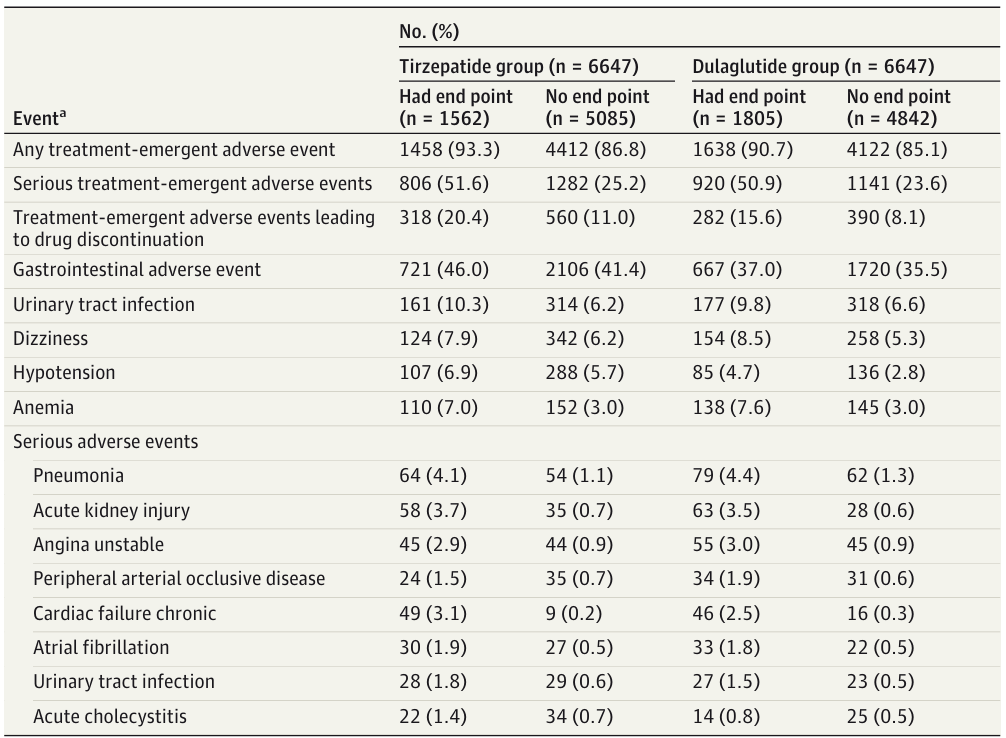
安全性方面,替尔泊肽组的胃肠道不良事件发生率更高(42.5% vs. 35.9%),因不良事件导致停药的比例也略高(13.2% vs. 10.1%),两组在其他不良事件方面未见显著差异,未发现新的安全性信号。
表2 发生与未发生心肾终点事件的受试者不良事件发生率
为何需要更广泛的终点评价
传统三组分MACE虽然是监管层面通用且被广泛接受的复合终点,但在CKM综合征的疾病框架下,其覆盖面的局限性日益凸显。2023年美国心脏协会(AHA)发布的主席建议明确提出了心血管-肾脏-代谢综合征的概念,强调肥胖、糖尿病、慢性肾病和心血管疾病之间的病理生理学关联。肥胖和糖尿病患者面临的不良结局远不限于动脉粥样硬化事件,还包括冠脉血运重建需求、心力衰竭住院、肾脏疾病进展,以及感染和恶性肿瘤导致的非心血管死亡。
从数据结构看,复合终点获益的主要驱动因素包括:全因死亡(HR 0.84)、冠脉血运重建(HR 0.84)和复合肾脏终点(HR 0.79)。其中,肾脏终点21%的相对风险降低是所有组分中效应量最大的,这与主试验中eGFR斜率改善的结果相呼应,提示双靶点肠促胰素治疗可能具有独立于心血管保护之外的肾脏获益。敏感性分析验证了结果的稳健性:剔除肾脏终点的五组分复合终点(HR 0.86)、剔除肾脏和心衰终点的四组分终点(HR 0.86)、以心血管死亡替代全因死亡的六组分终点(HR 0.85),均显示一致的获益方向。亚组分析未发现显著的交互作用。
需要注意的是,心衰住院终点未显示统计学差异(HR 0.96; 0.79–1.17),这与SUMMIT试验中替尔泊肽在射血分数保留型心衰(HFpEF)合并肥胖患者中展现的显著获益(复合心衰恶化事件HR 0.54)形成对照。两项研究之间结果差异的可能原因包括SURPASS-CVOT的入组人群并非以心衰为主要特征、基线心衰比例相对较低(约20%)以及心衰住院事件数量有限导致统计效力不足。
研究意义及局限性
本研究在活性药物对照背景下,将终点由传统3项MACE扩展至更广泛的心血管-肾脏复合终点,从而更全面地反映糖尿病合并ASCVD患者的整体疾病负担。结果显示,与度拉糖肽相比,替尔泊肽在多个终点上均呈现方向一致的风险降低趋势,提示其可能具有多维度的临床获益。
在各组成终点中,全因死亡及肾脏复合终点的结果尤为值得关注。既往多项GLP-1受体激动剂的安慰剂对照试验虽已证实其可降低心血管事件,但对全因死亡的影响并不一致。本研究在活性对照背景下观察到相关信号,提示双靶点激动剂在生存结局方面可能具有潜在优势。同时,肾脏复合终点所呈现的风险下降趋势,也提示其在肾脏保护方面具有进一步探索价值。
本研究具有一定的局限性。首先,本研究为基于原始随机试验的事后分析,而原试验的主要终点为相对较窄的复合终点,因此该类分析在一定程度上可能受到已知主要结局结果的影响,从而对扩展终点的构建带来潜在偏倚。同行评议的随刊编辑评论(Fonarow和McMurray)明确指出:“最终的确定性答案需要以优效性为目标、针对特定获益路径的专门设计的结局试验” 。其次,本研究纳入的均为已确诊ASCVD的高危患者,因此相关结果在低风险人群中的适用性仍有待进一步验证。最后,由于采用了更广泛的复合终点,事件数量较原始试验明显增加(约为其两倍),从而提高了统计学效能,但这一效能水平并非原试验设计时的预设目标。
展望——CKM一体化管理时代正在到来
在这项基于SURPASS-CVOT随机临床试验的事后分析中,替尔泊肽与较低的广泛心血管-肾脏复合终点风险相关,为糖尿病合并心血管疾病患者的治疗选择提供了更为全面的循证依据。
基于REWIND数据的间接估算提示替尔泊肽较安慰剂的MACE HR约为0.72,优于LEADER(利拉鲁肽,HR 0.87)和REWIND(度拉糖肽,HR 0.88),但间接比较的不确定性极大,不应作为治疗决策的依据。2025年发表于Nature Medicine的一项大规模真实世界研究(约100万成人)发现,在2型糖尿病患者的临床实践中,司美格鲁肽和替尔泊肽的心血管保护效果相当(HR 1.06; 95% CI 0.95–1.18)。这提示在心血管硬终点方面,两种药物可能并无临床上显著的差异。SURMOUNT-MMO(NCT05556512)是正在进行中的一项安慰剂对照试验,计划纳入约15,000例肥胖合并心血管疾病或高危因素但不伴糖尿病的患者,采用五组分复合终点,预计2027年10月获得结果。这项试验将为替尔泊肽的心血管获益提供最终的确证性证据。
随着肠促胰素类药物的不断发展,这类治疗正逐步从单一代谢控制手段,向同时覆盖心血管、肾脏及代谢多重风险的综合干预策略转变。当前,多种高效肠促胰素类药物已进入临床应用阶段,且仍有新型药物在持续研发中。总体而言,这类治疗为改善患者多维度临床结局提供了新的可能,也进一步支持心-肾-代谢一体化管理模式的发展,其在不同风险人群中的长期获益仍有待未来研究进一步明确。
参考文献:
⇅ 向上滑动阅览