

急性ST段抬高型心肌梗死(STEMI)的治疗核心在于尽早恢复冠状动脉血流。尽管以直接经皮冠状动脉介入为代表的再灌注策略显著改善了患者预后,但前壁STEMI患者仍存在较高残余风险。既往研究显示,梗死面积是决定预后的关键指标,每增加1%,一年内死亡及心衰住院风险分别增加约3.8%和4.0%。因此,在快速再灌注基础上进一步减少心肌损伤,仍是当前研究的重要方向。
在此背景下,“先卸载,后开通”(door-to-unload)策略逐渐受到关注。该策略通过经导管微轴流泵(TV-mAFP)在再灌注前进行左心室机械卸负荷,以降低心肌耗氧、改善冠脉灌注并减轻再灌注损伤。动物实验显示,再灌注前约30分钟的左室卸负荷可显著减少梗死面积。然而,这一基于实验模型的机制性获益是否能够转化为临床疗效,尚缺乏随机对照研究证据。STEMI-Door to Unload(STEMI-DTU)随机对照临床试验正是为回答这一关键科学问题而设计。2026年3月28日,ACC 2026会议上,西奈山伊坎医学院的Gregg W. Stone教授公布了STEMI-DTU研究的主要结果,为临床实践提供重要参考。
研究设计与方法
STEMI-DTU研究是一项前瞻性、多中心、随机、开放标签对照试验,旨在系统评估在无心源性休克的前壁STEMI患者中,相较于立即PCI策略,左室机械卸负荷联合延迟PCI策略是否能够有效减少梗死面积。
该研究在全球70个中心开展,涵盖美国、德国、意大利、瑞士、加拿大及英国,入组时间为2019年12月至2024年9月。研究纳入标准包括:年龄18~85岁、首次心肌梗死、发病1~6小时内就诊的前壁STEMI患者并具备PCI指征;排除标准包括:心源性休克或机械并发症、既往心肌梗死或冠脉重建史、既往接受溶栓或机械循环支持、以及存在Impella装置或心脏磁共振(CMR)检查禁忌等。最终,研究共纳入527例患者,按1:1随机分配至治疗组(262例)与对照组(265例)。治疗组在导管室内首先置入Impella CP装置并启动左室卸负荷,在机械支持下延迟至少30分钟后再行PCI,同时要求泵支持时间不少于4小时;对照组则接受标准的立即PCI治疗。两组基线特征总体均衡,平均年龄为61±11岁,男性占79.1%。
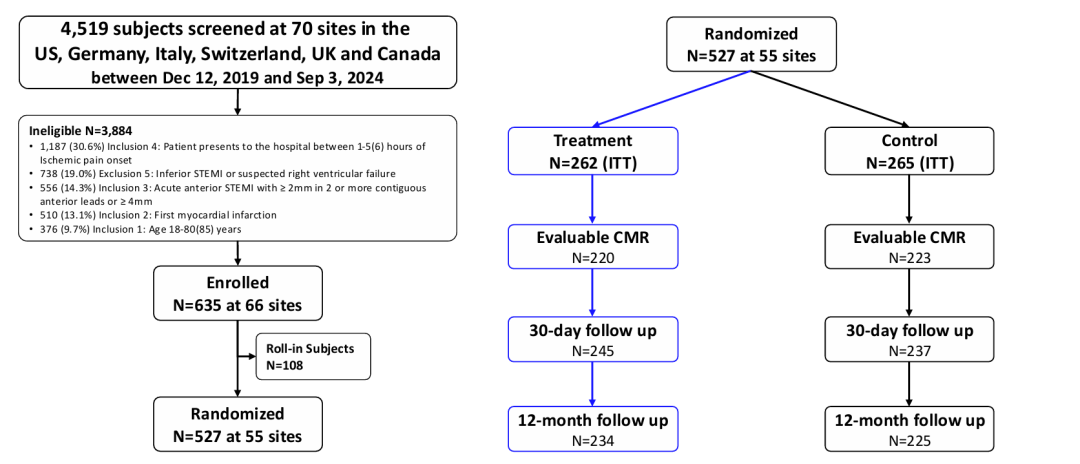
图1 STEMI-DTU研究患者筛选、入组及随机分组流程
主要终点为术后3至5天通过CMR评估的梗死面积(占左心室质量百分比)。关键次要终点为分层复合终点,包括心血管死亡、心源性休克、心力衰竭、器械治疗需求及梗死面积,采用Win Ratio方法分析。安全性终点为30天内治疗相关的BARC 3~5级出血或主要血管并发症发生率,并设定26.5%作为预设性能目标。
研究结果
(1)主要终点:梗死面积未见改善,策略未达预期
在意向性治疗分析中,治疗组的平均梗死面积为30.8% ± 16.2%,对照组为31.9% ± 16.9%,两组间差异无统计学意义(平均差异 -1.1%,95%置信区间 -4.2%至2.0%,p = 0.50)。在符合方案分析中,结果保持一致:治疗组为31.8% ± 16%,对照组为33.7% ± 16%,p = 0.28。23个预设亚组分析中,治疗效应在所有亚组间保持一致——没有任何亚群显示出统计学上有意义的获益信号。
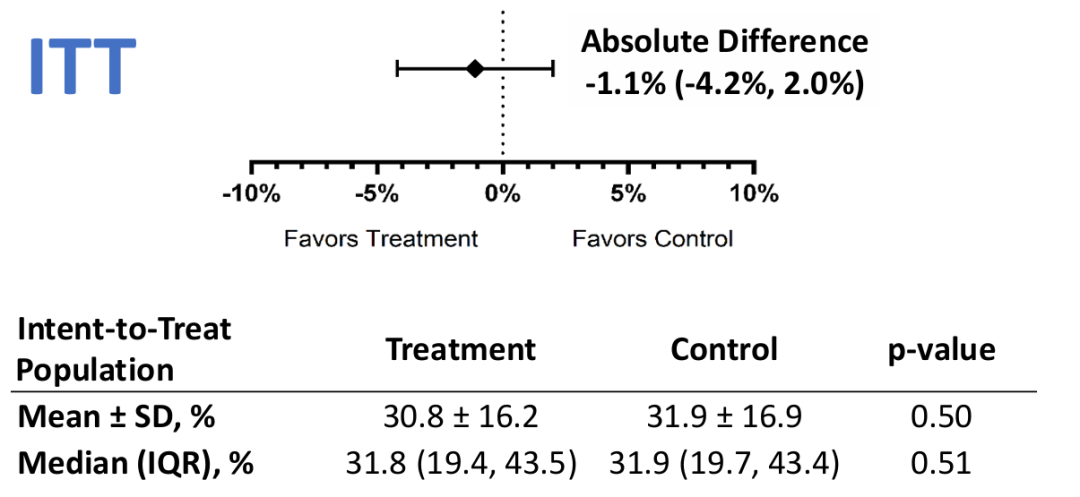
图2主要终点分析
治疗组由于策略性延迟再灌注,总缺血时间显著延长(中位212分钟 vs 165分钟,p < 0.0001),延迟时间约47分钟。尽管缺血时间延长,治疗组并未观察到梗死面积进一步增加,提示左室卸负荷可能在一定程度上抵消了延迟再灌注带来的不利影响,但这一作用未能转化为优于标准治疗的净获益。
(2)次要复合终点分析:未见显著获益
在关键次要复合终点方面,治疗组相较于对照组的Win Ratio为1.04(95%置信区间 0.84至1.28,p = 0.73),同样未显示出统计学差异。30天及12个月随访中,两组在全因死亡、心血管死亡及心力衰竭住院等临床结局方面亦无显著差异。
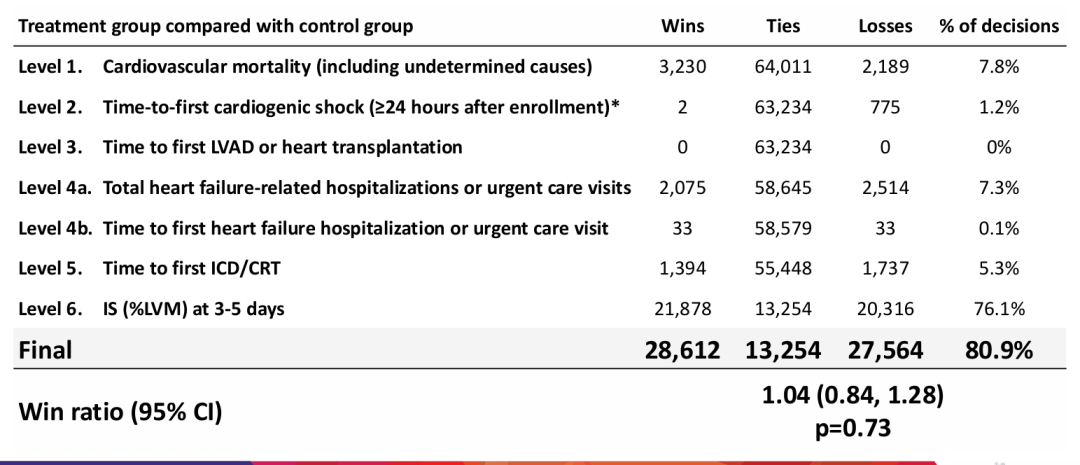
图3 次要终点分析
(3)安全性:出血与血管并发症显著增加
安全性分析是本研究最为关注的重点之一。治疗组中与设备或操作相关的BARC 3~5级出血或主要血管并发症的发生率为30.8%(95%置信区间 25.2%至36.8%),数值上高于预设的26.5%性能目标(p = 0.95),提示该策略未达到预设安全性要求。相比之下,对照组中该类事件的发生率仅为6.0%,两组间差异具有统计学意义。
治疗组中的出血事件以穿刺部位相关为主。多因素分析显示,出血风险主要与操作相关因素(如血管闭合技术)相关,而非基线血流动力学状态,提示出血并发症具有一定可干预性。在262例治疗组患者中,共有83例(31.7%)发生穿刺部位相关的出血或血管并发症。未见颅内出血,但发生一例致命性出血。此外,主要血管并发症(包括血肿、假性动脉瘤、动静脉瘘等)的发生率为5.0%。

图4 安全性分析
值得注意的是,事后分析显示,治疗组发生出血患者的12个月死亡率低于对照组(7.4% vs 31.6%)。这一看似矛盾的现象可能与出血类型的差异有关——治疗组出血绝大多数为穿刺部位出血,而对照组中发生出血的患者往往伴随更复杂的临床状况。然而,该结果基于有限事件数,且属于事后分析,应谨慎解读。
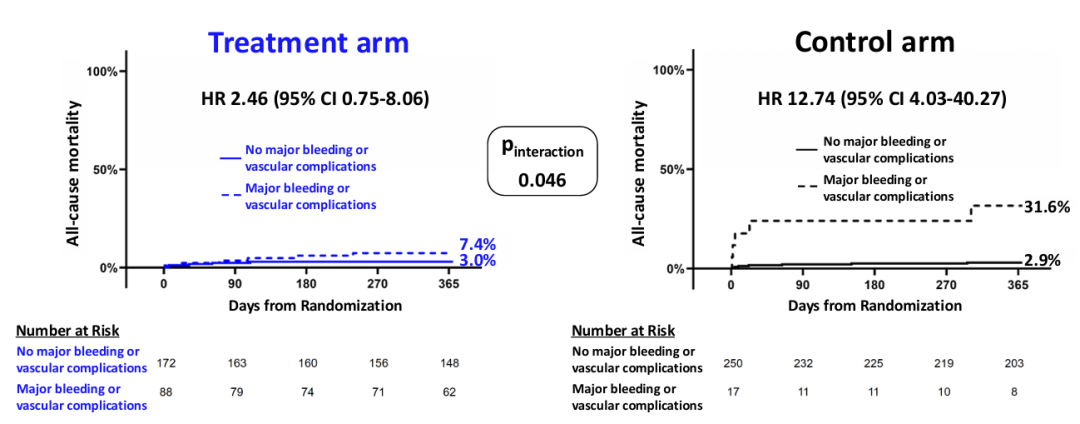
图5 主要出血/血管并发症与全因死亡风险的关系
(4)6个月心脏磁共振提示不良重构信号
6个月非增强CMR随访显示了一个值得高度关注的发现:治疗组的左室收缩末期容积(LVESV)为84.7±46.3 mL,显著大于对照组的75.2±40.6 mL(差异9.6 mL,95% CI: 0.8-18.4,P=0.033)。LVESV是心梗后不良心室重构的公认标志物,与远期心衰住院和死亡率密切相关。整个STEMI-DTU试验的出发点是卸载可减轻不良重构,但6个月数据提示干预可能反而促进不利方向的变化。尽管这一发现来自次要终点且需谨慎解读,但其从"中性"向"可能有害"方向的位移,对任何后续在非休克STEMI中探索Impella的设想构成了严肃的安全性警示。
机制悖论——有利的血流动力学,无效的心肌保护
STEMI-DTU最引人深思的发现之一是:Impella确实达到了预期的血流动力学目标——治疗组PCI前的主动脉舒张压显著更高(86.6 vs 77.3 mmHg,P<0.0001),计算的冠脉灌注压也显著升高(61.4 vs 52.5 mmHg,P=0.0005),且PCI前TIMI 0-1级血流的比例显著更低(55.9% vs 69.4%,P=0.0038),提示在30分钟的卸载期间,相当比例的患者出现了自发性再灌注。然而,这些有利的血流动力学改变并未转化为更小的梗死面积。
这一悖论至少有三层解释。第一,治疗组较高的自发再灌注率实际上削弱了"先卸载后再灌注"假设的前提——如果许多患者的冠脉在30分钟等待期间已经自行开通,那么所谓的"再灌注前心肌保护窗口"根本不存在。第二,人类STEMI的总缺血时间远超动物模型:本试验中位总缺血时间已达212分钟(治疗组),在此背景下额外30分钟的卸载仅是一个边际干预。第三,现代抗栓方案(普拉格雷/替格瑞洛+肝素)本身已可能捕获了Impella在未使用抗栓药物的动物模型中所提供的部分心肌保护效应,形成了"地板效应"。
最深刻的教训或许是:有利的血流动力学替代指标(灌注压升高、TIMI血流改善、室壁张力降低)是心肌保护的必要条件,但并非充分条件。再灌注损伤涉及活性氧、钙超载、线粒体通透性转换、中性粒细胞浸润和微血管阻塞等多条平行通路,单一的机械卸载策略不足以在人类STEMI中有效阻断这一级联反应。
再灌注损伤治疗的坟场——STEMI-DTU并不孤独
STEMI-DTU的阴性结果加入了一个已有四十年历史的名单。几乎所有针对心肌再灌注损伤的干预策略都遵循了相同的轨迹:动物模型中的显著获益→小样本先导试验的积极信号→大规模关键性试验的阴性结果。环孢素(CIRCUS,NEJM 2015,n=970,P=0.77)、远程缺血预适应(CONDI-2/ERIC-PPCI,Lancet 2019,n=5401,HR 1.10)、静脉美托洛尔(EARLY-BAMI,阴性)、治疗性低温、腺苷、缺血后适应,直至最近的冠脉内阿替普酶(STRIVE,TCT 2025,阴性)——STEMI-DTU为这一名单增添了一个机械策略的条目。
转化失败的根源是系统性的:再灌注损伤涉及过多平行通路,单一干预难以产生有意义的净效应;现代STEMI治疗已将梗死面积压缩至较低水平,留给附加干预的空间有限;动物模型的标准化条件与人类疾病的异质性之间存在不可弥合的差距。
为何动物实验的获益未能在临床复制?
应当公正地承认,STEMI-DTU拥有心肌保护领域迄今为止最系统、最具说服力的临床前证据体系。Kapur实验室在超过十年的系统研究中证实,在猪的急性前降支(LAD)闭塞模型中,Impella卸载30分钟后再灌注可将梗死面积减少约43-50%。该团队阐明了至少七种独立的保护机制,包括SDF-1α/CXCR4心肌保护通路的激活、冠脉侧支血流的增强和线粒体完整性的维护。Esposito等2018年发表于JACC的研究精确证明了"30分钟"是关键阈值——15分钟不够,再灌注后开始卸载则无效。
DTU-STEMI先导试验(Circulation 2019,n=50)确认了方案可行性。ITT分析未显示梗死面积差异(13.1% vs 15.3%,P=0.53),但per-protocol亚分析在LAD闭塞且完成完整卸载方案的33例患者中显示了有意义的梗死面积减少(IS/AAR 47% vs 60%,P=0.02)。然而,先导试验排除了36%的方案违反者——这一高比例预示了关键性试验中per-protocol人群与ITT人群之间可能出现的落差(关键性试验中实际差异达24.5%)。
临床转化失败的根源是多维度的:猪几乎没有冠脉侧支循环,在标准化条件下接受90分钟精确控制的LAD闭塞;而人类STEMI涉及数小时不等的缺血时间、异质性的侧支网络、合并症以及本身已具有心肌保护效应的强效抗栓治疗。从猪到人的效应量衰减是再灌注损伤领域反复出现的系统性现象,STEMI-DTU是这一规律的最新佐证。
出血终点的解读
30.8%的BARC 3-5级大出血率在血流动力学稳定的STEMI患者中无疑令人瞩目。但需要将这一数字置于合理的临床背景中。首先,方案设计要求所有患者在随机化前行股动脉造影以排除血管禁忌,导致两组均以股动脉入路为主(81.4%),远高于当代STEMI试验中桡动脉入路的普及率——这一方案要求本身即抬高了两组的基线血管并发症风险。其次,治疗组需经14Fr股动脉鞘管置入Impella CP,加之30分钟等待期内持续高剂量肝素抗凝、术前双联抗血小板治疗、以及Impella实际支持时间中位数长达10.4小时期间的持续抗凝暴露,加之部分中心的大口径血管闭合技术尚未完全成熟,出血的高发生率在很大程度上是方案设计和操作因素的叠加结果,而非器械本身固有缺陷的直接体现。这也意味着,随着血管闭合技术的改进和下一代更小口径pVAD(如9Fr入路的Impella ECP)的临床推广,出血风险方程有望从根本上改写。对照组仅在PCI术中接受短时抗凝。
一个耐人寻味的事后发现与DanGer SHOCK出血亚研究的结论相呼应:在发生出血事件的患者中,治疗组12个月死亡率反而低于对照组(7.4% vs 31.6%),而在无出血事件的患者中两组死亡率一致。这一"出血-死亡率悖论"可能反映了选择偏倚,但也提示:在MCS支持的患者中,出血事件的预后意义可能不同于无MCS支持的患者。这一观察为理解DanGer SHOCK中Impella获益的"出血耐受性"提供了跨试验的一致佐证。
从器械技术演进的角度看,下一代Impella ECP将入路鞘管降至9Fr,有望从根本上改善血管入路相关并发症。但核心的生物学问题仍然存在:如果有利的血流动力学效应本身不能缩小梗死面积,更小口径的器械在达到相似血流动力学效果的前提下也将面临相同的转化壁垒。
对Impella平台循证证据的影响
STEMI-DTU的阴性结果对Impella在非休克STEMI中的适应证拓展画上了句号。Impella的核心价值在心源性休克中已由DanGer SHOCK明确确立——12.7%的绝对死亡率降低(NNT=8),长期随访证实额外约600天的生存获益,2025 ACC/AHA指南将其在心源性休克中升级至2a类推荐。这一里程碑式的证据不受STEMI-DTU结果的影响。
这两项试验结局截然不同的核心解释在于血流动力学环境对泵效率的决定性影响。DanGer SHOCK入组的心源性休克患者前负荷高、后负荷低,恰恰是Impella泵效率最高的工作条件——装置能够最大限度地卸载左室并增加前向血流。而STEMI-DTU入组的血流动力学稳定患者基线平均收缩压高达143±25 mmHg,远高于临床前模型中的低血压条件,Impella需要对抗显著的高后负荷做功,实际泵效率可能大幅降低。试验方案虽推荐将收缩压控制至130 mmHg以下以优化卸载效果,但在急性STEMI的紧急场景中,这一目标的实际达成率仍有待亚组数据的进一步揭示。这一力学差异——而非器械本身的功能不足——是解释两项试验不同结局的关键,也为未来探索Impella联合积极降压预处理策略、在"高后负荷型"STEMI亚群中优化卸载效率提供了理论依据。
Impella ECP的关键性试验已在高危PCI适应证中展示积极数据,FDA审批推进中。PROTECT IV(高危PCI中1252例随机对照试验)是另一个重要催化性事件。STEMI-DTU实际上澄清了Impella的临床价值边界:其获益与患者疾病严重程度成正比——在血流动力学崩溃的心源性休克中挽救生命,在稳定的前壁心梗中缺乏额外获益。
结语:确立边界本身就是进步
STEMI-DTU给出了一个清晰而重要的答案:在非心源性休克的前壁STEMI中,Impella CP左室卸载30分钟联合延迟PCI不能缩小梗死面积,且以显著增加的出血风险和可能不利的6个月心室重构为代价。这一结果为左室卸载在急性心肌梗死中的应用划定了明确的循证边界。
但边界的确立本身就是医学进步的重要形式。STEMI-DTU是STEMI领域以CMR为终点的最大规模当代随机对照试验,其病理生理学数据——总缺血时间、PCI前乳酸水平和LVEDP作为梗死面积的独立预测因素——将指导未来的研究设计。对于Impella平台而言,STEMI-DTU与DanGer SHOCK共同构成了完整的循证图景:疾病越重,获益越大——这不是某一器械的局限,而是所有机械循环辅助技术的共同生物学原则。
尽管STEMI-DTU对"先卸载后再灌注"的特定方案给出了否定答案,但几个方向仍值得未来探索:针对SCAI B期前休克亚群的精准选择;Impella ECP(9Fr入路)对出血风险的根本性改写;以及在机械卸载基础上叠加靶向再灌注损伤药物的联合方案。此外,本试验患者基线收缩压高达143 mmHg,提示高后负荷对泵效率的制约可能是阴性结果的重要因素之一——未来研究是否可将基线血压纳入分层并探索卸载前短暂降压预处理,值得审慎评估。
最后,对STEMI-DTU研究团队的科学勇气表示敬意。敢于在"时间就是心肌"的金标准范式下主动延迟再灌注,即使有充分的临床前依据,也需要非凡的学术胆识。试验以100%的安全性完成卸载期间的临床观察(无一例需紧急PCI),证明了方案设计的严谨性。
阴性结果不是失败——它是科学方法运行正常的标志。真正的失败是不去检验那些需要被检验的假设。
参考文献:
Kapur NK, Mangner N, Aghili N, et al. Left Ventricular Unloading in Anterior STEMI without Shock: The STEMI Door to Unload (DTU) Randomized Controlled Trial, JACC (2026), doi: https://doi.org/10.1016/j.jacc.2026.03.071.