

复旦大学附属中山医院心内科黄浙勇教授
思辨介入困境
解析手术技巧
梳理中山经验
助您从新手变“心”手
每月15日、30日,严道医声独家发布
一
诊断
心肌壁内血肿临床表现缺乏特异性,影像学检查是确立诊断和判断预后的关键手段。
1、冠脉造影
冠脉造影可提供初始线索,表现为难以消散的造影剂外渗。外渗的造影剂滞留局限在室壁内或心外膜下,呈局限性“心肌染色”或“脂肪染色”,此时要想到心肌壁内血肿可能。

图1 造影表现为脂肪染色和心肌染色。
右冠中段CTO病变(A1),导丝穿孔,造影剂外渗形成局部脂肪染色(A2),提示房室沟心外膜下血肿。前降支中段CTO病变(B1),逆向介入间隔侧枝穿孔,造影剂外渗形成局部心肌染色(B2),提示室间隔壁内血肿。
2、床旁超声
超声心动图是IMH最常用的初筛工具,具有床旁、动态和可重复性强的优势。典型超声表现为局部室壁增厚,局部出现无回声囊腔/混合回声区,有时可出现“心肌分层征”:内外两层心肌之间形成低回声间隙。壁内血肿属于罕见并发症,并非日常关注重点,加上扫描角度受制于透声窗,因此极易漏诊。
此外,超声还可用于动态监测血肿体积变化及血流动力学影响,例如是否出现心腔压迫、流出道梗阻或心包积液。
3、心脏磁共振(CMR)
CMR是诊断心肌壁内血肿最可靠的影像学方法(图2)。①T1和T2加权信号改变。急性期血肿在T1加权像上呈高信号,在T2加权像上呈混合信号,这是由于血红蛋白分解产物所致。②晚期钆增强(LGE)表现。梗死心肌通常表现为明显的晚期增强,而血肿区域则多表现为低信号区,被高信号梗死心肌所包绕,形成所谓的“黑洞征(black hole sign)”,被认为是心肌壁内血肿较具特异性的CMR表现。③心肌夹层结构。CMR能够清晰显示血肿沿心肌纤维间隙扩展的范围,并判断是否接近心外膜或心内膜,从而评估破裂风险。
此外,CMR还可同时识别附壁血栓、微血管阻塞(MVO)及梗死范围。
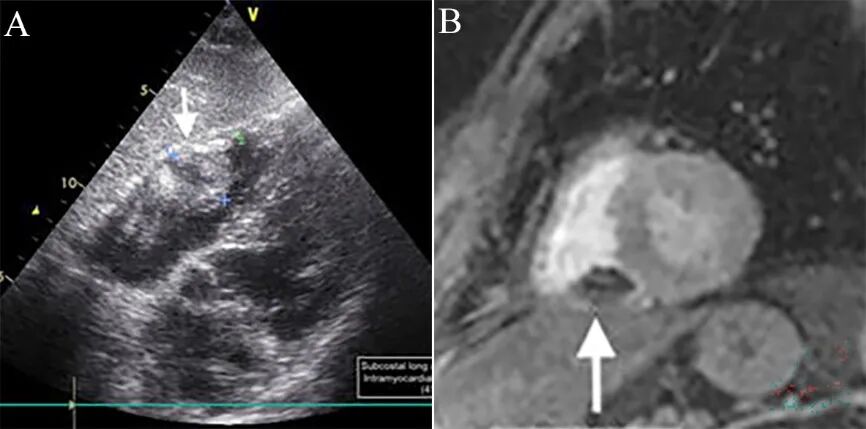
图2 CMR表现[1]。
急性下壁心肌梗死PCI顺利开通右冠,术后12小时出现胸痛和下壁导联ST段抬高,伴cTnT再次升高,但再次冠造未见血管堵塞和穿孔。随后数天症状缓解,cTnT逐渐降低,但下壁导联持续性ST段抬高,心超随访发现右室壁内血肿 (41×29 mm) (A,箭头),心脏MR证实右室下壁夹层血肿(B,箭头)。
4、心脏CT
心脏CT在壁内血肿诊断中的应用相对较少,表现为局限性心肌内低密度或混合密度区,增强扫描可显示血肿与心腔之间缺乏交通。若合并心包积血或心外膜下血肿,CT也可提供较清晰的解剖信息。
超声、CMR、CT等联合多模态成像无疑可提供更全面的价值(图3)。
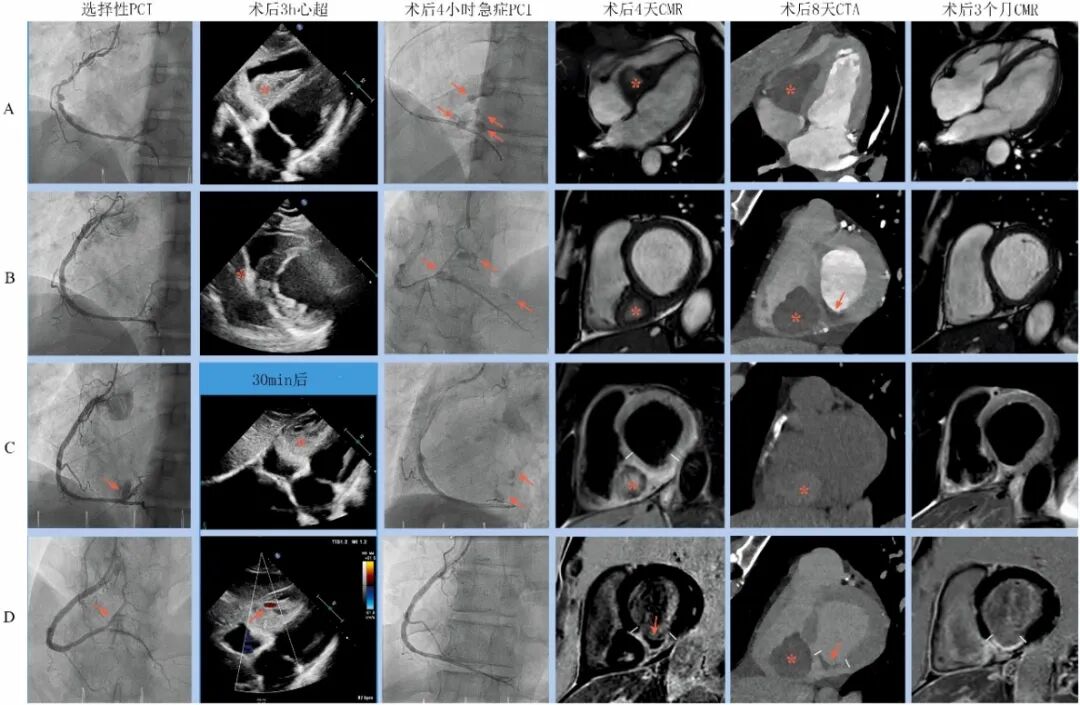
图3心肌壁内血肿的多模态成像[2]。
第一列为PCI图像,A.右冠造影;B.置入支架后;C-D 造影剂外渗。第二列为术后3小时心超,A.剑突下切面,可见室间隔血肿压迫右室;B.胸骨旁短轴切面;C-D 30分钟后复查剑突下切面心超,血肿快速进展,多普勒信号提示血流进入血肿。第三列为术后4小时再次PCI图像,A-B.紧急右冠造影可见多点外渗(箭头);C.长时间球囊封堵后依旧外渗;D 带膜支架植入,外渗停止。 第四列为第4天CMR图像,A和B分别为长轴四腔心和短轴电影,※为心肌内血肿;B.置入支架后;C.短轴T2加权,短线之间为高信号水肿,※为血肿;D短轴延迟增强,短线之间透壁性增强提示心肌梗死,箭头为微血管阻塞(MVO)。第五列为低8天CTA图像,A.注射造影剂后长轴四腔心,※为血肿,未见活动性造影剂外渗;B.相应短轴,※为血肿,箭头为微血管阻塞(MVO);C.无造影剂平扫,血肿显示为信号增强区;D短轴延迟增强,※为血肿,短线之间透壁性心肌梗死,箭头为微血管阻塞(MVO)。第六列为第3个月CMR图像,与第四列比较,可见心肌血肿完全消失(A和B),无水肿(C),慢性透壁性心肌梗死(D)
二
处理
心肌壁内血肿处理方法没有共识。传统观点要求外科手术,近年来有不少保守成功的案例。基于“血肿进展→血肿破裂或血流动力学崩溃”的病情三要素判断,可采取三种不同的治疗策略:血肿稳定型 → 保守;血肿进展型 → 介入;破裂/崩溃型 → 外科。
1、保守治疗
如同动脉壁内血肿一样,心肌内血肿一个月内可自行吸收。因此,“双稳定”状态(病变稳定 + 血流动力学稳定)的患者可以尝试保守治疗[3]:①血肿无进行性增大; ②无明显心腔受压或流出道梗阻、无破裂征象(心室瘘或心包积液);③血流动力学稳定。
保守处理:(1)采取 watchful waiting(密切观察)策略,序贯超声监测血肿变化趋势。序贯超声检测血肿发展趋势(早期每6小时一次);必要时CMR或CT随访。(2)严密监测血压与心率,及时发现低血压趋势;同时避免过高的血压波动,以减少血肿扩展风险。(3)抗栓调整。AMI或PCI后通常需要抗板或抗凝治疗,但并发心肌壁内血肿时,应权衡出血扩展风险与血栓风险,可暂时弱化抗栓方案。
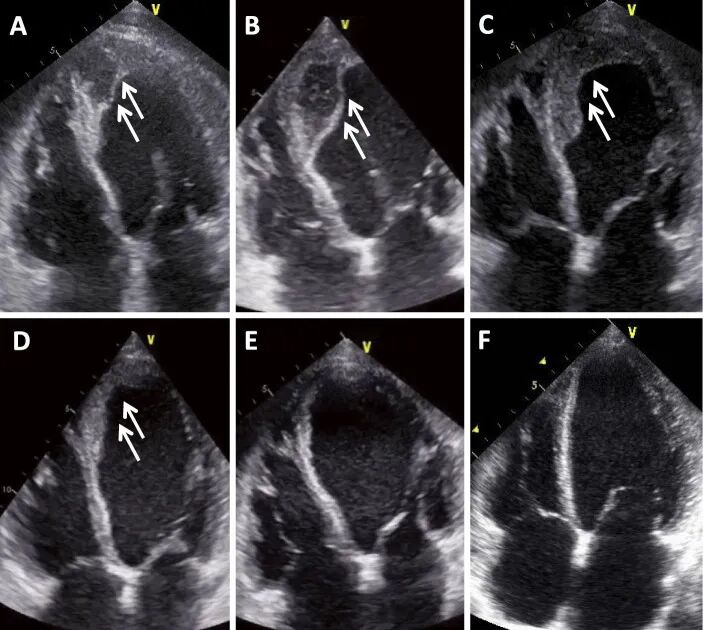
图4心肌壁内血肿的吸收过程[3]。
A为入院时,第3天(B)血肿增大,停用抗血小板药物;第9天(C)和15天(D)逐渐缩小,第23天(E)血肿消失,2个月(CABG后1个月,F)无复发。
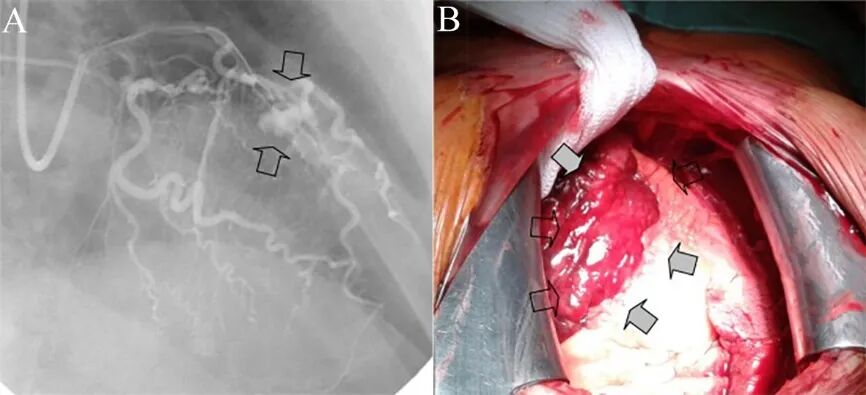
图5 保守处理介入相关心肌壁内血肿[6]。
72岁女性,不稳定性心绞痛。造影显示前降支和右冠狭窄,扭曲前降支球囊扩张后血管破裂,超声未见心包积液,病人血液动力学稳定,当时并未怀疑心外膜下血肿可能性。由于PCI未成功,6天后CABG手术,术中意外发现前壁广泛的心外膜下血肿,未见心包积液和黏连,未做处理,搭桥术后10天顺利出院。
2、介入干预
当冠脉穿孔导致的心肌壁内血肿快速增大时,可采取临时球囊阻断、近端带膜支架/远端栓塞等措施(图6)。
由于血肿具有局限性,很难进行常规心包穿刺。有人采取微导管抽吸血肿[4]。还有一种理论性治疗策略:介入硬导丝从血肿穿刺进入心室腔,并以小球囊扩张,从而人为形成可控性冠脉-心室瘘,以实现血肿减压。但该方法存在潜在心脏破裂风险,目前仅见个别报道[5]。
有时,血肿可导致严重心腔压迫(例如室间隔血肿压迫右心室),有条件者可考虑暂时性机械循环支持装置,如右室辅助装置,以维持血流动力学稳定并等待血肿逐渐吸收。
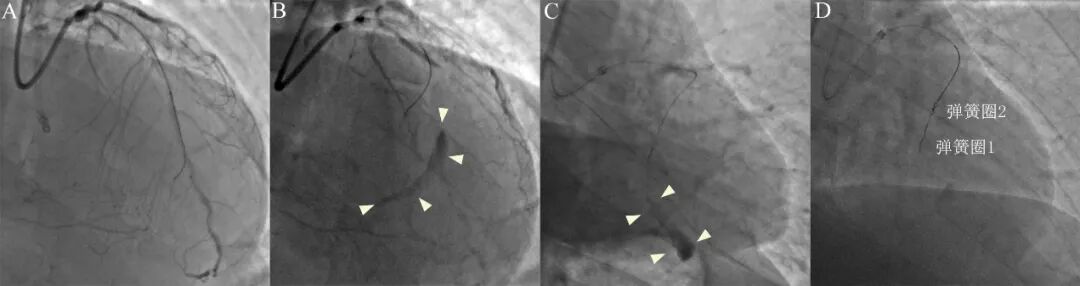
图6 弹簧圈封堵治疗心肌壁内血肿。
右冠CTO(A)尝试逆向开通,导丝在室间隔侧枝部位穿孔,形成新月形血肿(B,右肩位)。微导管超选择性造影确认穿孔血管(C),置入2*20mm弹簧圈2个封堵穿孔(D)。
3、外科手术
病人或病变不稳定时,介入封堵失败时,需要外科手术治疗。心肌壁内血肿的最大风险是进展为心脏破裂(图7)。如出血为活动性,血肿张力突破心外膜极限时,血肿破裂转化为心包腔游离性积液或室间隔缺损[7],需要急诊手术。AMI后壁内血肿也可能是心脏破裂的中间阶段(所谓亚急性心脏破裂),需要严密监测,要做好随时急诊手术的准备。
外科手术方式主要是血肿清除与心肌修补,通过切开血肿腔清除积血,并使用补片或缝合方式修补撕裂的心肌组织。若同时存在严重冠状动脉病变,可在手术中联合进行血运重建。
需要指出的是,血肿往往发生于AMI脆弱心肌区域,手术难度较大,围手术期死亡率高。因此,外科治疗通常仅用于无法通过保守或介入方式控制的进展性病例。
特别指出,全层撕裂导致的假性室壁瘤需要紧急手术,必须除外。超声特征是新发心包积液,窄颈,左室节段向外膨出;彩色多普勒可见湍流信号进入假性室壁瘤颈部。如超声微泡进入心包,提示心脏破裂。心脏MRI可提供进一步信息。

图7 心肌壁内血肿破裂后外科修补[8]。
心肌梗死后后心尖部梭形血肿(A),随访观察发现血肿进展(B),并出现新发的心包积液,提示心脏破裂(C)。紧急外科手术,切开心包可见大范围的血肿(E1),重建左室采用人工补片(E2-E3),切除心尖部梗死心肌后,左室腔暴露,四周缝线准备缝合人工补片(E4);人工补片缝合和固定(E5)。D为术后心超。
参考文献:
⇅ 向上滑动阅览
“中山PCI解码”下期预告
CTO开通后造影剂外渗:“心室瘘”或“冠脉穿孔”?
CTO开通后出现造影剂外渗,是“心室瘘”还是“冠脉穿孔”?可遵循“三步法”进行鉴别(图8):先看“命”:血流动力学是否稳定,是否存在心包填塞;再看“像”:外渗形态、方向及是否伴造影剂滞留;最后看“史”:基线造影是否已有类似表现。总体原则是优先排除冠脉穿孔以避免延误抢救,同时警惕将心室瘘误判为穿孔导致过度治疗


