健心知著
2026.04.08
第531期

基于冠状动脉CT血管造影的机器学习模型:精准预测心血管风险的新突破

刘健、赵妍、彭欣
北京大学人民医院
健心荐语
冠状动脉CT血管造影(CCTA)已广泛应用于冠心病诊断,但其在心血管事件风险预测中的潜力尚未被充分挖掘。本研究首次将机器学习(ML)与CCTA影像特征结合,构建了一个多维度的风险预测模型,显著提升了对主要不良心血管事件(MACE)的预测能力。研究发现,基于CCTA的机器学习模型在1-5年随访期间持续优于传统临床风险模型和冠状动脉钙化评分(CACS),为个体化心血管风险管理提供了新工具。
文章介绍
本研究由中国医学科学院阜外医院团队主导,发表于《Circulation: Cardiovascular Imaging》(2025年12月),基于CREATION前瞻性注册研究,纳入8431例疑似冠心病患者,通过六种机器学习生存模型对比分析,最终构建并验证了一个基于CCTA影像特征的MACE预测模型。
研究方法
研究设计:前瞻性队列研究,纳入2016年至2019年在阜外医院接受CCTA检查的疑似冠心病患者。
影响评估:采用标准化CCTA扫描方案,通过自动化软件(Deep Blue,GE Healthcare)定量分析斑块。根据CT值区分脂质斑块(<30 HU)、纤维斑块(30-150 HU)、钙化斑块(>350 HU)及管腔(150-350 HU)。不良斑块特征包括低衰减斑块、正性重构、点状钙化和餐巾环征;定性指标高危斑块定义为至少具备2个不良特征。定量指标包括各亚型斑块体积(mm³)及斑块负荷(斑块体积/血管体积×100%)。
特征选择与模型构建:共提取48个CCTA候选变量(包括狭窄程度、斑块分布、定性和定量特征)。采用6种机器学习生存算法(XGBoost、DeepHit、Cox比例风险、随机生存森林、GBSA、SVM),以70%为训练集、30%为测试集,通过5折交叉验证调整超参数。以XGBoost性能最优,并通过递归特征消除筛选出6个最重要特征:直径狭窄、脂质斑块负荷(%)、脂质斑块体积、高危斑块、总斑块体积、血管体积。构建5个比较模型:模型1(临床危险因素)、模型2(临床+CACS)、模型3(CCTA 6特征)、模型4(临床+CCTA)、模型5(临床+CACS+CCTA)。
结局指标:主要终点为MACE(包括全因死亡、急性心肌梗死、冠状动脉血运重建、卒中)。
统计方法:使用C指数、时间依赖性AUC、净重分类改善指数(NRI)等评估模型性能,并进行亚组分析与敏感性分析。
研究结果
本研究共纳入8431例患者,分为训练集(5901例,占70%)和测试集(2530例,占30%)。表1 展示了总人群、训练集(n=5901)与测试集(n=2530)的基线特征,总人群平均年龄54.73±10.21岁,男性占48.2%,有症状胸痛占50.9%。中位随访3.68年期间共发生319例MACE(3.8%),包括34例死亡、8例急性心梗、244例血运重建(202例PCI,42例CABG)和54例卒中。训练集与测试集两组在年龄、性别、危险因素、CACS分组、合并队列方程风险评分及MACE发生率(均为3.8%)方面均无显著差异,表明数据分割良好。
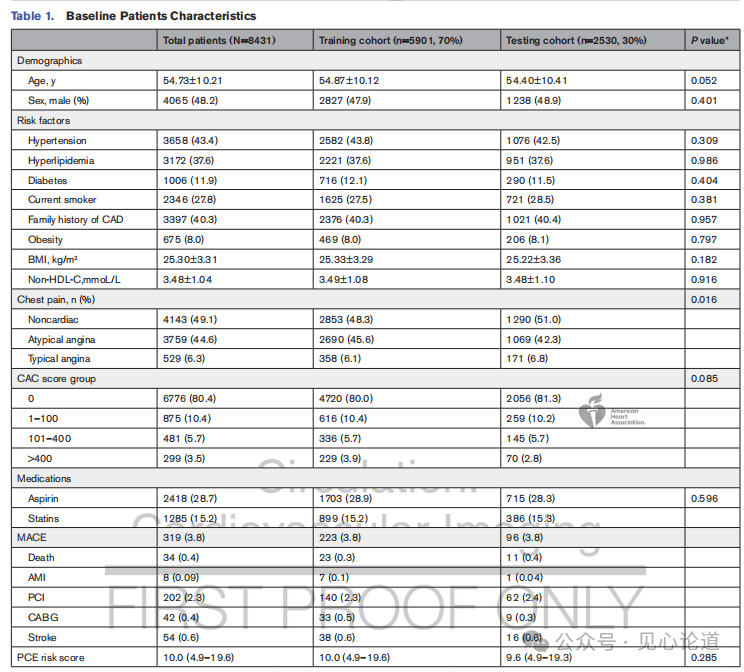
表1 患者基线特征
表2 比较了MACE组与非MACE组的冠脉特征。在CCTA检查中,76.4%的患者冠脉正常,11.1%存在非梗阻性斑块,7.7%存在单支血管梗阻性冠心病(狭窄≥50%),3.0%存在双支血管梗阻性病变,1.7%存在三支血管或左主干病变。全部患者的平均总斑块负荷为6.08%(标准差±12.74%),其中非钙化斑块负荷为5.78%(标准差±12.02%),纤维斑块负荷为5.04%(标准差±10.56%),脂质斑块负荷为0.73%(标准差±1.90%),钙化斑块负荷为0.30%(标准差±1.63%)。在训练队列中,MACE组患者的年龄显著大于非MACE组(60.66±9.49岁 vs. 54.65±10.08岁;P<0.001)。MACE组中男性比例更高(66.8%),并且除冠心病家族史、体重指数和非高密度脂蛋白胆固醇外,其他传统心血管危险因素的患病率也高于非MACE组。MACE组患者梗阻性冠心病、更高狭窄率及高危斑块的发生率也更高。在冠脉定量分析中,MACE组在不同斑块亚型的斑块体积和斑块负荷方面均表现出显著差异(所有P<0.001)。这些结果在测试队列中与表2的结果相似。
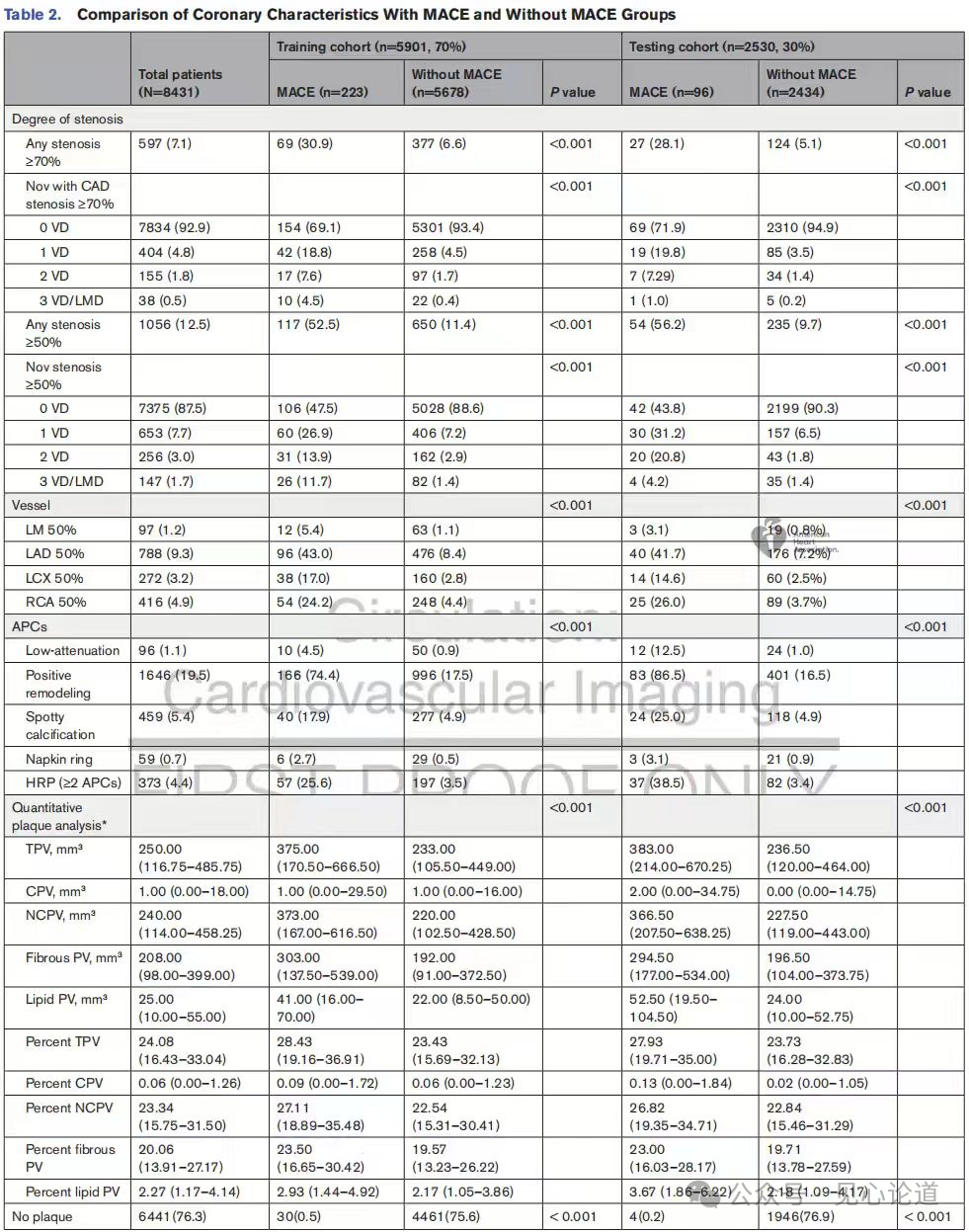
表2 MACE组与非MACE组的冠脉特征
表3 比较了6种机器学习算法的预测性能。无论使用全部48个变量还是仅使用前6个变量,XGBoost均表现最佳(训练集C-index 0.925/0.909,测试集0.918/0.911)。
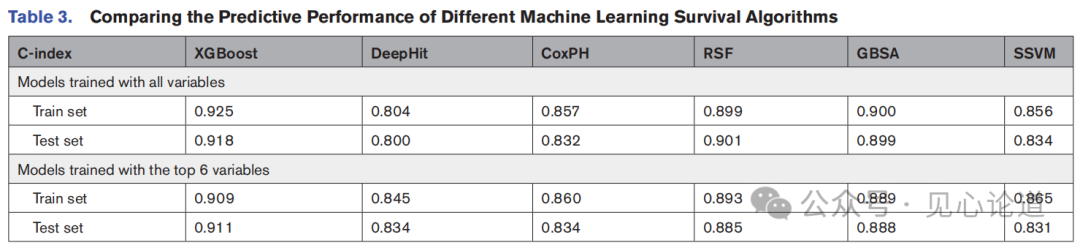
表3 不同机器学习生存算法在训练集与测试集中预测MACE的性能比较
图1 展示了XGBoost模型中各特征的重要性排序(SHAP值)。排名前6的特征依次为:脂质斑块负荷(%)、血管体积、脂质斑块体积、高危斑块、直径狭窄、总斑块体积。其中脂质斑块负荷与MACE风险相关性最强(校正后每增加5%的HR为2.524,95% CI:2.157–2.996,P<0.001)。在训练队列和测试队列中,这6个CCTA特征均与较高的MACE风险独立相关,且独立于传统心血管危险因素和CACS。

图1 XGBoost机器学习模型预测MACE的特征重要性排序
图2 展示了5个模型在训练集和测试集中预测MACE的ROC曲线。在测试集中,单纯临床模型(模型1)的AUC为0.708,临床+CACS模型(模型2)为0.753(△AUC=0.045,P=0.308),而CCTA模型(模型3)的AUC达到0.899,显著优于模型1和模型2(△AUC分别为0.191和0.146,均P<0.001)。临床+CCTA模型(模型4)和临床+CACS+CCTA模型(模型5)的AUC进一步提升至0.895和0.905,但模型5与模型3相比无统计学差异。这些发现表明,CCTA模型在预测心血管事件方面表现出优越的区分能力,并且在测试队列中得到了验证。尽管临床模型和CACS模型也显示了一定的预测能力,但CCTA模型的表现优于它们。此外,这些模型的联合使用进一步增强了区分能力,提示CCTA特征在临床模型和CACS模型之外提供了额外的预测价值。
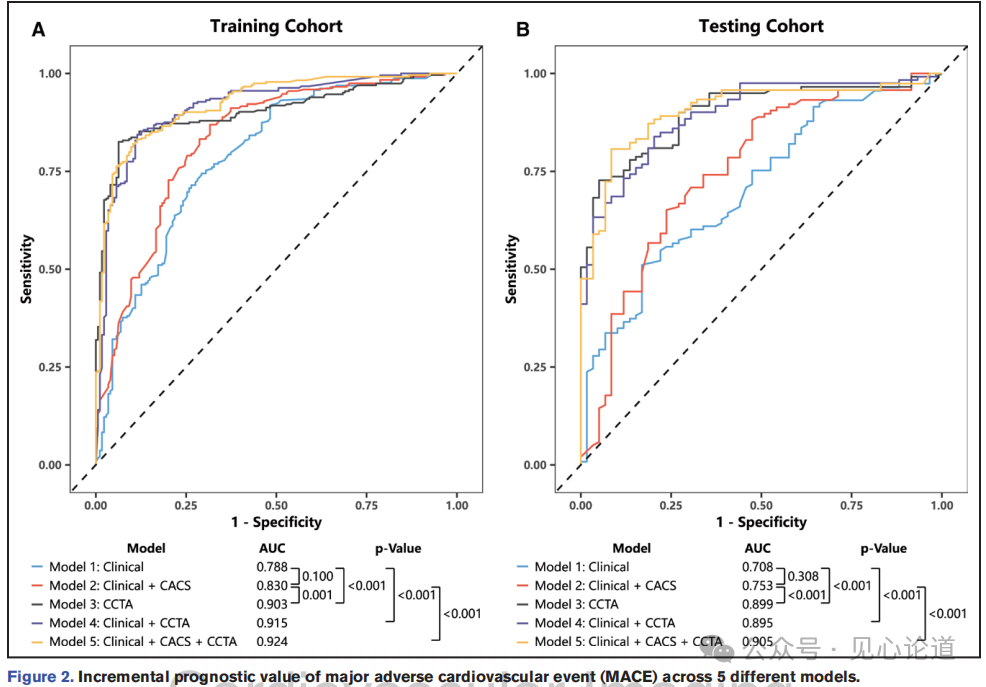
图2 不同风险模型在训练队列(A)与测试队列(B)中预测MACE的ROC曲线及AUC比较
表4总结了在测试队列中五种风险模型预测MACE的性能。结果显示,单纯临床模型的AUC为0.708、C-index为0.746;加入CACS后略有提升(AUC 0.753,P=0.308 vs 临床模型),但改善不显著。相比之下,仅含6个CCTA特征的模型(模型3)表现出显著更优的区分能力(AUC 0.899,C-index 0.911,均P<0.001 vs 临床或临床+CACS),且净重分类改善指数显著(与临床模型相比NRI=0.703,与临床+CACS相比NRI=0.420,95%CI均不包含0),同时Brier评分更低(0.032 vs 临床模型的0.057),校准更佳。在临床或临床+CACS基础上加入CCTA特征(模型4、5)可进一步提升AUC至0.895~0.905、C-index至0.897~0.919,并降低Brier评分至0.028~0.030。总体而言,CCTA模型及其联合模型在区分度、重分类改善和校准度上均显著优于传统临床模型及临床+CACS模型。

表4 测试队列中不同风险模型的区分度(AUC/C-index)、NRI及校准度(Brier评分)
图3展示了按1年间隔进行的时间依赖ROC曲线分析。在评估5个预测模型在不同时间点的预测能力时,无论事件发生的时间如何,CCTA预测模型均显示出比临床+CACS模型更高的预测能力。此外,临床+CACS与CCTA的联合模型表现出增强的预测价值。但值得注意的是,所有模型的预测能力随时间延长均有一定程度下降。
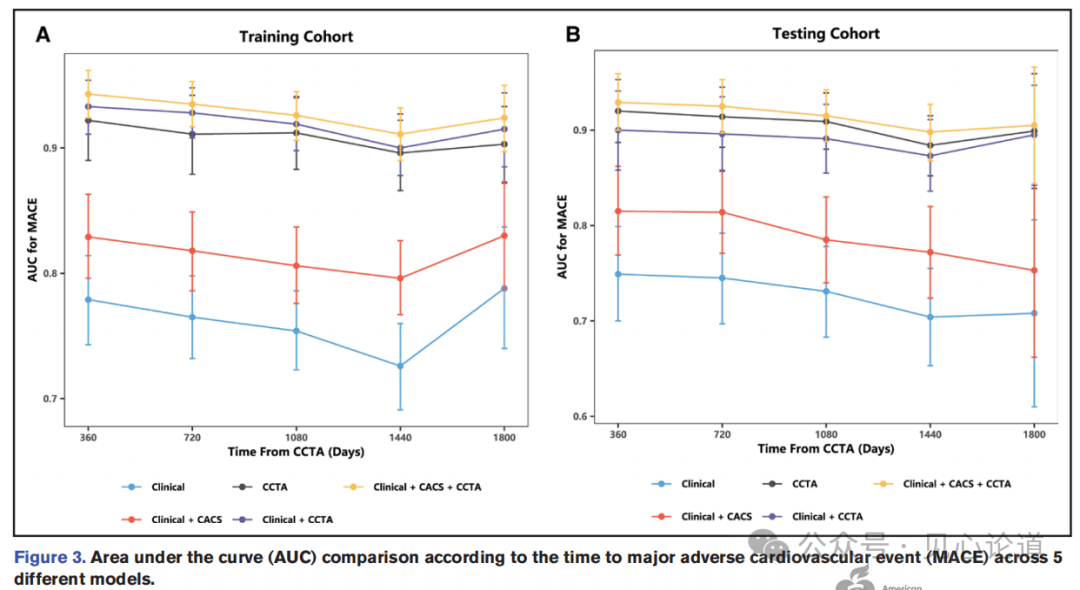
图3 五种风险模型在1至5年随访期内预测MACE的时间依赖AUC比较
图4 展示了两个代表性病例的个体化风险解释,其中脂质斑块负荷对MACE事件的贡献最大。在所展示的MACE事件病例中,脂质斑块负荷在预测未来MACE发生时对分类器输出的增量贡献最大。

图4 测试队列中两例代表性患者的SHAP瀑布图:各CCTA特征对MACE风险预测的贡献
在亚组分析中,CCTA模型在性别(男/女)、症状(有/无胸痛)、发病年龄(早发/晚发)亚组中均一致地优于临床模型和临床+CACS模型。敏感性分析(排除正常冠脉患者或仅纳入CACS>0的患者)结果与主分析一致。当采用次要终点(排除血运重建)时,各模型表现无明显变化。
结 论
基于CCTA的机器学习模型能显著提升对MACE的预测准确性,尤其在识别高危斑块特征和量化斑块负荷方面具有独特优势。该模型具有较好的校准能力和临床可解释性,可用于个体化心血管风险分层与早期干预决策支持。
讨论
本研究的核心价值在于:
① 风险预测精准化:首次将机器学习与CCTA多维影像特征结合,实现了对MACE的个体化、动态化风险预测。
② 临床实用性强:模型仅需6项CCTA特征即可实现高效预测,易于集成至现有影像系统中,辅助临床决策。
③ 超越传统工具:在预测性能上显著优于传统临床风险评分和CACS,尤其适用于已接受CCTA检查的患者。
④ 可解释性高:通过SHAP值可视化特征贡献,增强了模型的临床可信度与接受度。
局限:本研究为单中心数据,尚未进行外部验证;未记录降脂药物具体使用情况;未来可进一步整合血流储备分数(FFR)、血管周围脂肪衰减指数等新型参数以提升预测效能。