
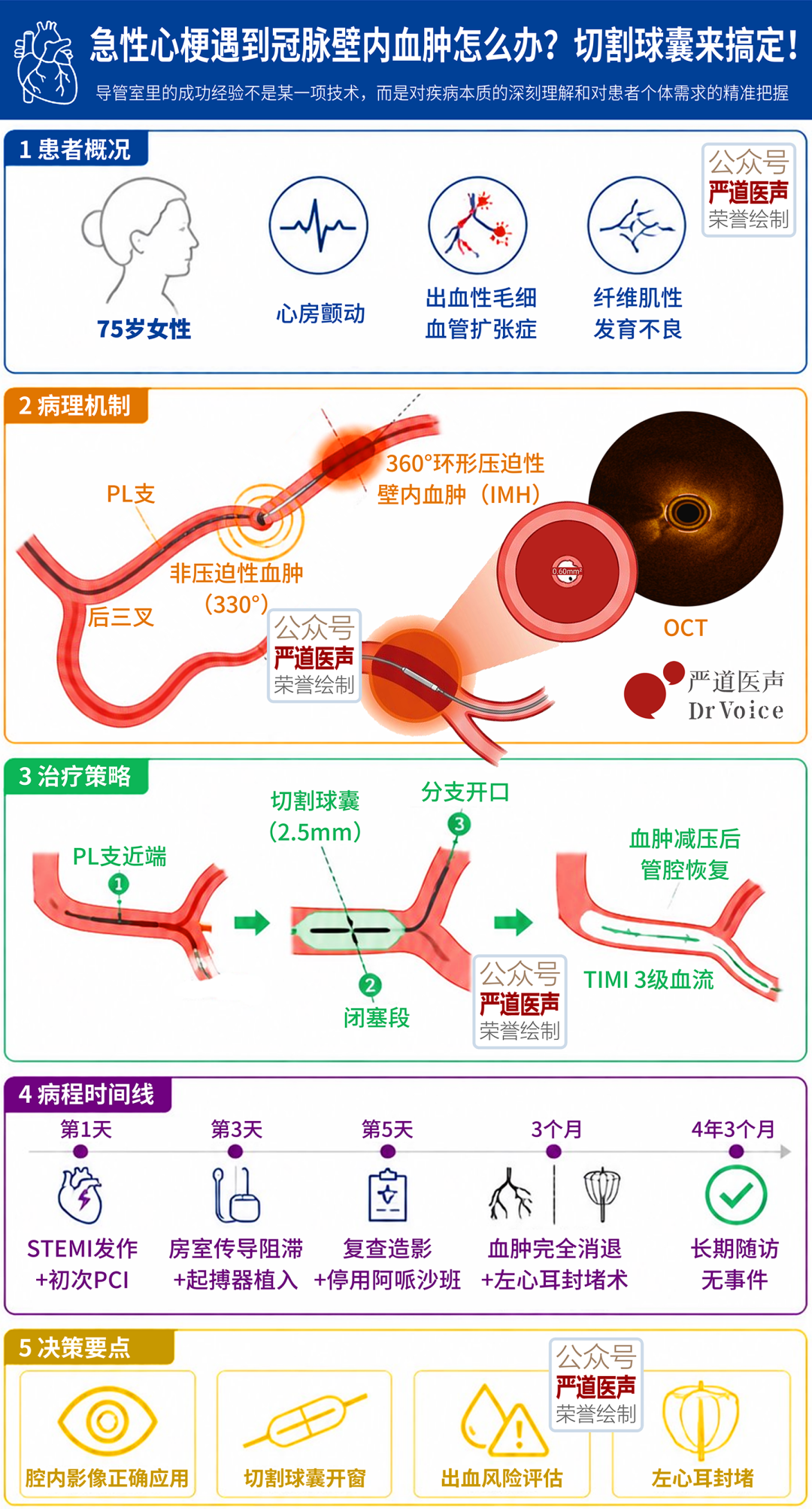
急性冠脉综合征(ACS)的病因多样,除了常见的动脉粥样硬化斑块破裂,冠状动脉壁内血肿(intramural hematoma, IMH)也是需要警惕的原因之一。传统观点认为,冠脉壁内血肿多见于年轻女性,与自发性冠状动脉夹层(spontaneous coronary artery dissection,SCAD)相关。然而,在老年患者中,壁内血肿的发生率极低,文献报道甚少。

近日,《JACC: Case Reports》发表了一篇题为“Compressive Coronary Hematoma in an Elderly Woman Receiving Oral Anticoagulation Treated With Cutting Balloon Fenestration”的病例报告,详细描述了一例75岁女性患者因口服抗凝药(阿哌沙班)期间发生下壁ST段抬高型心肌梗死(STEMI),经光学相干断层扫描(OCT)明确诊断为压迫性冠脉壁内血肿,并采用切割球囊开窗(cutting balloon fenestration)策略,成功避免了支架植入,取得长期良好预后。本文将该病例的诊治要点及决策逻辑进行系统梳理,供各位同道参考。
01
病例摘要
患者,女性,75岁,因急性胸骨后疼痛和下壁STEMI入院(第1天)。
入院前2个月,因新诊断心房颤动开始口服抗凝治疗(阿哌沙班)。
既往史还包括:2个月前曾发生心源性栓塞性缺血性卒中、帕金森病,以及遗传性出血性毛细血管扩张症(Rendu-Osler病)。
02
初次造影
在STEMI第1天进行的冠状动脉造影显示:
左室后支(posterolateral branch,PL)急性闭塞。
右冠状动脉(right coronary artery,RCA)远端出现不寻常的锥形狭窄(图1A)。
左冠状动脉系统以及RCA近段、中段均正常,无动脉粥样硬化的证据。
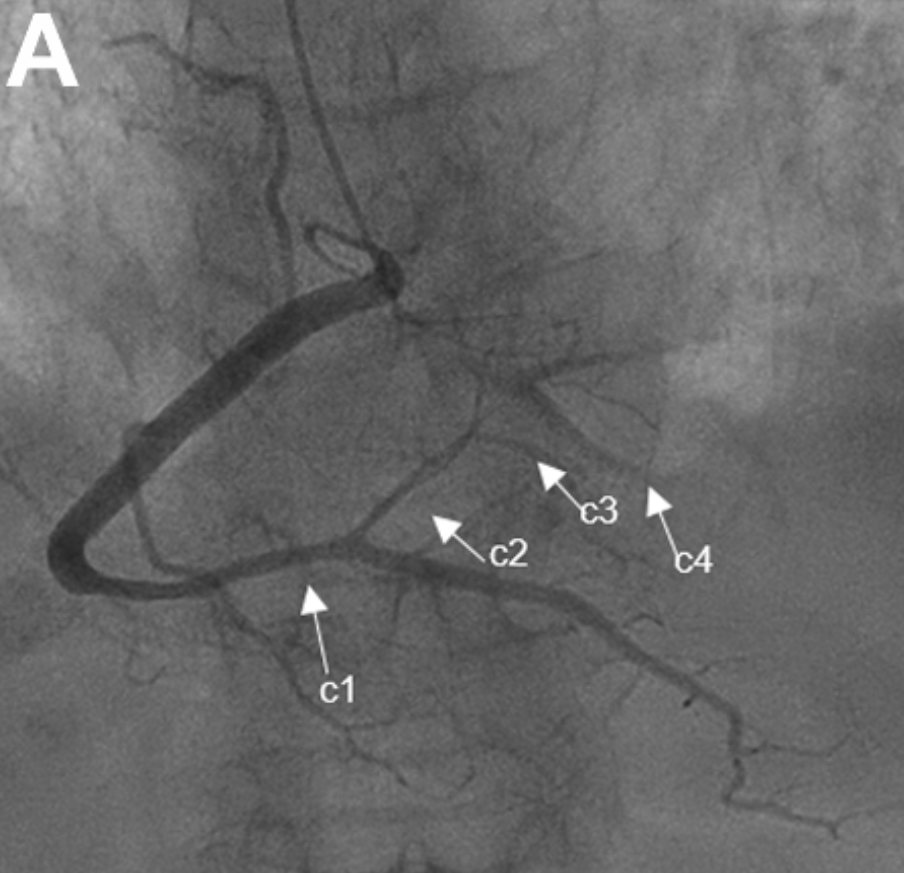
图1A 初次冠状动脉造影显示PL支急性闭塞
03
OCT检查
OCT显示,在RCA及PL支的多个层面提供了清晰的血管壁及管腔信息,证实存在两种截然不同的壁内血肿模式(图1C1至1C4,视频1):
RCA远端:存在非压迫性壁内血肿。位于后降支(PDA)-PL支分叉近端,血肿弧度约330°,最小管腔面积(MLA)为4.6mm²,残余管腔直径为2.53mm。该血肿未造成血流动力学明显受限。
PL支近端:存在非压迫性壁内血肿(血肿弧度约330°,MLA为2.16mm²,残余管腔直径1.6mm)。
PL支闭塞段:呈360°环形压迫性壁内血肿,MLA仅为0.60mm²(该面积实际上仅能容纳导丝和OCT导管的空间),残余管腔直径0.9mm,为罪犯病变。
PL支远端(血肿以远):为正常血管段,外弹力膜直径3.4mm,未见壁内血肿。
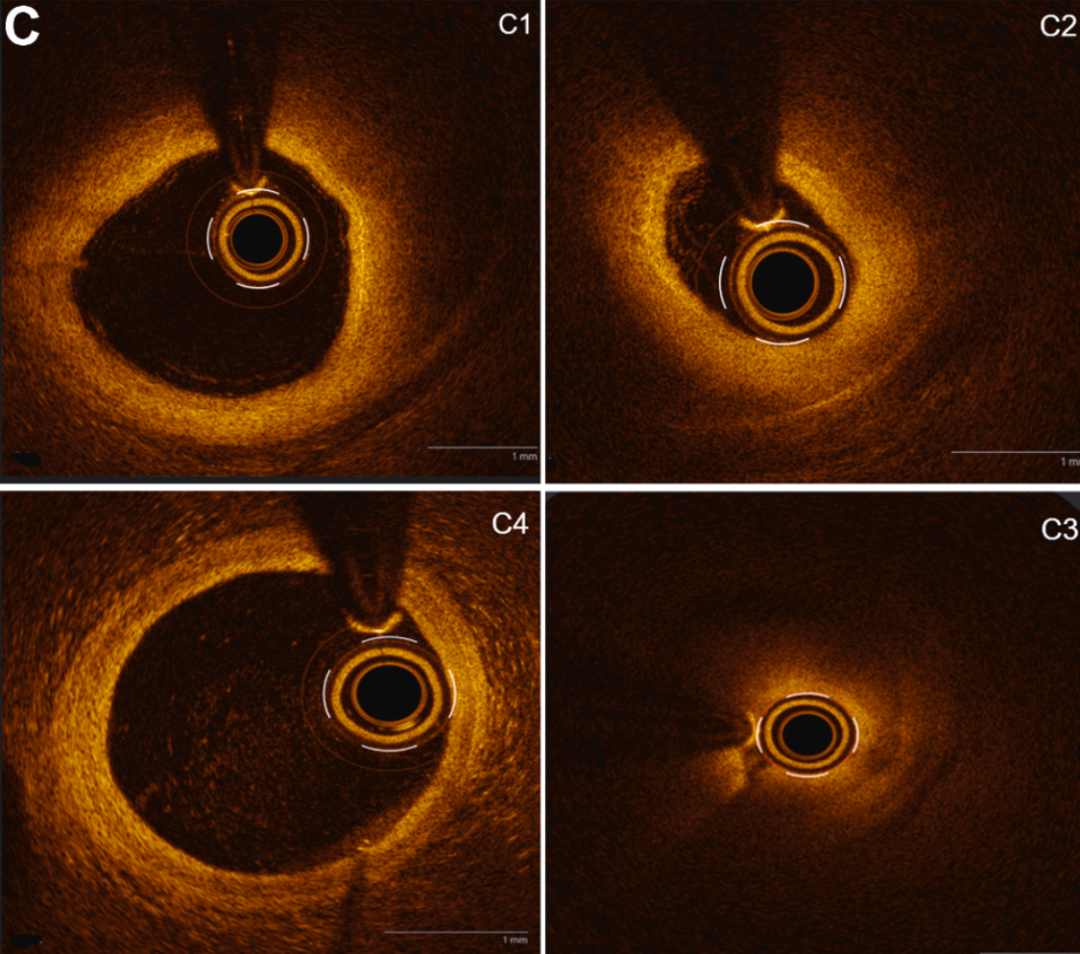
图1C 急性期OCT图像
C1:RCA远端,位于PDA-PL支分叉近端,显示非压迫性壁内血肿。C2:PL支近端,显示非压迫性壁内血肿。C3:PL支闭塞段,显示360°环形压迫性壁内血肿,管腔缩小到仅能容纳导丝和OCT导管的空间。C4:PL支远端血肿以远,正常血管段,外弹力膜直径3.4mm。
04
治疗策略
由于患者持续胸痛、ST段抬高持续存在,且PL支血流仅为TIMI 1级。
考虑到压迫性血肿位于两个分叉区域之间——近端为PDA-PL支分叉,远端为两个PL支的分叉。此处植入支架易导致血肿向分支蔓延、侧支闭塞以及复杂的分叉处理。另外,若植入支架,需延长双重或三重抗栓治疗(抗凝+双联抗血小板),但患者年事已高且存在出血体质(遗传性出血性毛细血管扩张症),出血风险极高。
术者决定进行OCT引导下的经皮冠状动脉介入治疗(PCI):
选用2.5mm×10mm Wolverine切割球囊。
针对三个区域分别进行3次切割:PL支近端、闭塞段(远端)及上侧分支开口处。每次16个标准大气压,持续20秒。(视频2)
结果显示,成功实现了对血肿的减压,PL支血流恢复至TIMI 3级,心肌缺血迅速缓解(图1B、视频4)。

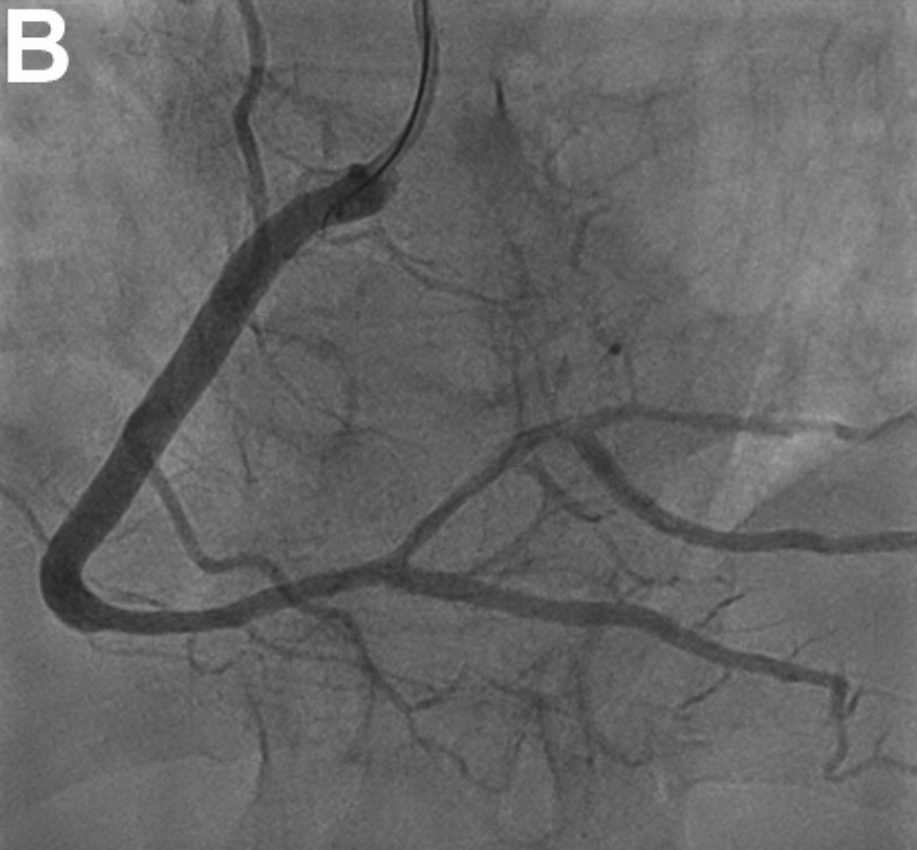
图1B OCT引导的PL支切割球囊开窗术后最终造影结果,恢复TIMI 3级血流

术后继续单用阿哌沙班抗凝。
05
后续病程的波折
患者在第3天出现完全性房室传导阻滞,在从房颤自行转为窦性心律时最长停搏超过7秒,结合临床情况提示存在潜在的传导系统疾病,无复发胸痛或缺血性心电图改变。考虑机制为多因素:基础疾病(快慢综合征)以及可能因PL支血肿影响房室结动脉供血导致的房室结一过性缺血,由于停搏时间过长且未来可能需要长期抗心律失常治疗,因此植入了永久起搏器。
由于未在血肿处植入支架,术者在第5天进行了冠状动脉造影复查。结果发现:
PL支壁内血肿有蔓延,残留管腔狭窄,但切开部位仍保持TIMI 3级血流。
RCA远端的壁内血肿也出现进展(图1D)。
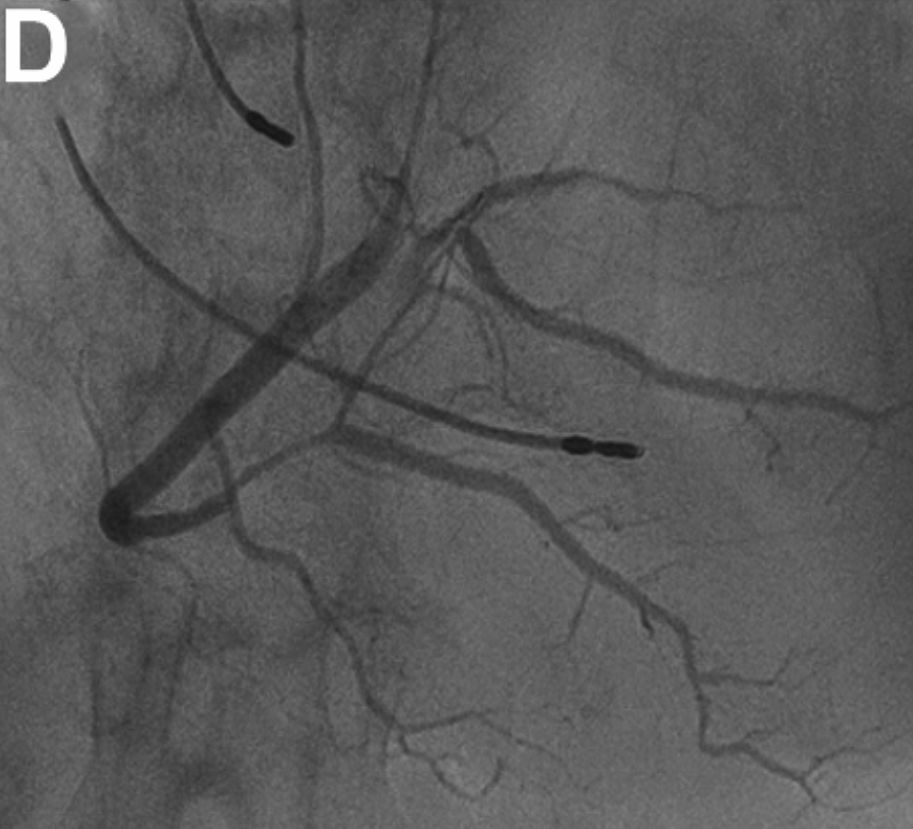
图1D:第5天造影复查显示RCA远端壁内血肿进展,但冠脉血流正常
这一发现促使临床团队决定永久停用阿哌沙班,改为单用阿司匹林抗血小板治疗。理由如下:结合患者存在的遗传性出血性毛细血管扩张症(HHT)和后续确诊的纤维肌性发育不良(FMD),其血管壁本身存在脆性。口服抗凝药虽不是导致壁内血肿的根本病因,但可能通过抗凝作用加重了血肿的扩展。停用抗凝后血肿逐渐愈合,进一步支持了这一判断。
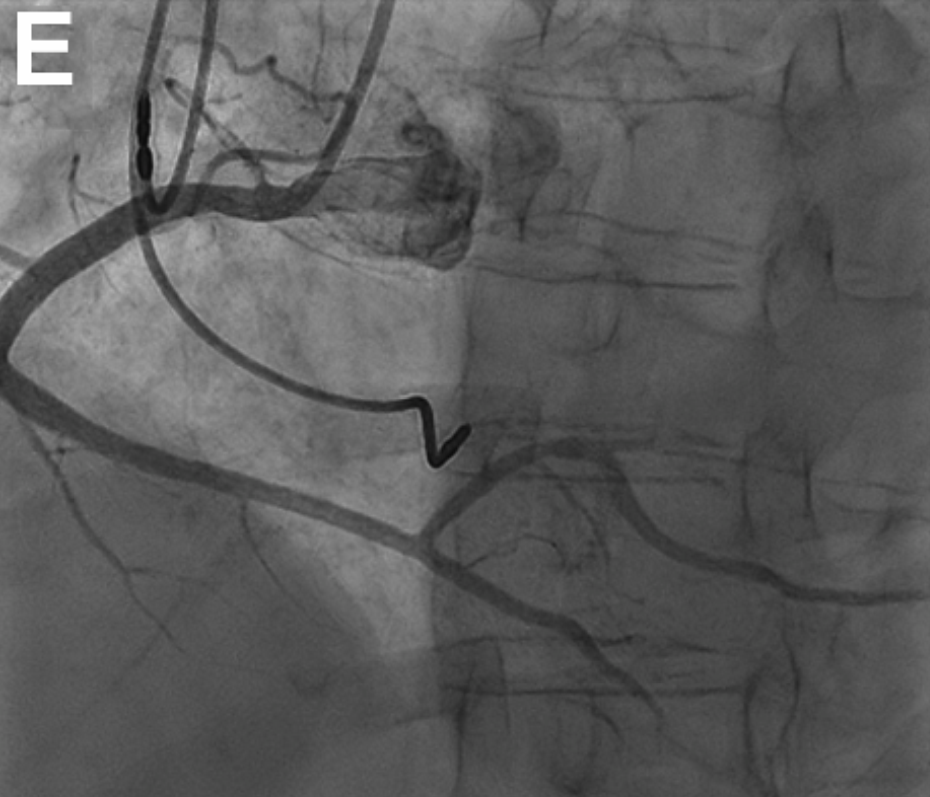
图1E 3个月造影随访显示壁内血肿完全消退,血管愈合
3个月后复查冠状动脉造影显示:PL支和RCA远端的壁内血肿完全消退,血管愈合(图1E)。临床无症状。
由于患者需长期预防心源性卒中,但口服抗凝药已被视为绝对禁忌,因此3个月后行经皮左心耳封堵术(使用22mm Amulet装置)用于二级卒中预防(图2)。
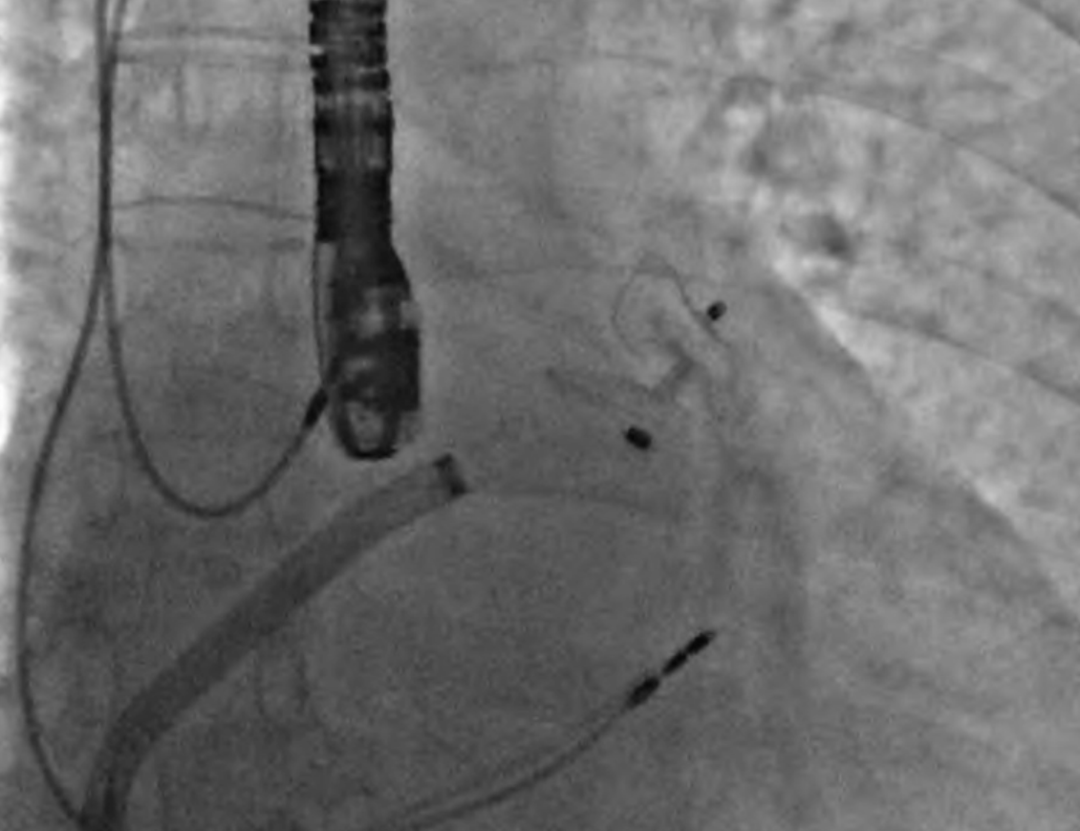
图2 经皮左心耳封堵术
06
长期随访
患者全主动脉及分支动脉CTA(1个月后)显示:腹腔干和肝动脉明显扩张、迂曲,肝内动脉分支增粗,无局灶性动脉瘤。这些发现高度提示纤维肌性发育不良(FMD)。
随访4年3个月,无再发缺血性或出血性事件。
07
讨论
OCT的不可替代性
本病例再次证明,对于非动脉粥样硬化性急性冠脉综合征,腔内影像学(尤其是OCT)是明确病因的金标准。OCT能够区分压迫性血肿与非压迫性血肿、评估血肿的范围和血管壁状态,并能指导干预,如仅针对压迫性血肿进行切开,非压迫性血肿可保守管理,从而减少不必要的支架植入。
切割球囊开窗治疗
切割球囊通过可控的血肿开窗,在真腔与壁内血肿之间建立沟通,从而促进血肿减压,恢复冠脉血流。既往文献已有报道将其作为独立策略或联合支架植入。本病例中,由于血肿位于分叉区域且患者存在出血高危,避免支架是明智之举。
血管脆性与抗凝药的关系
本病例的血管脆性主要源于两种基础病:遗传性出血性毛细血管扩张症(HHT)和纤维肌性发育不良(FMD)。两者均为公认的冠脉IMH易感因素。口服抗凝药(阿哌沙班)并非主要病因,但可能作为加重因素,促进血肿进展。停用抗凝后血肿完全愈合,提示在明确存在血管脆性的患者中,应谨慎使用口服抗凝药,并优先考虑非药物性卒中预防措施(如左心耳封堵)。
08
严道心得
本例中,造影所见仅为PL支闭塞和RCA远端狭窄,如果没有OCT,很容易误认为是血栓或斑块破裂,从而可能直接植入支架。而OCT清晰揭示了360°环形壁内血肿,并区分了压迫性与非压迫性两种形态,直接改变了治疗策略,避免了不必要的支架植入及随之而来的强化抗栓治疗。
这提醒我们,在遇到中青年或老年无明确动脉粥样硬化危险因素的心梗患者时,应主动进行腔内影像学检查。
对于血肿压迫导致的急性闭塞,部分医师会选择长支架覆盖血肿段,但这可能带来血肿蔓延、边支丢失、支架内血栓等风险。本例采用切割球囊精准切开,仅解除压迫,保留血管自身愈合能力,最终完全恢复。这并非首次报道,但本例的长期随访证实了其疗效持久性。
本例患者同时患有HHT和FMD,血管壁本身存在胶原异常或中层发育不良,口服抗凝药如同在脆弱的血管壁上火上浇油,导致血肿持续扩大。这提示我们,对于有出血性疾病患者,启动口服抗凝治疗前应充分评估血管壁风险。一旦发生IMH,应首先考虑停用抗凝,并积极寻找替代的卒中预防方案。
本例中,FMD是在事件后1个月通过腹部CTA回顾性诊断的。FMD是SCAD和IMH的重要基础病因,累及肾动脉、颈动脉及冠脉。对于没有传统危险因素的ACS患者,尤其是女性,应主动筛查FMD,以便进行长期管理(如避免使用激素类避孕药、控制血压、监测其他血管床病变)。
请记住:导管室里的成功经验不是某一项技术,而是对疾病本质的深刻理解和对患者个体需求的精准把握。