

随着各类先进器械的应用,经皮冠状动脉介入治疗的应用率不断上升。导丝断裂、球囊嵌顿、支架输送系统断裂等器械故障偶有报道,可能引发严重不良事件。导管室内的器械故障虽然罕见,却可能成为一场真正的噩梦。当球囊在支架内无法回缩、甚至断裂脱落时,术者面临的不仅是技术挑战,更是对患者生命安全的严峻考验。当非手术方法无法取出断裂器械时,不得不实施创伤更大的外科取出术及急诊旁路手术以挽救病情。

《Ann Card Anaesth》报道了一篇真正的紧急情况“Surgical retrieval of broken, inflated angioplasty balloon catheter within intracoronary stent: A real emergency”,详细解析一例球囊嵌顿于冠脉支架内的急诊处理过程,旨在为心血管内科医师提供参考与警示。
01
病例报告
一位54岁女性患者,右桡动脉入路冠状动脉造影(CAG)显示:前降支(LAD)狭窄60%,回旋支轻微病变,右冠状动脉(RCA)慢性完全闭塞(CTO)病变。
对RCA开通,RCA的CTO病变导丝成功通过,并进行了预扩张。随后植入一枚3×48mm的Xience Xpedition支架,并用Hawk PTCA高压球囊进行后扩张。
然而,球囊竟然无法回缩,尝试回拉时,球囊从导管杆处断裂。患者出现胸痛和轻微不适,但血流动力学稳定。
将经桡动脉指引导管回撤至主动脉内,经右股动脉置入另一根指引导管至RCA,在微导管支持下,多次尝试用导丝挤压或刺破球囊,均未成功。随即请外科团队急诊取出支架内嵌顿的充盈球囊,并实施急诊冠状动脉旁路移植术(CABG)。
患者术前已接受标准负荷剂量阿司匹林300mg、氯吡格雷300mg口服,普通肝素5000单位静脉注射。
在手术室中,局麻下建立所有有创通路:左桡动脉用于有创血压监测,右颈内静脉用于中心静脉压(CVP)监测,左股动脉用于采血及必要时置入主动脉内球囊反搏(IABP)。
全身肝素化后建立体外循环(CPB):双腔静脉插管引流静脉血,升主动脉插管输送动脉血。阻断升主动脉,使用高钾冷血心脏停搏液保护心肌。
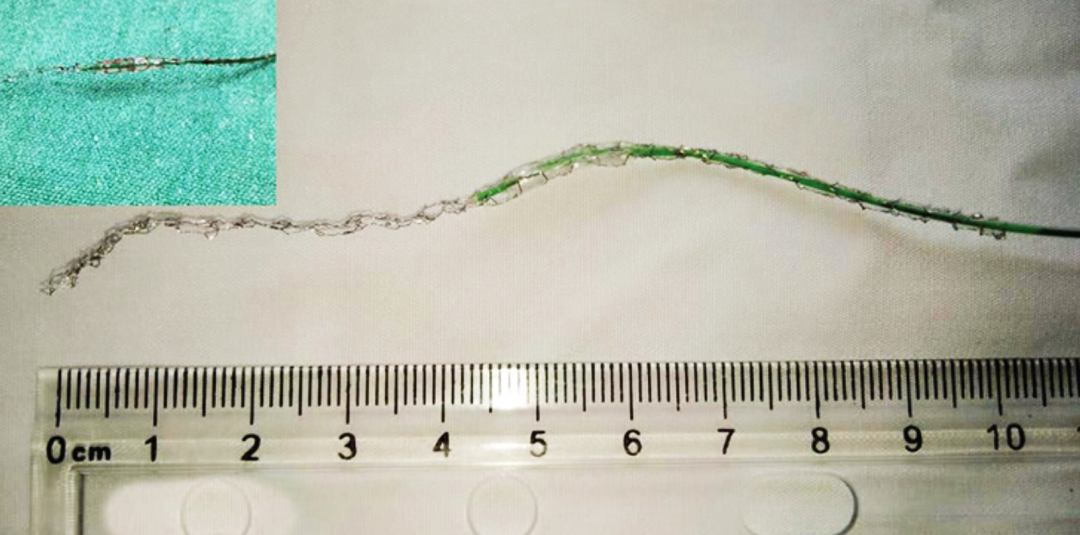
术者触诊定位RCA内支架,在支架远端行RCA切开,完整取出支架、充盈球囊及导管杆。仔细检查取出的支架与充盈球囊[图1]。
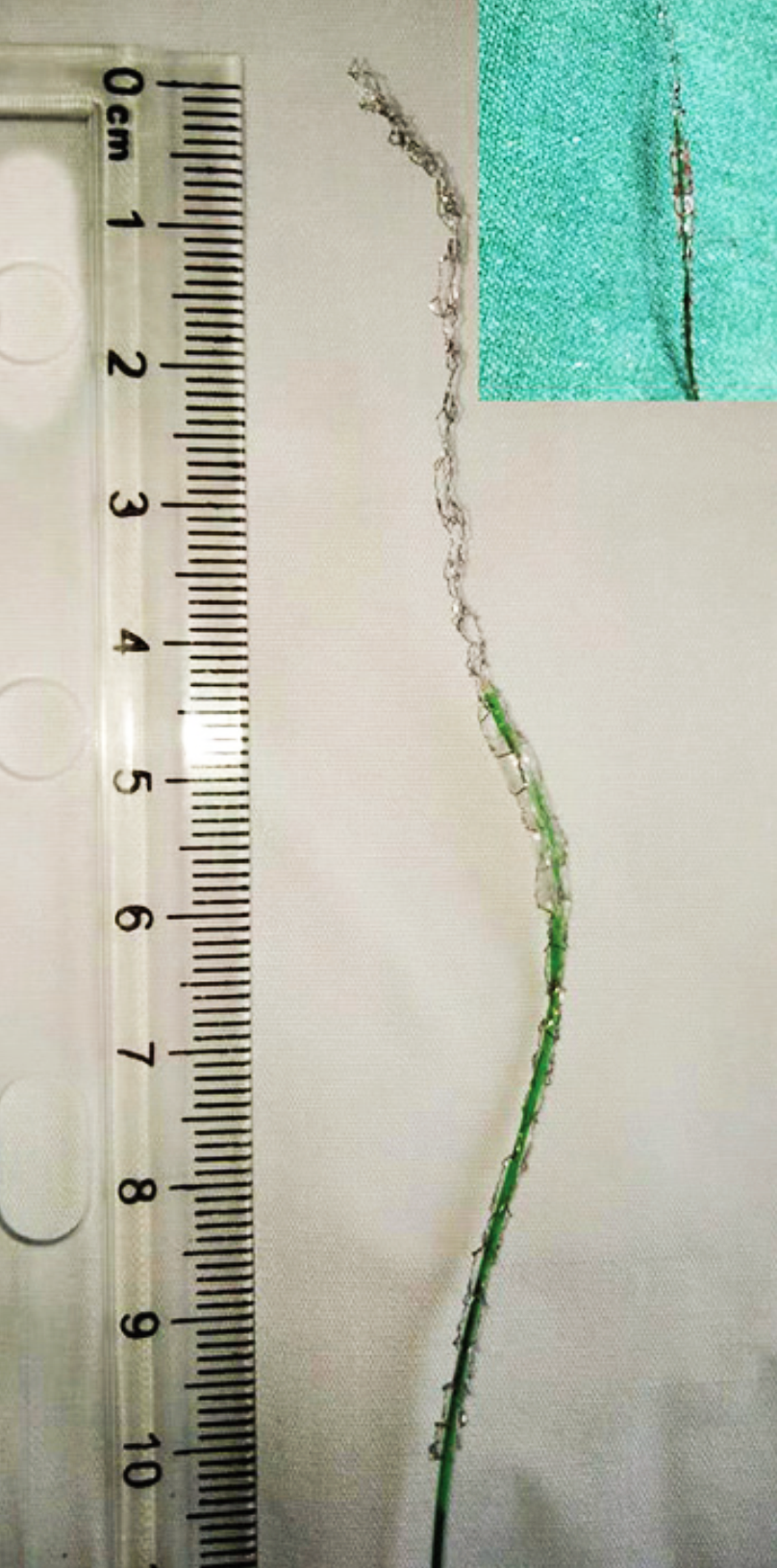
图1:支架连同充盈的球囊以及26cm长的断裂输送系统。插图:球囊处于膨胀状态,嵌顿于支架内。
动脉切开处以静脉补片关闭,在切口远端用倒置大隐静脉与右冠状动脉行旁路移植;LAD病变同期行倒置大隐静脉旁路移植。因手术紧急,未采用左乳内动脉(LITA)搭桥。
患者顺利脱离体外循环,术后6小时内拔管。
术后恢复顺利,术后第7天出院。
02
讨论
任何在操作中受力的器械均可能发生器械故障,包括球囊扩张导管断裂、导丝断裂、支架球囊无法正常充气或放气、后扩张球囊嵌顿于已释放支架的支架梁之间。
尤其在钙化血管中,术者需扩张坚硬的钙化狭窄病变。在本病例中,尽管患者支架能够完全释放,但球囊卡在支架的中段;然而,在尝试后扩张时,球囊无法回缩。球囊被充气至16个大气压(ATM)。尝试了多种方法使球囊回缩,如使用双压力泵、圈套器,均失败。术者的持续操作导致输送系统断裂,球囊以膨胀状态卡在支架内,造成远端血管完全闭塞。尝试通过从右股动脉插入的另一根引导导管,经微导管送入导丝挤压或刺破球囊,但所有操作均未成功。
此类灾难性事件的处理取决于患者的血流动力学状态。虽然患者主诉胸闷、轻微疼痛,未出现心电图改变和低血压。原因是患者术前存在CTO。
已有文献报道采用非手术方法取出嵌顿器械,如使用第二套扩张系统解脱嵌顿球囊。在本病例中,钙化病变阻止了断裂球囊被拉出,且也没有旋磨备用方案。
Keltai等报道,断裂导丝的远端20cm片段导致LAD和LCX立即发生急性血栓性闭塞,需急诊旁路手术。
在另一例病例中,由于患者血流动力学稳定,在2周后进行了择期手术取出,但术中未能找到导丝的断裂端。随访18个月后,患者情况良好,而导丝仍留在原位。
在本病例中,外科医生从外部触摸到支架,并通过RCA切口,将整个支架连同膨胀的球囊以及断裂的输送系统轻轻取出。取出了26cm长的断裂输送系统、支架和球囊。
心脏内残留器械的急诊手术面临特殊难题:因术前双联抗血小板药物负荷剂量与术中肝素化,易出现血流动力学紊乱与出血过多。
麻醉医生、心内科医生和外科医生应了解这些并发症,并准备好应对这些独特的挑战。术者应熟悉取出嵌顿器械的替代方法,或根据情况决定是否进行急诊手术干预。
严道心得
这是一例极为罕见的并发症——球囊在支架内膨胀后无法回缩,且在尝试取出时断裂,最终只能通过急诊开胸手术解决。对于心血管内科医师而言,这无疑是导管室中最不愿面对的紧急情况。然而,正是通过这样详尽的病例记录,我们得以窥见其发生机制、处理策略以及多学科协作的重要性。
器械故障多发生于钙化病变、复杂操作中。本例患者为CTO合并钙化,可能因钙化斑块挤压导致球囊无法回缩。术者启动了应急方案,但本例中这些非手术方法均失败,提示在极端情况下,手术是唯一出路。
本例患者因术前为CTO,远端已有侧支循环,因此球囊嵌顿后未出现严重缺血或血流动力学崩溃。这为外科团队争取了宝贵的准备时间。若患者为急性冠脉综合征或左主干病变,后果可能截然不同。因此,术者需根据患者状态快速判断:是继续尝试介入方法,还是立即呼叫外科。
从病例中可以看到,在介入失败后,外科团队迅速到位,麻醉医生精准管理抗凝与止血,手术医生巧妙取出支架并完成搭桥。整个过程体现了团队的高度默契。尤其值得注意的是,患者术前已接受双联抗血小板治疗和肝素化,术中出血风险极高,这提示我们,对于急诊手术,抗凝管理需要个体化。
作为介入医生,我们应关注器械的可靠性,并在操作中轻柔、规范。一旦发生卡顿,切忌暴力回拉,以免断裂。本例中,术者多次尝试后导致输送系统断裂,这提醒我们:当球囊无法回缩时,应首先尝试其他补救方法,避免反复操作加重损伤。
我们应时刻保持警惕。导管室内的噩梦虽然罕见,但一旦发生,后果严重。我们需要熟悉各种并发症的处理流程,与外科、麻醉科建立紧密协作机制,并不断从文献中学习经验。愿每一位术者都能从这样的病例中汲取教训,让噩梦不再重演。