
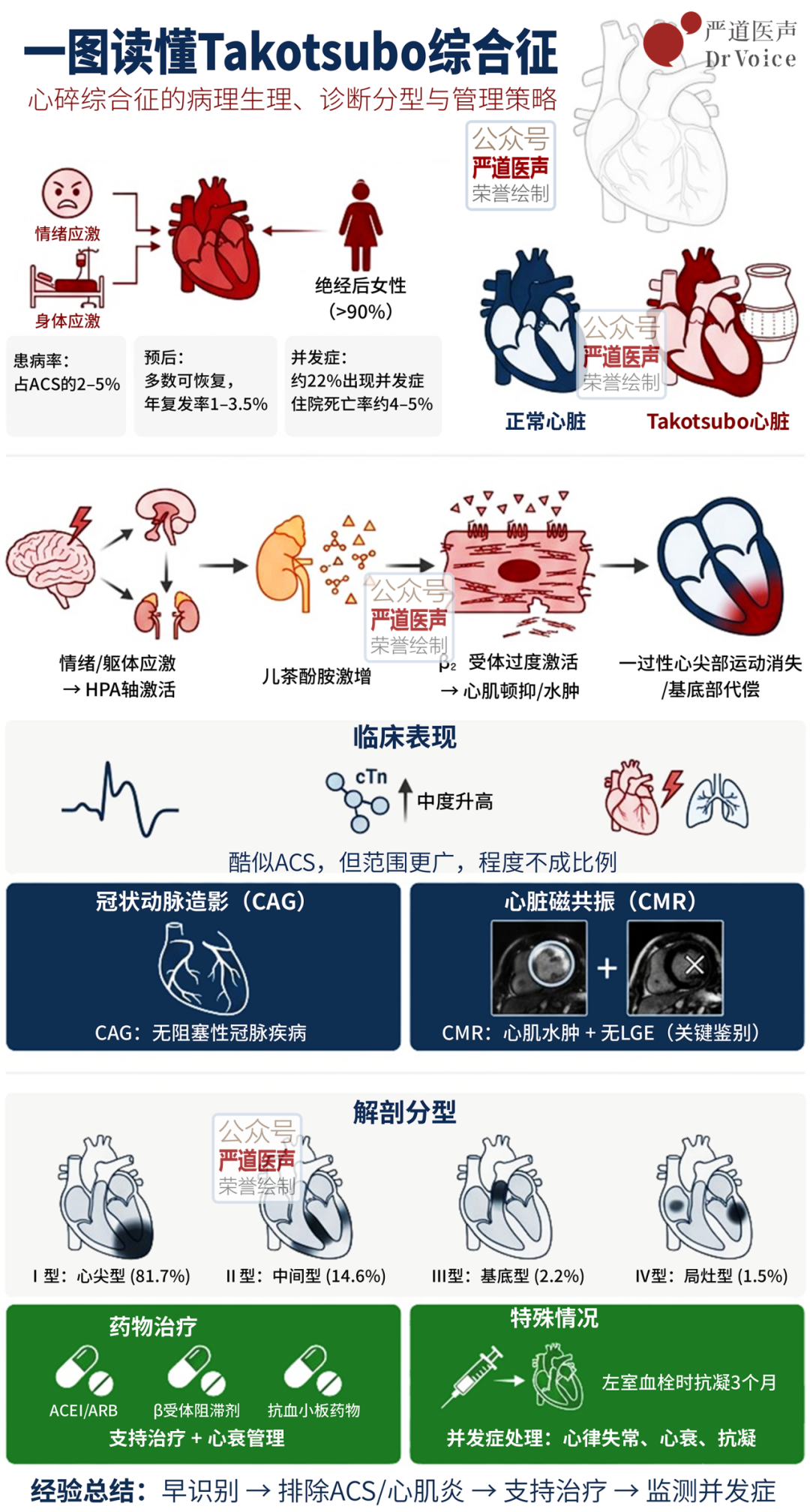
在CCU的日常工作中,我们时常面对各种急性冠脉综合征(ACS)的鉴别诊断。Takotsubo综合征(又称应激性心肌病)以其可逆的左心室心尖部气球样变和基底段过度收缩为特征,通常预后良好。然而,当这种良性疾病与一种常见的冠状动脉解剖变异——心肌桥(myocardial bridge)共存时,却可能酿成致命的并发症:心脏破裂。

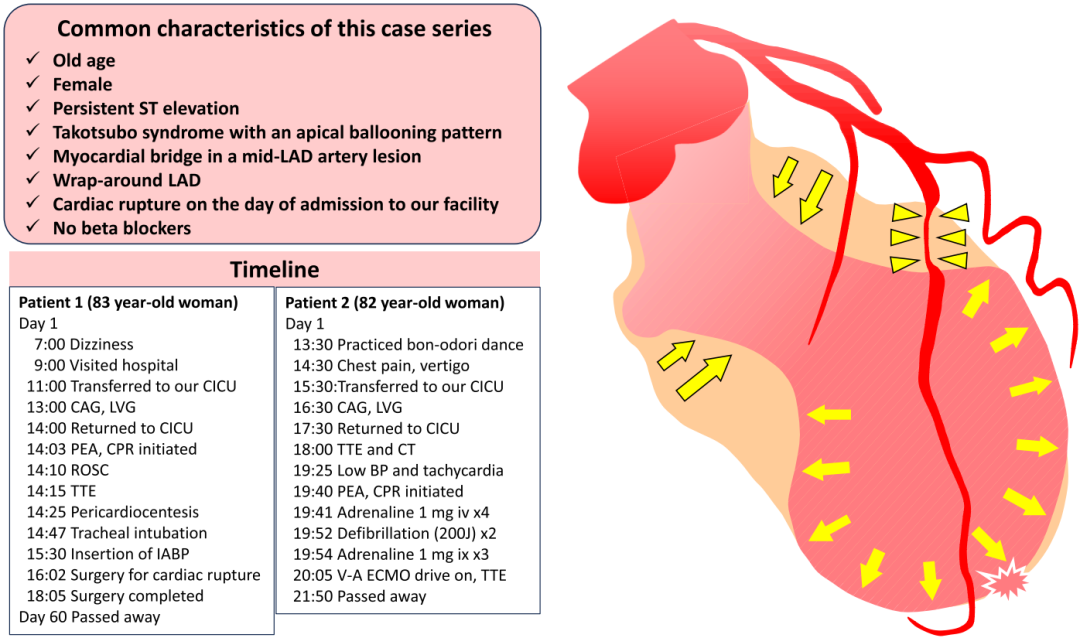
发表于《Eur Heart J Case Rep》的一篇病例系列报告“Cardiac rupture due to Takotsubo syndrome complicated by a myocardial bridge: a case series”,描述了两例因Takotsubo综合征合并心肌桥导致心脏破裂的老年女性患者,为我们敲响了警钟。
01
病例摘要
患者1
83岁女性,主诉头晕。因心电图显示V1–4导联ST段抬高,疑似ST段抬高型心肌梗死(STEMI)转入CCU。
患者既往有高血压和糖尿病,服用血管紧张素转换酶抑制剂和降糖药物。体格检查无异常。
急诊冠状动脉造影(CAG)显示前降支(LAD)中段因心肌桥出现收缩期挤压现象。
左心室造影(LVG)显示心尖部气球样变伴血栓形成,基底段过度收缩,符合Takotsubo综合征诊断(图1)。
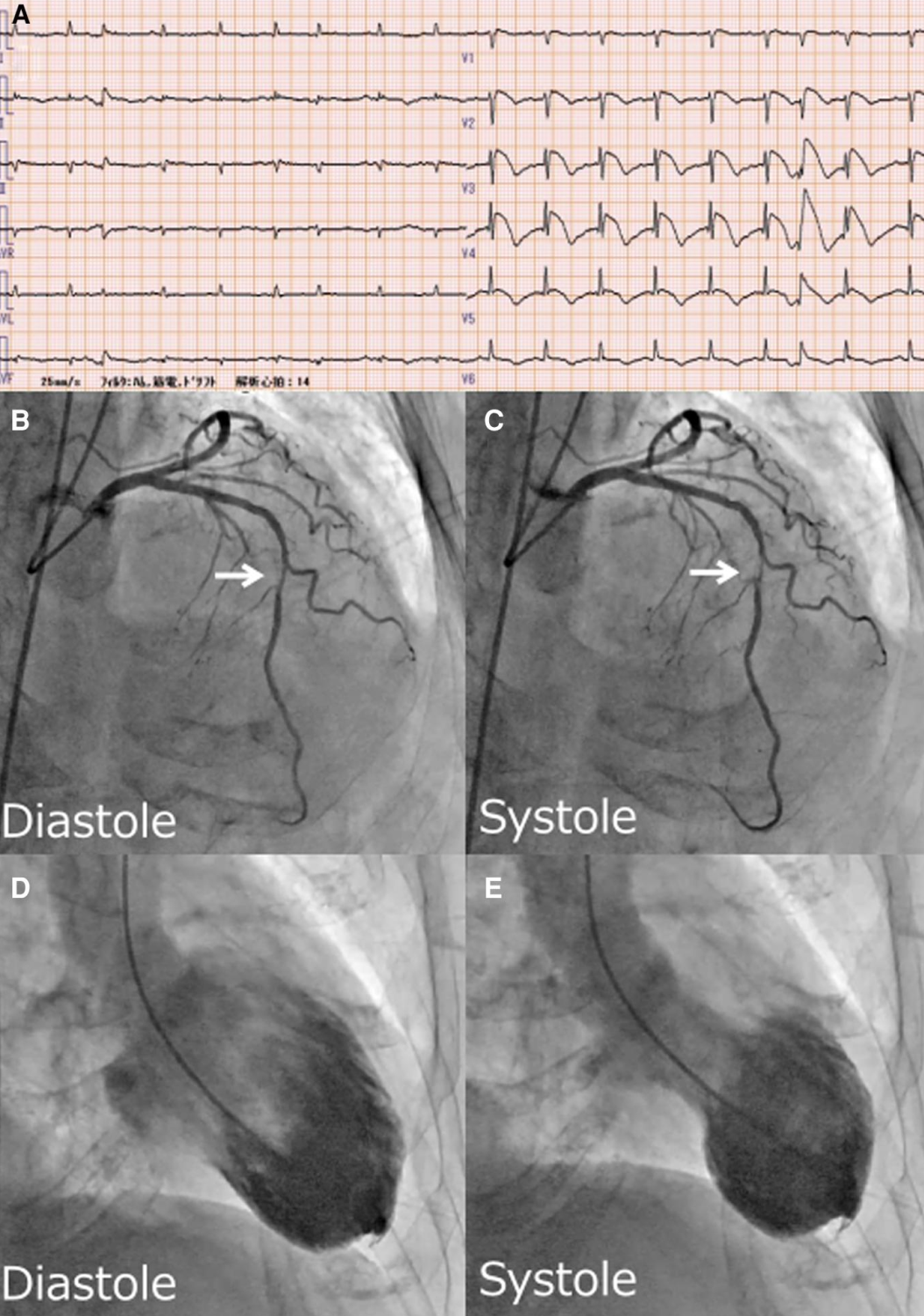
图1患者1的心电图与影像学发现。
图1A:患者1入院时心电图显示V1–4导联ST段抬高。 图1B、C:患者1冠状动脉造影显示LAD中段心肌桥(箭头示收缩期挤压)。 图1D、E:患者1左心室造影显示基底段过度收缩和心尖部气球样变。
检查结束后,患者血压突然下降,出现无脉性电活动(PEA)。心肺复苏(CPR)后恢复自主循环(ROSC)。
超声心动图显示大量心包积液,提示心脏破裂导致心脏骤停。紧急心包穿刺后血压趋于稳定。术后康复过程平稳,但患者在第60天死于吸入性肺炎导致的呼吸衰竭。
患者2
82岁女性,主诉运动时胸痛。
心电图显示II、III、aVF及V3–5导联ST段抬高,据此怀疑为STEMI。
患者无特殊病史,目前未服用任何药物。体格检查无异常。
急诊CAG显示LAD中段存在心肌桥的压迫效应,LVG显示心尖部运动消失、基底段过度收缩,诊断为Takotsubo综合征(图2)。
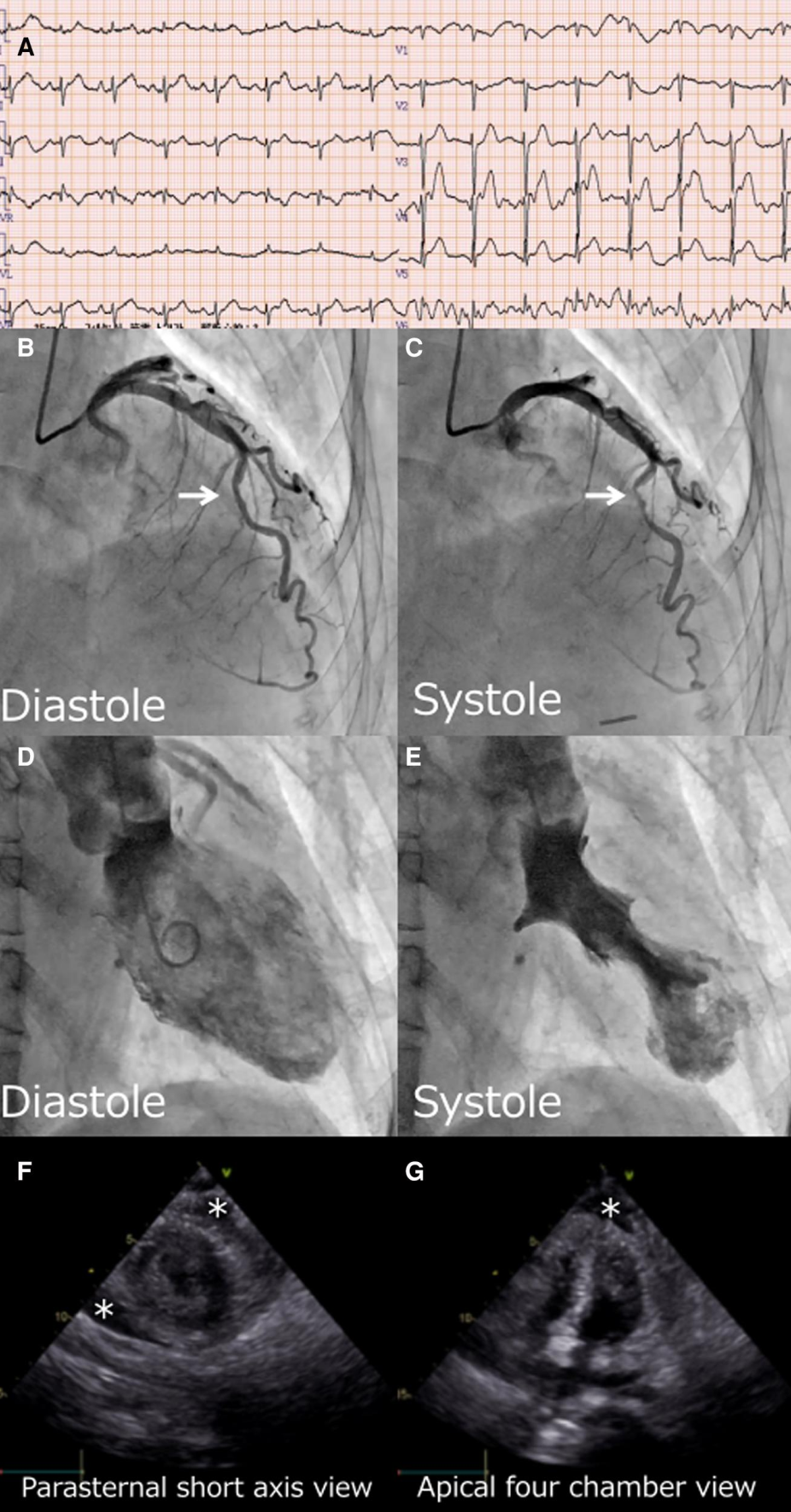
图2患者2的心电图与影像学发现。
图2A:患者2入院时心电图显示II、III、aVF及V3–5导联ST段抬高。图2B、C:患者2冠状动脉造影显示LAD中段心肌桥(收缩期挤压)。图2D、E:患者2左心室造影显示基底段过度收缩和心尖部气球样变。图2F、G:患者2超声心动图显示大量心包积液(*标记处)。
造影术后2小时,患者血压骤降,随后出现呕吐和PEA。
紧急CPR未恢复自主循环,故启动静脉-动脉体外膜肺氧合(VA-ECMO)。
超声心动图显示大量心包积液(图2F、G),提示心脏破裂为心脏骤停原因。
因患者高龄,家属拒绝手术干预,患者当日死亡。
02
讨论
Takotsubo综合征的特征是左心室短暂性区域收缩功能障碍,主要累及心尖部,临床表现类似心肌梗死,但冠状动脉造影无阻塞性冠心病或急性斑块破裂的证据。尽管其预后总体良好,但心脏破裂是一种罕见(发生率约1.8%)且致命的并发症,其病理生理机制尚不完全清楚。
心肌桥是指原本走行于心肌表面的冠状动脉段被心肌覆盖(即壁内走行),最常见于LAD中段。尸检发现率约50%,但血管造影检出率仅0.4%–15.8%,因为造影只能间接观察到收缩期“挤奶效应”(squeezing phenomenon)。心肌桥患者长期预后通常良好,但偶有报道增加心肌缺血、心绞痛、心肌梗死、致命性心律失常、猝死以及Takotsubo综合征的风险。
心脏破裂的发生率与危险因素
左心室游离壁破裂在Takotsubo综合征中的发生率为0.2%–1.8%,死亡率高达81%。尽管机制未明,但潜在的危险因素包括:儿茶酚胺介导的心肌损伤、高肾上腺素能状态加重需求性缺血、心腔内压力梯度,以及心尖部气球样变与基底段过度收缩在铰链点(hinge point)处产生的过度室壁应力。
女性、高龄、持续性ST段抬高、高血压、射血分数保留以及心脏负荷增加为Takotsubo综合征患者心脏破裂的危险因素。
当心肌桥邂逅Takotsubo综合征
本报告的两例患者均具备上述多项危险因素(女性、高龄、心尖型),同时合并LAD心肌桥。
血流动力学研究显示,有症状的心肌桥可导致收缩期和舒张期血管直径持续狭窄,并降低血流储备。在Takotsubo综合征急性期,冠状动脉血流储备受损和微血管阻力增加也很常见。因此,两者共存可能协同加重缺血,尤其是当心肌桥位于LAD中段时。
此外,当包绕型LAD同时供应心尖部和下壁,可能导致更广泛的心尖部气球样变,进一步增加局部室壁应力,从而易发生心脏破裂。
既往文献与本文差异
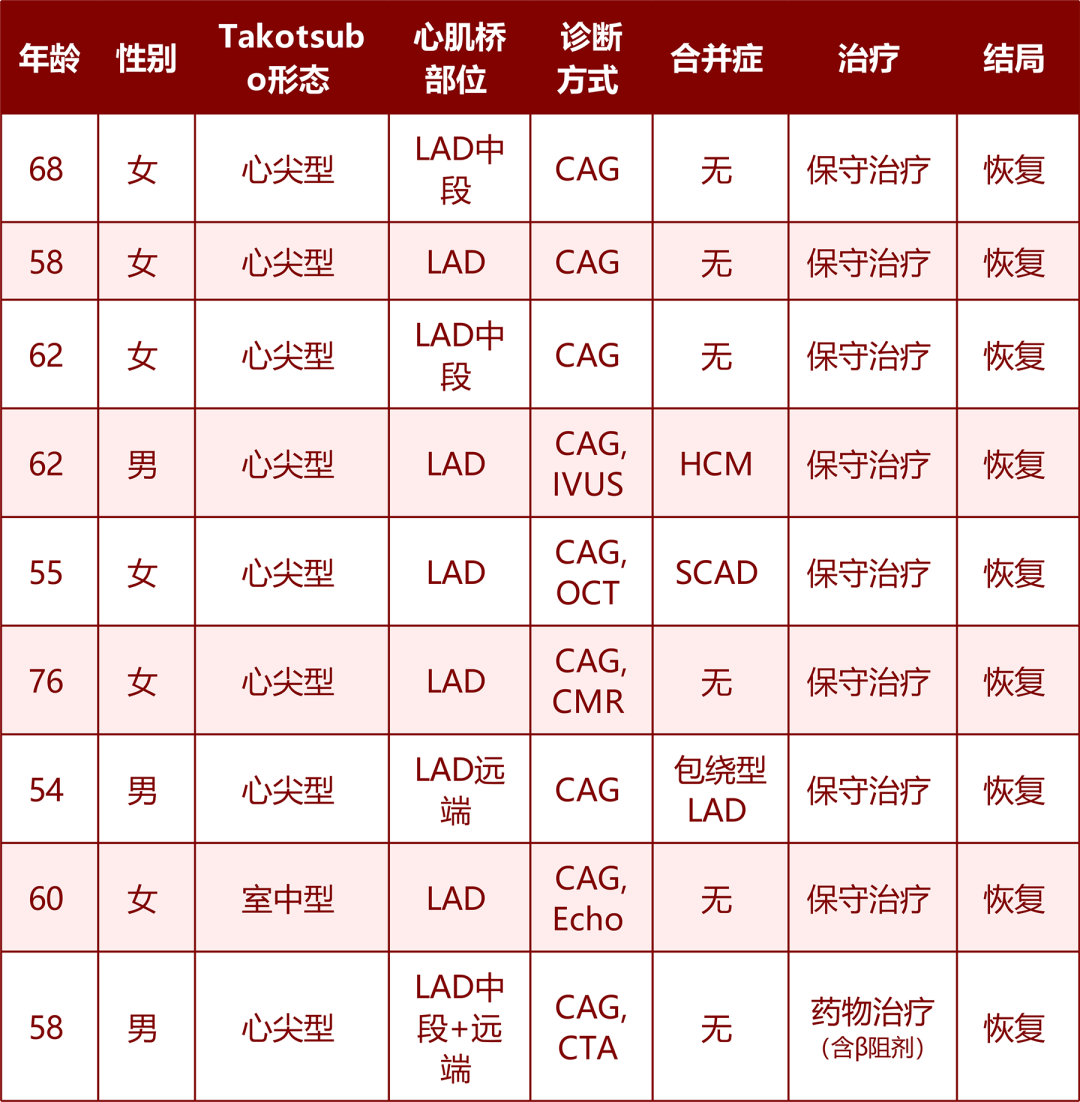
既往报告(表1)中,Takotsubo综合征合并心肌桥的患者预后普遍良好,而本文两例均死于心脏破裂。这提示,尽管大多数此类患者预后良好,但结构脆弱性与过度肾上腺素能刺激的组合可能具有灾难性后果。β受体阻滞剂理论上可通过减弱交感神经驱动和降低室壁应力来减少破裂风险,但在血流动力学不稳定的老年患者中临床应用仍具挑战。
表1 Takotsubo综合征合并心肌桥病例汇总
严道心得
读完这篇病例系列,我的第一反应是后怕。
在临床工作中,我们遇到Takotsubo综合征患者时,往往因为其可逆性而放松警惕,尤其是当冠状动脉造影未见阻塞性病变时,容易认为患者已脱离危险。
然而,这篇文献提醒我们:心肌桥这个看似良性的解剖变异,在Takotsubo综合征的急性期可能成为压垮骆驼的最后一根稻草。
宁可信其有!
两位老年女性患者,均表现为典型的STEMI样心电图改变,造影仅发现心肌桥而无阻塞性病变,左心室造影证实心尖部气球样变——这几乎是教科书级别的Takotsubo综合征诊断流程。但随后发生的循环崩溃、心包填塞,以及最终死亡,让所有参与救治的医生措手不及。
从病理生理角度看,心肌桥导致的收缩期挤压不仅影响血流,还可能引起局部心肌缺血和纤维化,使得心尖部在儿茶酚胺风暴中更加脆弱。而包绕型LAD使得心尖部缺血范围更大,室壁应力更集中。
这让我联想到一个临床细节:对于Takotsubo综合征患者,如果造影发现LAD中段心肌桥,尤其是伴有LAD包绕心尖征象时,是否应该更积极地监测心包积液?是否应该更早地考虑使用β受体阻滞剂(在血流动力学允许的情况下)?是否应该将这类患者列为心脏破裂的高危人群,并提前与家属沟通风险?
当然,本文仅为两例病例报告,无法得出普遍性结论。但我们或许可以推测:少数具有特定解剖特征和临床特征的患者,可能处于心脏破裂的高风险中。未来需要更大样本的观察性研究来验证这一假设。
最后,我想强调一点:在重症监护室,任何看似良性的诊断都不应让我们放松警惕。