
【据《Circulation》2022年7月报道】:基于ECG机器学习的复合终点模型可识别未确诊、具有临床意义的结构性心脏病,它优于单一疾病模型,具有较高的阳性预测值,有更好临床实用性。该方法可促进超声心动图的靶向筛查,从而改善结构性心脏病的漏诊率。(作者Alvaro E. Ullo-Cerna等)
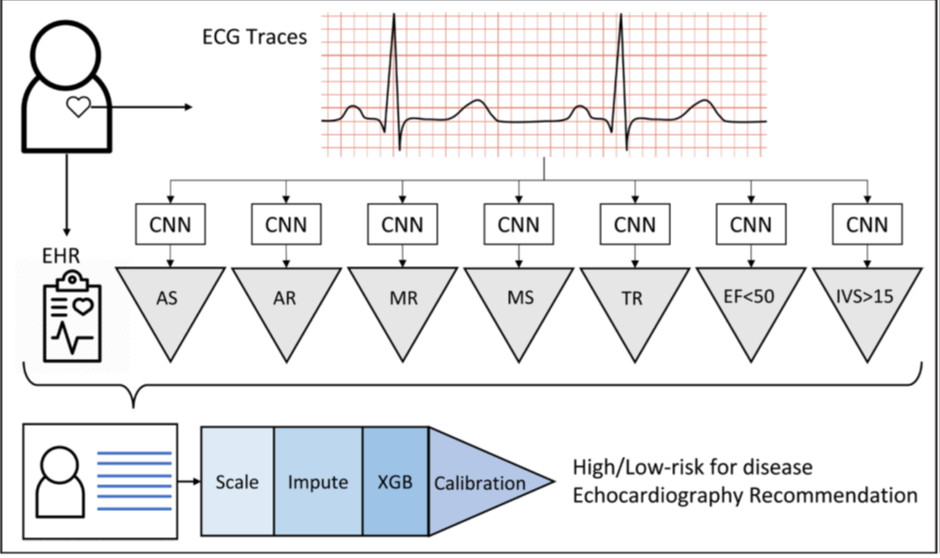
rECHOmmend 模型图显示了ECG轨迹和其它电子病例记录数据的分类传递途径
每个应用于ECG轨迹数据的CNN输出串联了实验室指标、生命体征及人口学统计特征形成特征向量。特征向量输入模型进行分类(最小-最大分级、平均估算、XGBoost分类器以及校正),最后产生疾病的复合预测。AR,主动脉瓣反流;AS,主动脉瓣狭窄;CNN,卷积神经网络;ECG,心电图;EF,射血分数;EHR,电子病历;IVS,室间隔;MR,二尖瓣反流;MS,二尖瓣狭窄;TR,三尖瓣反流。
结构性心脏病患者有较高的致残、致死风险,超声心动图可提供重要的诊断、预后和管理的循证学指征。心脏超声是许多结构性心脏病的主要诊断检查,包括瓣膜性疾病,左室收缩功能不全,以及各型心肌病。尽管结构性心脏病的循证学诊疗方法和心脏超声的应用不断增加,但是临床中仍然存在诊断不充分,漏诊的发生。研究显示,百万级别的患者存在诊断不充分,此外还有很多患者在出现不良事件或不可逆并发症时才被诊断。及时诊断结构性心脏病可改善患者预后。虽然心脏超声筛查不具有实用性,但基于ECG的预测模型可帮助识别目标高危患者。
Alvaro E.等人开发了一项新型基于ECG的机器学习方法以预测多种结构性心脏病,复合终点模型可获得更高的患病率和阳性预测值,给予有临床价值的超声心动图建议。同时利用该模型模拟大规模回顾性数据集以评估其应用于临床的预期真实世界表现。
使用1984年至2021年间484765名成年人的电子病例和超声心动图报告相关联的2232130份心电图,训练机器学习模型来预测存在或不存在7种心脏瓣膜病(1年内的超声心动图确认)。 复合终点包括:中度或重度瓣膜病(主动脉/二尖瓣狭窄或反流、三尖瓣反流)、射血分数降低<50%或室间隔厚度>15毫米。 同时测试了各种输入特征(人口统计学特征、实验室值、结构化ECG数据、ECG轨迹)的组合,并使用5折交叉验证、在1个站点上训练并在10个独立站点上测试的多站点验证以及在2010 年之前数据集模拟训练,并应用在2010 年数据集。结果显示, rECHOmmend复合模型使用了年龄、性别和 ECG 轨迹,接受者操作特征曲线下面积(AUROC)为 0.91, 90%灵敏度的阳性预测值(PPV)为42%,复合终点患病率为 17.9%。个体疾病模型的AUROC为0.86至0.93,阳性预测值更低从 1% 到 31%。使用不同输入特征模型的AUROC从 0.80 到 0.93 不等,并随附加特征的增加而增加。多站点验证显示与交叉验证相似的结果,在单站点训练后,10个临床站点的独立测试集中,AUROC总面积为 0.91。回顾性模拟测试表明,对于 2010 年没有结构性心脏病的患者中获得的心电图,11% 被归类为高风险,41%(占患者总数的 4.5%)在1年内发展为超声心动图确诊的心脏病瓣膜病。因此,研究者认为,基于ECG机器学习的复合终点模型可识别未确诊、具有临床意义的结构性心脏病,它优于单一疾病模型,具有较高的阳性预测值,有更好临床实用性。该方法可促进超声心动图的靶向筛查,从而改善结构性心脏病的漏诊率。
山西省心血管病医院心内科 王飞 报道
Circulation, 2022, 146: 36-47.

扫描二维码,马上进入“瓣月谈”